
【题目】铝是大自然赐予人类的宝物,是现代文明不可缺少的物质基础。
(1)人类冶炼和使用金属铝的时间较晚。可能是因为______(填字母)。
a.地壳中铝元素含量少
b.冶炼铝的技术要求高
(2)用铝锂合金制造“神舟号”航天飞船的一些部件,主要是利用其强度高、耐腐蚀和____(写一条)等性质。高温下,铝与Li2O反应可置换出金属锂,写出该反应的化学方程式:_____。
(3)用砂纸去除铝片表面的氧化膜,将其浸人硫酸铜溶液中,一段时间后,观察到铝片表面有红色物质析出,并有气泡产生,经检验气体为氢气。
①写出生成红色物质的化学方程式:_________。
②硫酸铜溶液中的阳离子有_________(填离子符号)。
(4)原子簇是若干个原子的聚集体,有望开发成新材料。某铝原子簇由13个铝原子构成,其最外层电子数的总和为40时相对稳定。写出该稳定铝原子簇的微粒符号:________。(铝原子的结构示意图为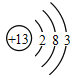 )
)
【答案】b 密度小(质轻等) 
![]() Cu2+和H+
Cu2+和H+ ![]()
【解析】
(1)铝是地壳中含量最多的金属元素,人类冶炼和使用金属铝的时间较晚,可能是因为冶炼铝的技术要求高,故选b。
(2)铝锂合金具有强度高、耐腐蚀和密度小等性质。高温下,铝与Li2O反应可置换出金属锂和氧化铝,该反应的化学方程式 。
。
(3)①铝和硫酸铜溶液反应,生成硫酸铝和铜,其化学方程式:![]() 。
。
②有氢气产生,说明金属铝和硫酸反应,则硫酸铜溶液中的阳离子有Cu2+和H+。
(4)某铝原子簇由13个铝原子构成,这粒子符号的右下角应为13,每个铝原子的最外层电子数为3,若最外层电子数的总和为40时相对稳定,则该粒子应带1个单位的负电荷,该稳定铝原子簇的微粒符号:![]() 。
。


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:
【题目】菱镁矿中主要含MgCO3、FeCO3和SiO2。以菱镁矿为原料制取镁的工艺流程如下。
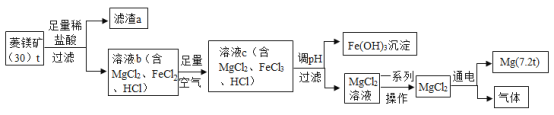
回答下列问题:
(1)菱镁矿属于___(选填“纯净物”或“混合物”)。
(2)流程中滤渣a主要成分是___。
(3)写出菱镁矿中MgCO3与稀HC1反应的化学方程式___。
(4)溶液b→溶液c反应的化学方程式为:![]() (补充完方程式)____。
(补充完方程式)____。
(5)溶液c调pH使Fe2+完全沉淀为Fe(OH)3从而与Mg2+分离,则调pH的范围应为2.8-__。
已知:物质沉淀的pH见下表:
物质 | Mg(OH)2 | Fe(OH)3 |
开始沉淀的pH | 8.9 | 1.5 |
完全沉淀的pH | 10.9 | 2.8 |
(6)结合流程中的数据计算。
①菱铁矿中镁元素的质量分数为_____(不考虑整个流程转化中的损失)。
②MgCl2通电制得的气体的质量____(写出计算过程)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请根据如图甲、乙、丙三种固体物质的溶解度曲线,回答下列问题。
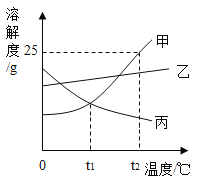
(1)在___℃时,甲、丙两种物质的溶解度相等;
(2)在t2°C时,向盛有25g甲物质的烧杯中加入50g水,充分溶解后,所得溶液的溶质质量分数为_____;
(3)若乙物质中混有少量甲物质,最好采用____(填"降温结晶'或“蒸发结晶")的方法提纯;
(4)t2°C时,甲、乙、丙三种物质的饱和溶液各100g,所含溶剂的质量由大到小的顺序是____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】人类社会需要充足的能源,良好的环境。
(1)我国南海蕴藏着丰富的“可燃冰”能源,“可燃冰”的成分是甲烷水合物,可燃冰属于_____能源(填“可再生”或“不可再生”)。
(2)PM2.5是我国测定空气质量的重要指标,下列措施中能降低空气中PM2.5含量的是___(填字母)。
A 化工厂加高烟囱 B 禁止焚烧秸秆 C 植树造林
(3)酸雨也是重要的环境问题之一。酸雨的pH___5.6 (填“>”、“<”或“="),形成酸雨的主要物质是含硫煤燃烧所产生的______气体(填化学式)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】兴趣小组设计实验探究氢氧化钠的性质,请你参与他们的探究。
(实验过程与分析)
实验一 | 实验二 | 实验三 | |
实验操作 |
|
|
|
实验现象 | __________ | __________ | 无明显现象 |
实验结论 | 氢氧化钠能与硫酸铜发生反应 | 氢氧化钠能与氯化铵发生反应 | 氢氧化钠不能与硫酸发生反应 |
(1)实验一的现象:___________。
(2)实验二的现象:__________。
(实验反思与拓展)
(3)实验一中发生反应的化学方程式: _____。
(4)某同学认为实验三的结论不正确,他改进了该实验方案:先向氢氧化钠溶液中滴入几滴酚酞溶液并振荡,再滴入稀硫酸,观察到溶液由____色变为无色,由此可知氢氧化钠与稀硫酸确实发生了反应,该反应的化学方程式为__________。
(5)由实验三联想到二氧化碳通入到氢氧化钠溶液中也没有明显现象,那么二氧化碳与氢氧化钠是否发生了化学反应呢? (本实验中忽略CO2溶于水)
①甲同学设计了如图所示实验方案,当观察到_________现象时,说明两者发生了化学反应。
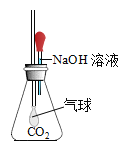
②乙同学重新设计实验方案:取NaOH溶液于试管中,通入少量CO2,然后向所得溶液中加入____溶液,当观察到_____现象时,也能证明二氧化碳与氢氧化钠发生了化学反应。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】钢铁的腐蚀是重要研究课题。
(知识回顾)用如图所示实验进行铁钉腐蚀的研究。一段时间后试管A、B中铁钉几乎没有生锈,而试管C中铁钉明显锈蚀,试管D、E中铁钉严重锈蚀。

(1)由A、B、C的现象可知,铁的锈蚀是铁跟________________(填化学式)等物质作用的过程。
(2)试管B中使用“煮沸并迅速冷却的蒸馏水”,其目的是________________。
(实验探究)向试管D中(含生锈铁钉)加人过量10%稀盐酸,浸泡。可观察到铁锈逐渐消失,铁钉表面有气泡产生,溶液呈黄色,一段时间后黄色变为浅绿色。
(3)写出铁锈溶于盐酸的化学方程式:________________。
(4)推测试管D中溶液由黄色变为浅绿色,可能是因为氯化铁与某些物质发生反应所致。现进行如下3个实验(持续10小时,已知氢气不影响该反应)。
序号 | 实验I | 实验Ⅱ | 实验Ⅲ |
实验内容 |
|
|
|
现象 | 溶液颜色始终呈黄色 | 产生红褐色沉淀 | 溶液逐渐由黄色变浅绿色 |
①设计实验I的目的是________________。
②综合分析上述3个实验,试管D中溶液由黄色变为浅绿色的原因是__________。
(拓展延仲)研究水样的pH、水中溶解氧浓度与钢铁腐蚀速率的关系。查阅相关文献得到如下资料。
(5)如图表示水样温度22℃、氧含量6mL·L-1时,钢铁腐蚀速率与水样pH的关系。当pH<4时,钢铁腐蚀速率明显增大的原因是___________________。

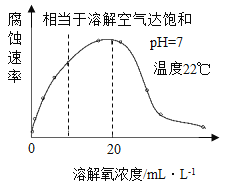
(6)如图表示温度22℃、pH=7时,钢铁腐蚀速率与水中溶解氧浓度的关系。当溶解氧超过20mL·L-1时,钢铁腐蚀速率明显下降的原因可能是________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(1)下图为实验室制取并收集气体的装置图,回答下列问题。
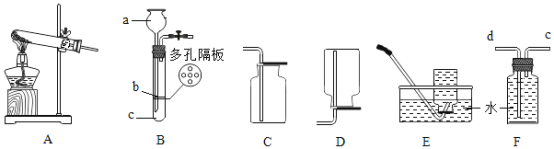
①a仪器的名称是___________。
②实验室用高锰酸钾制取并收集干燥的氧气应选用的装置组合是________(填序号)。
③若用F装置收集并测量氧气的体积,应在________(填“d”或“e”)段连接量筒。
④实验室制取二氧化碳的化学方程式是_________,用B装置制取二氧化碳便于控制反应的发生与停止,制取时应将大理石放在________(填“b”或“c”)。
(2)某化学兴趣小组在学完金属活动性顺序相关知识后,他们做了钠与硫酸铜溶液反应的实验,发现并没有铜生成,而是产生蓝色沉淀和少量黑色物质。于是他们进行了如下探究:
(实验探究1)取一块绿豆大小的金属钠,放入盛有20mL蒸馏水的烧杯中,发现金属钠浮在水面上,熔化成一个闪亮的小球并四处游动,发出嘶嘶的响声,收集反应产生的气体,发现该气体能燃烧。
(实验探究2)在上述反应所得溶液中滴加硫酸铜溶液,产生蓝色絮状沉淀。
(实验探究3)将蓝色絮状沉淀加热得到黑色固体。
(查阅资料)①钠在常温下能与水剧烈反应,生成一种碱和一种气体。②氢氧化铜受热易分解。③氧化铜为黑色固体。
(问题分析)①写出钠与水反应的化学方程式___________,点燃反应产生的气体前一个先____________。
②写出产生蓝色絮状沉淀的化学方程式____________。
(实验结论)在金属活动性顺序中,活动性较强的金属____________(填“一定”或“不一定”)能将位于其后面的金属从它们的盐溶液中置换出来。
(反思与交流)钠与硫酸铜溶液反应产生少量黑色物质的可能原因是____________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小雨同学为验证镁、铁、锌三种金属的活动性,进行了下图所示实验:
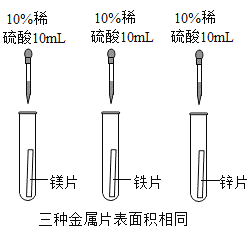
①实验中,小雨观察到的现象是_____________,由此得出三种金属的活动性:镁>锌>铁;
②小明还补充了铁片与硫酸铜溶液反应的实验,实验中观察到的现象是______________,有关反应的化学方程式为____________。由此得出铁、铜两种金属的活动性:铁_____________铜(填“>”“=”“<”)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学就在我们身边,人类的衣、食、住、行都离不开化学。
(1)如图是某服装标签的部分内容。面料和里料中属于合成纤维的是______。

(2)某学校的早餐饼配料表见图,其中富含蛋白质的物质是_____;当衣服上沾有花生油时,可用洗涤剂除去,是由于洗涤剂对花生油有______作用。

(3)钢和玻璃都是重要的建筑材料。
①钢中含有的主要元素是_______。
②普通玻璃是以纯碱、石灰石和石英砂为原料制得。纯碱的化学式为_______。
(4)目前,多数汽车使用的燃料是汽油和柴油。下列说法不正确的是_______。
a 石油炼制可获得汽油和柴油,汽油和柴油属于可再生能源
b 在汽油中加入适量乙醇作汽车燃料,可减少汽车尾气的污染
c 氢能源代替汽油和柴油作汽车燃料,具有放热多,无污染等优点
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com