

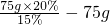 =25g,则加水的体积为:
=25g,则加水的体积为: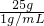 =25mL;由于量取水时是仰视液面,会导致量取的水的体积比25mL要多,即加水加多了,因此会导致溶液中溶质的质量分数变小;故答案为:25,小于
=25mL;由于量取水时是仰视液面,会导致量取的水的体积比25mL要多,即加水加多了,因此会导致溶液中溶质的质量分数变小;故答案为:25,小于

科目:初中化学 来源: 题型:
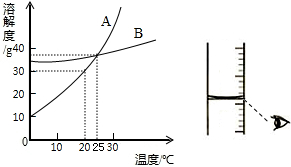
查看答案和解析>>
科目:初中化学 来源:2008年黑龙江省哈尔滨市南岗区中考化学三模试卷(解析版) 题型:选择题
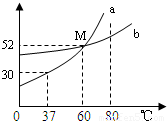
查看答案和解析>>
科目:初中化学 来源:2010年山东省泰安市新泰市第一教研区中考化学模拟试卷(二)(解析版) 题型:选择题
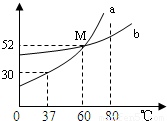
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com