
【题目】已知A、B、C、D、E是初中化学常见的物质。A是胃酸的主要成分,D是一种钠盐,广泛用于玻璃、造纸、纺织和洗涤剂的生产,C、E为氧化物。它们间的相互关系如图所示(“—”表示两种物质能发生化学反应,“→”表示两种物质间的转化关系,部分反应物、生成物及反应条件已略去)。请回答。
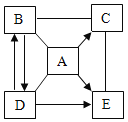
(1)E的化学式是_____;C的一种用途是_____。
(2)若A→E反应生成黄色溶液,写出该反应的化学方程式_____。
(3)D→B反应的化学方程式是_____。
【答案】H2O 灭火或气体肥料(合理即可) Fe2O3+6HCl=2FeCl3+3H2O或3HCl+Fe(OH)3=FeCl3+3H2O(合理即可) Ca(OH)2+Na2CO3=CaCO3↓+2NaOH
【解析】
A、B、C、D、E是初中化学常见的物质,A是胃酸的主要成分,A是盐酸,D是一种钠盐,广泛用于玻璃、造纸、纺织和洗涤剂的生产,D是碳酸钠,C、E为氧化物,B和碳酸钠可以互相转化,氢氧化钠与二氧化碳反应生成碳酸钠和水,氢氧化钙和碳酸钠生成碳酸钙和氢氧化钠,B是氢氧化钠,C是二氧化碳,E是水。
(1)B和碳酸钠可以互相转化,B是氢氧化钠,C是二氧化碳,E是水,E的化学式是H2O;C的一种用途是灭火或气体肥料。
(2)若A→E反应生成黄色溶液,反应是氧化铁和盐酸生成氯化铁和水,盐酸和氢氧化铁生成氯化铁和水,该反应的化学方程式为Fe2O3+6HCl=2FeCl3+3H2O或3HCl+Fe(OH)3=FeCl3+3H2O。
(3)D→B反应是氢氧化钙和碳酸钠生成碳酸钙和氢氧化钠,反应的化学方程式是Ca(OH)2+Na2CO3=CaCO3↓+2NaOH。


 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案科目:初中化学 来源: 题型:
【题目】碳酸钠、碳酸氢钠是生活中两种常见的重要的盐。
(1)碳酸钠(俗称纯碱、苏打)与碳酸氢钠(俗称_____),均为________色固体,水溶液均呈_______性,向它们的水溶液中分别滴入无色酚酞试液,酚酞试液均变红色。
(2)碳酸钠、碳酸氢钠均可与稀盐酸反应,其中碳酸钠与稀盐酸反应的化学方程式为_____。但是,碳酸钠、碳酸氢钠与稀盐酸反应产生二氧化碳的速率是否相同?校兴趣小组同学针对于此,展开探究:
(方案设计)
①甲设计的实验如图1所示,实验时,同时全部推出足量稀盐酸后,观察到图2所示现象。于是他得出______和稀盐酸反应产生二氧化碳较快的结论。

②乙同学通过计算可知:0.318 g碳酸氢钠约产生0.167 g二氧化碳,而0.318 g碳酸钠产生二氧化碳的质量为______g,等质量的碳酸钠与碳酸氢钠与足量的稀盐酸作用,碳酸氢钠产生二氧化碳的质量更多,显然甲同学的设计不妥,应取含碳元素质量相同的碳酸钠和碳酸氢钠进行实验。若碳酸钠的质量仍为0.318g,应称取碳酸氢钠的质量为_______g。
③小组同学在老师指导下设计了图3所示实验。连通管除消除稀盐酸滴入占有体积引起的误差,还有______的作用。
分别取等体积、含碳元素质量相同的碳酸钠和碳酸氢钠稀溶液(各滴2滴酚酞溶液)以及相同体积、相同浓度的足量稀盐酸进行实验。实验时,广口瓶内压强随时间变化如图4所示,溶液颜色变化记录如表1。
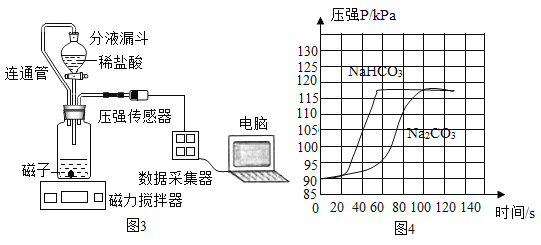
表1:
滴入酚酞溶液 | 滴入稀盐酸,溶液颜色变化 | |
碳酸钠溶液 | 红色 | 红色→浅红色→无色 |
碳酸氢钠溶液 | 浅红色 | 淺红色→无色 |
(实验结论)分析图4所示的实验数据可得到:相同条件下,碳酸氢钠与稀盐酸反应产生二氧化碳速率更快,你判断的理由是_______。
(实验反思)小组同学分析表1实验现象和图4数据,得出碳酸钠能与稀盐酸反应产生二氧化碳,反应是分步进行的。第一步发生的化学反应方程式是:_______,第二步发生的反应是:NaHCO3+HCl=NaCl+H2O+CO2↑。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图为测定空气中氧气含量的实验装置,下列做法合理的是( )
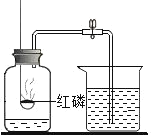
A.用足量的红磷进行实验
B.实验开始前不需要检查装置的气密性
C.红磷熄灭后,立即打开止水夹
D.用木炭代替红磷进行实验
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学实验室现有一包固体混合物A,它可能由Fe、Cu、CuO、Ca(OH)2、Na2CO3五种物质中的三种或多种组成。某化学兴趣小组的同学欲探究其成分组成,他们按下图所示进行了实验探究,出现的现象如图中所述。(设过程中所有可能发生的反应都恰好完全进行)
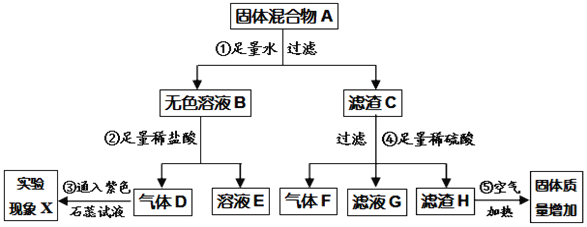
根据上述信息,试回答下列问题:
⑴现象X中,气体D使紫色石蕊试液变成了_____色;无色气体F是_____(写化学式)。
⑵溶液E中一定大量存在的金属阳离子为_____(写离子符号)。
⑶写出步骤②中发生反应的化学方程式:_____。
⑷写出步骤⑤中发生反应的化学方程式:_____。
⑸根据上述信息,可推知固体混合物A中一定存在的物质是(写化学式)_____。
⑹根据上述信息,固体混合物A中仍然不能确定的物质是(写化学式)_____,你的理由是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某白色固体甲的主要成分为NaCl,可能含有MgCl2、KCl、BaCl2和NaOH中的一种或几种杂质,为检验白色固体甲的成分并除去其中杂质,进行如下实验:

(1)写出生成白色固体丙的化学方程式_________________;
(2)向无色溶液D中加入过量稀盐酸的目的是__________________;
(3)分析上述实验可知,白色固体甲中一定没有的物质是______________________;
(4)取溶液无色溶液A、B、C、D的一种,分别滴加到稀硫酸和NaOH溶液样品中,就能把二者鉴别开来的是无色溶液________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】氧化铜与稀盐酸发生反应时,容器中溶液总质量随时间的变化曲线如图所示。下列说法错误的是
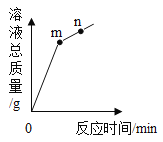
A. 该实验是将稀盐酸逐渐加入到盛有氧化铜的容器中
B. m点表示氧化铜与稀盐酸恰好完全反应
C. m点和n点对应溶液中铜元素的质量不相等
D. m点和n点对应溶液蒸发结晶后得到的固体成分相同
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在化学世界里没有生命的阿拉伯数字也变得鲜活起来,它们在不同的位置表示着不同的含义.下列化学符号中数字“2”表示的意义正确的是
A.Mg2+:一个镁离子带2个单位正电荷B.CO2:二氧化碳中含有2个氧原子
C.2H:2个氢元素D.![]() :氧化钙的化合价为+2价
:氧化钙的化合价为+2价
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某同学查阅资料得知,实验室常用电石(主要成分是CaC2)与水反应制取乙炔(C2H2),反应的化学方程式为CaC2 +2H2O==Ca(OH) 2 +C2H2↑(电石中的杂质不溶于水且不与水反应,也不与Na2CO3溶液反应)。在实验室中,该同学把一定量的CaC2加入Na2CO3溶液中充分反应后过滤,得到滤渣和滤液,并对滤液的成分进行探究。
[提出问题]滤液中溶质的成分是什么?
[猜想与假设]
猜想一:NaOH
猜想二:NaOH、Na2CO3
猜想三:NaOH、Ca(OH) 2
[实验验证]
实验序号 | 实验操作 | 实验现象 | 实验结论 |
实验一 | 取少量滤液于试管中,向其中加入过量稀盐酸 | 无气泡产生 | 猜想________不成立 |
实验二 | 取少量滤液于试管中,向其中滴加适量碳酸钠溶液 | _________ | 猜想三成立,发生反应的化学方程式为_______ |
[拓展延伸]
(1)若向CuCl2溶液中加入少量CaC2充分反应,可观察到有气泡产生,且_______。
(2)实验室保存电石应注意__________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列反应中属于置换反应的是( )
A.C+H2O![]() CO+H2B.2Na2O2+2CO2═2Na2CO2+O2
CO+H2B.2Na2O2+2CO2═2Na2CO2+O2
C.3CO+Fe2O3![]() 2Fe+3CO2D.2NaCl(熔融)
2Fe+3CO2D.2NaCl(熔融)![]() 2Na+Cl2↑
2Na+Cl2↑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com