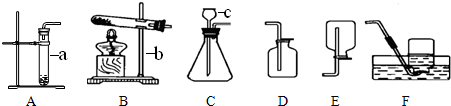
解:(1)由图中所指①指的是长颈漏斗,②指的是水槽,故答案为:长颈漏斗;水槽;
(2)因过氧化氢分解生成水和氧气,在甲和乙装置中,甲装置中的长颈漏斗的下端没有伸到液面以下,则生成的氧气可能会从长颈漏斗逸出,导致收集不到氧气,则选择乙装置可以生成气体并能收集到气体,故答案为:2H
2O
2
2H
2O+0
2↑;乙;长颈漏斗的下端未伸到液面以下;生成的气体从长颈漏斗逸出,而收集不到气体;
(3)因氧气不溶于水,可采用排水法收集,又氧气的密度比空气的大,则可采用向上排空气法收集,排空气法往往空气排不干净而导致氧气不纯,则一般采用排水法可收集到较纯净的氧气,即选择C装置可收集纯净的氧气,故答案为:氧气不溶于水;氧气的密度比空气大;C;
(4)因氧气具有助燃性,则将带火星的木条放在集气瓶口,若木条复燃则收集满,若过一段时间后用带火星的木条伸入瓶口、瓶中、瓶底,都未觅木条复燃,则可能使装置漏气,集气瓶中没有收集到氧气,所以都不能看到木条复燃,故答案为:集气瓶口;装置漏气,在集气瓶中未收集到氧气;
(5)因二氧化锰和氧化铁的质量在反应前后都没有变化,比较实验①②③可知加快了反应的进行,则它们的作用是催化作用,选择同一种催化剂时,30%浓度的过氧化氢反应用时最少,但是不便于收集,所以选用5%的.在同种浓度时,选择二氧化锰作催化剂用时间少,故答案为:催化作用;5%;过氧化氢来制取氧气可选择5%的溶液并使用二氧化锰作催化剂.
分析:(1)根据常见的仪器和仪器的名称来回答图中仪器的名称;
(2)根据反应物和生成物来书写化学方程式,比较甲和乙装置后根据氧气能否收集到来分析解答;
(3)根据氧气的溶解性和密度来分析收集方法,两种方法比较来选择收集纯净氧气的方法;
(4)根据氧气的助燃性来验满,利用收集到的氧气的量少来分析不能使木条复燃的原因;
(5)根据二氧化锰和氧化铁的质量不变化来分析在反应中的作用,根据表格中的数据来选择合适的浓度,通过对比的方法得出选择合适的催化剂和合适的浓度来解答.
点评:本题较复杂,考查学生对氧气制取的实验的掌握,学生应熟悉实验装置、物质的性质,能根据实验中的数据来分析问题、解决问题.


 2H2O+02↑;乙;长颈漏斗的下端未伸到液面以下;生成的气体从长颈漏斗逸出,而收集不到气体;
2H2O+02↑;乙;长颈漏斗的下端未伸到液面以下;生成的气体从长颈漏斗逸出,而收集不到气体;

 名校课堂系列答案
名校课堂系列答案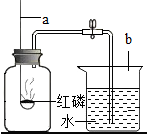 学们对竹子中的气体成分展开了探究,测定其成分.
学们对竹子中的气体成分展开了探究,测定其成分.