
科目: 来源: 题型:
【题目】2011年11月28日至12月9日,南非德班国际气候大会召开,以CO2为主的温室气体排放再次成为各国关注的焦点。则回答:
(1)《京都议定书》第一承诺期将于2012年到期,其核心内涵是减少温室气体的排放量,以控制全球的气候变暖。下列导致温室效应的主要气体是(____)
a.二氧化碳 b.氧气 c.氮气 d.氢气
(2)“碳汇”是指从空气中清除和吸收二氧化碳的过程与机制。为了应对气候变化,减少全球温室气体排放,其重要原则有:
①拒用原则。请举出低碳生活的一个实例:_____________。
②再生原则。开发和利用清洁而高效的新能源替代传统能源,如图是科学家设计的一种理想的氢元素循环模式,它实现了低碳减排,请写出(Ⅰ)中发生反应的化学方程式为______________________。
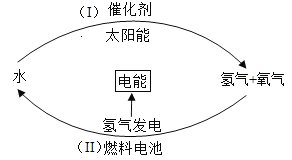
③回收原则。目前使用膜分离法从空气中分离出CO2 ,这个过程CO2发生_______(填“物理”或“化学”)变化。这些CO2可作为气体肥料,还可制造用于__________。
查看答案和解析>>
科目: 来源: 题型:
【题目】电动汽车所用电池生产和回收的管理不当也会污染环境,处理不当会导致人体血铅超标。化学电池是一类重要的能源,铅酸蓄电池是一种可充电的二次化学电池,其反应的原理用化学方程式表示为Pb+PbO2+2H2SO4![]() 2PbSO4+2H2O。则回答:
2PbSO4+2H2O。则回答:
(1)铅酸蓄电池放电时能量转变是化学能转变成____能。
(2)某铅酸电池厂生产电池用的28%的稀硫酸,将98%浓硫酸稀释配制成该稀硫酸时,正确的操作是_____________,并不断搅拌以防液体飞溅。
(3)使用铅酸蓄电池的电动车与使用汽油燃料的轻便摩托车相比,电动车的突出优点是不会产生____等温室气体,但电池对土壤和水体的污染也是不容忽视,因此要回收再利用废旧电池。
查看答案和解析>>
科目: 来源: 题型:
【题目】目前我国正大力研发电动汽车,制约电动汽车发展瓶颈的是电池的容量和性能。我国“十二五规划”确定新能源开发等七种战略性新兴产业,电动汽车使用清洁能源,有助于推广电动汽车产业。则回答:
(1)电动汽车车载的锂电池具有质量轻、电量大等优点,其中的反应有Li+MnO2=LiMnO2 ,关于该反应的说法中正确的是(____)
a.反应中MnO2是催化剂 b.反应前后Mn元素的化合价不变
c.该反应为化合反应 d.生成物Li MnO2为氧化物
(2)新型锂离子电池在新能源的开发中占有重要地位,已知锂元素(Li)的原子结构示意图为 ,则锂离子的符号为_____;
,则锂离子的符号为_____;
(3)科技人员已研制出一种新型电池即锂空气电池,它能提供相当于普通锂电池10倍的能量。该电池在放电时锂(Li)与水和空气中氧气反应生成氢氧化锂(LiOH),该反应的化学方程式是____________________。
查看答案和解析>>
科目: 来源: 题型:
【题目】研究发现燃烧排放的气体中,CO2浓度(用体积分数表示)越高,越容易被收集。与传统的燃料燃烧方式相比,化学链燃烧具有排放CO2浓度更高,易于收集的优点。下图为利用镍元素(Ni)进行化学链燃烧的原理示意图。
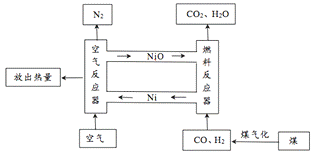
(1)空气反应器中,金属镍与氧气在一定条件下发生燃烧反应,其化学方程式为______________。
(2)燃料反应器中发生的部分化学反应如下(在高温下进行):H2+ NiO![]() Ni+H2O CO + NiO
Ni+H2O CO + NiO![]() Ni+CO2 反应前后化合价发生改变的元素有________。
Ni+CO2 反应前后化合价发生改变的元素有________。
(3)与CO、H2直接在空气中燃烧相比,化学链燃烧从燃料反应器排放出的CO2浓度更 高的原因是________。
查看答案和解析>>
科目: 来源: 题型:
【题目】数型图象是研究化学问题的一种常见描述方法,根据下列图象进行回答:
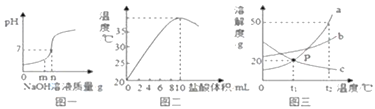
(1)图一是用盐酸和氢氧化钠进行中和反应时,反应过程中溶液的pH变化曲线.向盐酸中加入的氢氧化钠溶液质量为mg时,所得溶液中含有的离子为__________(填离子符号);
(2)图二是20℃时,取10mL10%的NaOH溶液于烧杯中,逐滴加入10%的盐酸,随着盐酸的加入,烧杯中溶液温度与加入盐酸体积的变化关系.
①由图可知中和反应是放热反应,你的依据为__________;
②甲同学用氢氧化钠固体与稀盐酸反应也能得到相同结论,乙同学认为不严密,因为__________;
(3)图三是a、b、c三种物质的溶解度曲线.a与c的溶解度相交于P点,据图回答:
①t1℃时,接近饱和的c物质溶液,在不改变溶液质量的条件下,可用_________的方法达到饱和状态;
②将t2℃时,150ga物质的饱和溶液降温到t1℃时,可以析出______物质.
查看答案和解析>>
科目: 来源: 题型:
【题目】化学与我们生产生活息息相关,请用所学知识填空.
(1)各种洗涤剂广泛进入人们的生活中,下列洗涤过程中所用洗涤剂具有乳化功能的是____________.
A.用沐浴露洗澡 B.用洗洁精清洗餐具上的油污 C.用汽油除去衣服上的油污 D.用肥皂液洗衣服
(2)随着塑料制品进入千家万户,生活中废弃的塑料垃圾越来越多,形成难于处理的环境污染物,造成所谓“__”.
(3)催化剂在生产生活中有重要作用,如在汽车上安装尾气催化转化器,将尾气中有毒的CO和NO在催化剂作用下转化为能够参与大气循环的CO2和N2.请写出该过程的化学方程式____________________.
查看答案和解析>>
科目: 来源: 题型:
【题目】青少年一定要爱护自己的眼睛,在光线不足时看书、写字要用照明工具,如图是一种照明用台灯.

(1)如图中标示的各部件中,用金属材料制成的是_______(填序号)
(2)灯管后面的反光片为铝箔,铝块能制成铝箔是利用了铝的_________性.铝制品具有很好的抗腐蚀性,原因是______________________(用化学方程式解释).
(3)若要验证铜、铁、铝的活动性顺序,某同学已经选择了打磨过的铜片和铝片,你认为他还需要的一种溶液是_________(填溶质的化学式).
(4)废弃的电器需分类回收,请简述废旧金属回收的意义是____________________.
查看答案和解析>>
科目: 来源: 题型:
【题目】实验小组进行了如下实验。
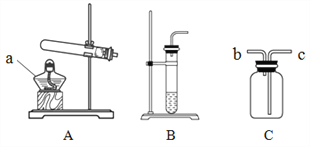
(1)写出仪器a的名称_______。
(2)实验室用装置A制取氧气的化学方程式为_______。
(3)实验室用装置B制取二氧化碳,反应的化学方程式为_______。
(4)用装置C收集二氧化碳,验满时,燃着木条应放在_____(填“b”或“c”)端。
查看答案和解析>>
科目: 来源: 题型:
【题目】根据下表信息,相关说法正确的是( )
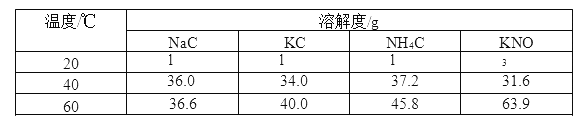
A.20℃时,NaCl 的溶液度为 36.0
B.40℃时,KCl 饱和溶液的溶质质量分数为 40%
C.40℃时,向 100g 水中加入 50gNH4Cl 充分溶解,溶液质量为 145.8g
D.60℃时降温到 20℃时,KNO3 和 KCl 的饱和溶液析出晶体较多的是 KNO3
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com