
C与D形成的常见晶体(乙),与甲晶体的熔点相比,乙________甲,其原因是________.
科目:高中化学 来源:2010年温州市省一级重点中学高一下学期期末统一测试化学试题 题型:填空题
A、B、C、D、E、F六种元素分布在三个不同的短周期,它们的原子序数依次增大,其中B与C为同一周期,D、E、F为同一周期,A与D,C与F分别为同一主族,C元素的原子最外层电子数是次外层电子数的三倍,D是所在周期原子半径最大的元素。又知六种元素所形成的常见单质在常温常压下有三种是气体,三种是固体。请回答下列问题:
(1)写出F在周期表中的位置________。画出D的离子结构示意图___________。
(2)由A、C两元素可以组成X、Y两种化合物,X在一定条件下可以分解成Y,X的电子式为_______________。1gA的单质与C的单质完全反应生成Y(Y为液态),放出142.9KJ的热量,请写出该反应的热化学方程式_______________________。
(3)C与F形成的常见化合物属于_________晶体。若E的单质是常见的半导体材料,则A与B形成的常见化合物R、C与D形成的常见化合物S、C与E 形成的常见化合物T, R、S、T三者的沸点从高到低排列为___________________________(写化学式)。
(4)画出B单质的结构式_______________。最近科学家合成出了B元素形成的B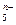 电子式
电子式 ,则n值为___ 。
,则n值为___ 。
(5)A的单质与C的单质在KOH的溶液中可以形成原电池,已知M、N均为碳电极,在电池的M极通入A的单质气体,N极通入C的单质气体,则N极的电极反应式为____________________________________。
(6)在10L的密闭容器中,通入2molFC2气体和3mol C的气体单质,一定条件下反应后生成FC3气体,当反应达到平衡时,单质C的浓度为0.21 mol·L—1,则平衡时FC2的转化率为________。
查看答案和解析>>
科目:高中化学 来源:同步题 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:
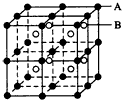
(1)由A、B两元素组成的离子晶体结构(甲)如图
所示,则该晶体的化学式是: 。
(2)C原子的最外层电子排布为nsnnpm,其某一激发态可使这两个亚层的每一个轨道都处于充满状态,1个C原子与2个D原子结合,使双方都达到8电子稳定结构。则在C与D形成的分子中,C原子发生轨道的杂化方式是 ,分子构型是 ,从成键方式看,该分子中含有的共价键的类型和数目分别是 。
(3)C与D形成的常见晶体(乙),与甲晶体的熔点相比,乙 甲,其原因是
。
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)由A、B两元素组成的离子晶体结构(甲)如图所示,则该晶体的化学式是: 。
(2)C原子的最外层电子排布为nsnnpm,其某一激发态可使这两个亚层的每一个轨道都处于充满状态,1个C原子与2个D原子结合,使双方都达到8电子稳定结构。则在C与D形成的分子中,C原子发生轨道的杂化方式是 ,分子构
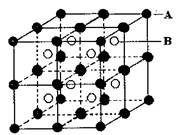
型是 ,从成键方式看,该分子中含有的共价键的类型和数目分别是 。
(3)C与D形成的常见晶体(乙),与甲晶体的熔点相比,乙 甲,其原因是
。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com