


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:2004全国各省市高考模拟试题汇编·化学 题型:013
2002年12月某日,在某著名商标新闻发布会上,长安酒厂的“长安牌”注册商标荣获著名商标.成为西安地区白酒生产企业唯一获此殊荣的厂家.该酒厂生产的一种白酒醇香浓厚,其标签上标有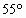 的字样,它表示
的字样,它表示
[ ]
A.该酒是在温度为55℃的条件下酿造的
B.喝了该酒后,人体内温度可达55℃
C.该酒的沸点为55℃
D.该酒中酒精的含量
查看答案和解析>>
科目:高中化学 来源: 题型:
2002年12月31日,世界上第一条商业磁悬浮铁路在上海投入运营。磁悬浮的核心技术是利用超导体的反磁性。以Y2O3、BaCO3和CuO为原料,经研磨烧结可合成一种高温超导物质YBa2Cu3Ox。现欲合成0.5mol此高温超导物质,理论上需取Y2O3、BaCO3和CuO的物质的量(mol)分别为 ( )
A.0.50、0.50、0.50 B.0.50、1.0、1.5
C.0.25、1.0、1.5 D.1.0、0.25、0.17
查看答案和解析>>
科目:高中化学 来源: 题型:
请你根据所学知识及有关信息完成下列各题:
(1)H3AsO3中As元素的化合价为_________。
(2)从经济、易得、实用的角度考虑,你认为投入的5.0×104 kg白色固体是_________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com