
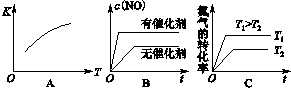
| △n |
| V?△t |
| △n |
| V?△t |
| 0.5mol |
| 2L×5min |
| (3×10-3 )2 |
| (2.5×10-1)×(4.0×10-2) |


 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案 应用题作业本系列答案
应用题作业本系列答案科目:高中化学 来源: 题型:
| A、有单质参加或有单质生成的反应一定是氧化还原反应 |
| B、金属单质在化学反应中一定作还原剂 |
| C、失电子的反应物在反应中作氧化剂,反应中被还原 |
| D、氧化还原的本质是元素化合价的升降 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、含有NH4+和H- |
| B、NH5中N元素的化合价为+5价 |
| C、1mol NH5中含有5NA个N-H键 |
| D、与乙醇反应时,NH5被还原 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| A、用图①所示装置收集HCl气体 |
| B、用图②所示装置配制一定物质的量浓度的硫酸 |
| C、用图③所示装置检查该装置的气密性 |
| D、用图④所示装置进行实验室制取的实验 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、10s | B、大于10s |
| C、小于10s | D、无法判断 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
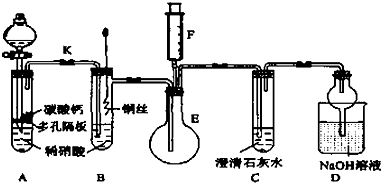
查看答案和解析>>
科目:高中化学 来源: 题型:
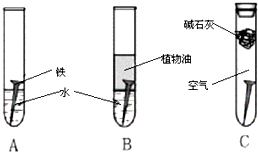 某研究小组对铁生锈进行研究:
某研究小组对铁生锈进行研究:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| A、①和②产物的阴阳离子个数比不相等 |
| B、①和②生成等物质的量的产物,转移电子数不同 |
| C、25℃、101kPa下,Na2O2(s)+2Na(s)═2Na2O(s)△H=-317 kJ?mol-1 |
| D、常温下Na与足量O2反应生成Na2O,随温度升高生成Na2O的速率逐渐加快 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com