
����Ŀ���û�ѧ��Ӧԭ���о������仯���������ش���ش���������:
��1����֪: N2(g)+3H2(g)![]() 2NH3(g) ��H=-92.4 kJ/mol
2NH3(g) ��H=-92.4 kJ/mol
N2(g)+O2(g)=2NO(g) ��H=+180.5 kJ/mol
2H2(g)+O2(g)=2H2O(g) ��H=-483.6kJ/mol
����34g��������������ȫ����һ�����������ˮ�������ų�������Ϊ_______��
��2��T1�¶�ʱ�����ݻ�Ϊ2 L �ĺ����ܱ������з�����Ӧ: 2NO(g)+O2(g)![]() 2NO2(g) ��H<0��ʵ����:v��=v(NO)����=2v(O2 )����=k��c2(NO)��c(O2)��v��=v(NO2)����=k��c2(NO2) ��k����k��Ϊ���ʳ��������¶�Ӱ�졣�����и���Ӧ�������������ʵ�����ʱ��仯��ͼ��ʾ:
2NO2(g) ��H<0��ʵ����:v��=v(NO)����=2v(O2 )����=k��c2(NO)��c(O2)��v��=v(NO2)����=k��c2(NO2) ��k����k��Ϊ���ʳ��������¶�Ӱ�졣�����и���Ӧ�������������ʵ�����ʱ��仯��ͼ��ʾ:
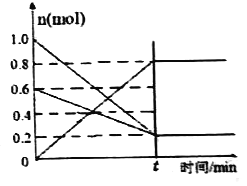
������˵���ܱ����÷�Ӧ�Ѵﵽƽ��״̬����______(�����)��
A.���������ܶȲ��� B.����������ɫ����
C. k����k������ D.2v��(O2)= v��(NO2)
����ѧƽ�ⳣ��K�����ʳ���k����k������ѧ��ϵ��K=_______��
��T1�¶�ʱ����ѧƽ�ⳣ��K=______�����������¶ȸı�ΪT2ʱ����k��=k�� ����T2___T1 (����>������<������=��)��
��3�� �������ǵ�Ԫ����Ҫ�ĺ�����֮һ��25�棬���amol/LHNO2ϡ��Һ��pH=b�����¶���HNO2����ƽ�ⳣ���ľ�ȷ�������ʽΪK=______(�ú�a��b�Ĵ���ʽ��ʾ)����amol/L��NaCN��Һ��0.01mol/L������������Ϻ����ҺpH=7������Һ��![]() =_____(�ú�a �Ĵ���ʽ��ʾ)��
=_____(�ú�a �Ĵ���ʽ��ʾ)��
���𰸡� 452.5 kJ B�� D k ��/k �� 160 �� 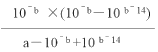 1 /(100a��1)
1 /(100a��1)
�������������������1�����ݸ�˹���ɼ���34g��������������ȫ����һ�����������ˮ�������ų�����������2��������ƽ���־������������ƽ��״̬ʱv��= v���������۸���![]() ������
������![]() �����������¶ȸı�ΪT2ʱ����k��=k������K=1���¶ȸı�ΪT2ʱƽ�ⳣ����С����Ӧ�����ƶ���(3)����K=
�����������¶ȸı�ΪT2ʱ����k��=k������K=1���¶ȸı�ΪT2ʱƽ�ⳣ����С����Ӧ�����ƶ���(3)����K=![]() ���������ݵ���غ㡢�����غ����
���������ݵ���غ㡢�����غ����![]() ��
��
��������1���� N2(g)+3H2(g)![]() 2NH3(g) ��H=-92.4kJ/mol
2NH3(g) ��H=-92.4kJ/mol
�� N2(g)+O2(g)=2NO(g) ��H=+180.5kJ/mol
�� 2H2(g)+O2(g)=2H2O(g) ��H=-483.6kJ/mol
���ݸ�˹�������![]() ����� 2NH3(g)+
����� 2NH3(g)+ ![]() O2(g)= 2NO(g)+ 3H2O(g) ��H= - 452.5 kJ/mol������34g��������������ȫ����һ�����������ˮ�������ų�������452.5 kJ����2������Ӧǰ���������������������������������
O2(g)= 2NO(g)+ 3H2O(g) ��H= - 452.5 kJ/mol������34g��������������ȫ����һ�����������ˮ�������ų�������452.5 kJ����2������Ӧǰ���������������������������������![]() ���ܶ��Ǻ��������������ܶȲ��䲻һ��ƽ������A����������������ɫ������˵��NO2��Ũ�Ȳ��䣬һ���ﵽƽ��״̬����B��ȷ�� C. k����k��ֻ���¶ȱ仯���¶��Ǻ���������k����k���Ǻ�����k����k����������һ��ƽ������C���� 2v��(O2)= v��(NO2)�����淴Ӧ���ʱȵ���ϵ������һ���ﵽƽ��״̬����D��ȷ����ƽ��״̬ʱv��= v������k��c2(NO)��c(O2) =k��c2(NO2)��
���ܶ��Ǻ��������������ܶȲ��䲻һ��ƽ������A����������������ɫ������˵��NO2��Ũ�Ȳ��䣬һ���ﵽƽ��״̬����B��ȷ�� C. k����k��ֻ���¶ȱ仯���¶��Ǻ���������k����k���Ǻ�����k����k����������һ��ƽ������C���� 2v��(O2)= v��(NO2)�����淴Ӧ���ʱȵ���ϵ������һ���ﵽƽ��״̬����D��ȷ����ƽ��״̬ʱv��= v������k��c2(NO)��c(O2) =k��c2(NO2)��![]() ��������ͼ����ƽ��ʱNO��Ũ����0.1mol/L��O2��Ũ����0.1mol/L��NO2��Ũ����0.4mol/L��
��������ͼ����ƽ��ʱNO��Ũ����0.1mol/L��O2��Ũ����0.1mol/L��NO2��Ũ����0.4mol/L�� ![]() ��������Ӧ�������¶���T1�ı�ΪT2��ƽ�ⳣ����С����Ӧ�����ƶ�������T2>T1����(3)25�棬���amol/LHNO2ϡ��Һ��pH=b����
��������Ӧ�������¶���T1�ı�ΪT2��ƽ�ⳣ����С����Ӧ�����ƶ�������T2>T1����(3)25�棬���amol/LHNO2ϡ��Һ��pH=b����![]() �����ݵ���غ���
�����ݵ���غ���![]() �����������غ���
�����������غ���![]() ������K=
������K=![]() =
=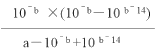 ����amol/L��NaCN��Һ��0.01mol/L������������Ϻ�PH=7����
����amol/L��NaCN��Һ��0.01mol/L������������Ϻ�PH=7����![]() �����������غ�
�����������غ�![]() ��
��![]() ��
��![]() �����ݵ���غ���
�����ݵ���غ���![]() ��
��![]() ��
��![]() ��
��![]() =
=![]() =1 /(100a��1)��
=1 /(100a��1)��


 ��ĩ���100�ִ��½����ȫ�Ծ�ϵ�д�
��ĩ���100�ִ��½����ȫ�Ծ�ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������һ�ֽ���������ʳƷ��������ij�ֶ��ɵ����ϱ��У��ٴ���ֲ���ͣ���ʳ���Σ��ܰ�ɰ�ǣ������ʻơ�
��1�����������ʵ���_________(����ţ���ͬ)��
��2��������֬����_________��
��3�������������_________��
��4��������ɫ������________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ijɷ���ҪΪFeCr2O4������������Al2O3��SiO2���Ӹ���������ȡ�������Ļ�����,����ø�����Ĺ�������������
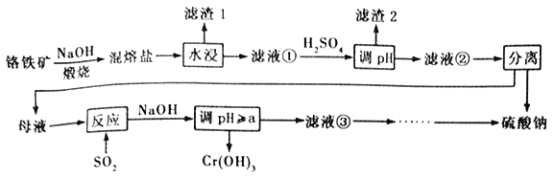
��֪�������Ρ��к���Na2CrO4��NaFeO2������NaFeO2����ˮ�⡣�Իش�����������
��1��������1��Ϊ���ɫ�������仯ѧʽΪ_________________������Һ���м�H2SO4����pH����Ŀ����һ��ʹCrO42-ת��ΪCr2O72- ������____________________________��
��2�������ա�������ʱ����Ҫ��Ӧ�Ļ�ѧ����ʽΪ_______________________________��
��3��������ͼ�ܽ��(S)~�¶�(T)�����ж�������Һ�����е���ѡ����롱����Ϊ_________(�����)��
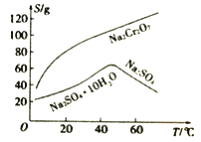
A.�����ᾧ B.����Ũ�������ȹ��� C.����Ũ������ȴ�ᾧ������
��4������Ӧ�������ӷ���ʽΪ_______________________________��
��5��Cr(OH)3������������������[CrCln(H2O) 6-n]x+��0.0015 mol [CrCln(H2O) 6-n]x+�������ӽ�����֬(HR)��ȫ�������ӽ�����
[CrCln(H2O) 6-n]x++xHR��Rx[CrCln(H2O) 6-n]+xH+�����ɵ�H+����25.00 mL0.1200 mol��L -1NaOH��Һǡ���к͡���������ӵĻ�ѧʽΪ__________________��
��6����֪25��ʱ��Cr(OH)3���ܶȻ�����Ksp[Cr(OH)3]=1.0��10-32����ʹCr3+ǡ����ȫ����������Һ��c(Cr3+) =1.0��10-5 mol��L -1ʱ��Ӧ������ҺpH����СֵaΪ����? (��ʽ����)____________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����MgSO4��Al2��SO4��3�Ļ����Һ�У���μ���NaOH��Һ������ͼ���У�����ȷ��ʾ������Ӧ���ǣ��������ʾ����NaOH��Һ��������������ʾ��Ӧ���ɳ�������������������
A.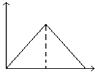
B.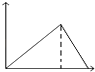
C.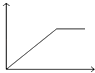
D.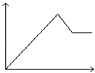
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪25��ʱ�����ֳ���������ʵĵ���ƽ�ⳣ�����±���ʾ:
����� | H3PO4 | NH3��H2O | C6H5OH |
����ƽ�ⳣ�� | K1=7.5��10-3 K2=7.5��10-8 K3=7.5��10-13 | 1.7��10-5 | 1.1��10-10 |
����˵����ȷ����
A. NaH2PO4��Һ�ʼ���
B. 25��ʱ��0.1moL/L��ˮ��pH=11+lg1.7
C. ����C6H5OH��Na3PO4��Ӧ�����ӷ���ʽΪ:2C6H5OH+PO43-=H2PO4-+2C6H5O-
D. 25��ʱ�����������Ũ�ȵı�����Һ�백ˮ��ϣ������Һ�и�����Ũ�ȹ�ϵ��c(C6H5O-)>c(NH4+)>c(OH-)>c(H+)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������˵����ȷ����
A.��ѧ���Ķ��ѹ����зų�����
B.��ѧ���γɵĹ�����Ҫ��������
C.���������仯�����ʱ仯���ǻ�ѧ�仯
D.��ѧ��Ӧ���������µ������⣬�������������ı仯
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������У���֤��ij��������һ���������Ӽ�����
A.������ˮB.����״̬�ܵ���
C.ˮ��Һ�ܵ���D.���нϸߵ��۵�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��A����Է�������Ϊ84���ش��������⣺
��1����A�ķ���ʽΪ ��
��2������AΪ���������������е�̼ԭ����ͬһƽ���ϣ��÷��ӵ�һ��ȡ����ֻ��һ�֣� ��A�Ľṹ��ʽΪ����Ϊ ��
������A��Br2��CCl4��Һ��Ӧ����B��д����A����B�Ļ�ѧ����ʽ�� ��
����A��Ϊͬ���칹�壬������̼ԭ�Ӹ�����A��ͬ���������֣�������A��
��3����A����ʹBr2��CCl4��Һ��ɫ������һ�ȴ���ֻ��һ�֣���A�Ľṹ��ʽΪ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й��л����������ȷ����
A. ��ˮ�����ķ�����Ҫ�������������������ӽ�����
B. �߾������Է�������һ��Ϊ������Է���������������
C. ![]() ������ֻ�����Ȼ����ǻ����ֹ�����
������ֻ�����Ȼ����ǻ����ֹ�����
D. ú�ĸ���������Һ�����������仯
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com