
用NA表示阿伏加德罗常数的值,下列说法正确的是( )
A.在1 L 0.1 mol/L硫化钠溶液中阴离子总数大于0.1NA
B.1 mol O2作氧化剂时转移电子数一定为4NA
C.标准状况下,22.4 L戊烷所含分子数为NA
D.在1 L 1.0 mol/L NaCl溶液中含有NA个NaCl分子
科目:高中化学 来源:2014高考化学专题突破训练 专题8电化学原理练习卷(解析版) 题型:选择题
用惰性电极电解NaCl和CuSO4混合液250 mL,经过一段时间后,两极均得到11.2 L气体(标准状况下),则下列有关描述中,正确的是( )
A.阳极发生的反应只有:4OH--4e-=2H2O+O2 ↑
B.两极得到的气体均为混合气体
C.若Cu2+起始浓度为1 mol·L-1,则c(Cl-)起始为 2 mol·L-1
D.Cu2+的起始物质的量应大于0.5 mol
查看答案和解析>>
科目:高中化学 来源:2014高考化学专题突破训练 专题4化学反应中的能量变化练习卷(解析版) 题型:填空题
Ⅰ.利用化学原理可以对工厂排放的废水、废渣等进行有效检测与合理处理。用乙烯作为还原剂将氮的氧化物还原为N2是燃煤烟气的一种脱硝(除NOx)技术。其脱硝机理如图所示。写出该脱硝过程中乙烯和NO2反应的化学方程式 。
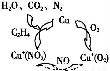
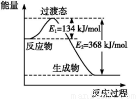
Ⅱ.(1)如图是1 mol NO2(g)和1 mol CO(g)反应生成CO2和NO过程中的能量变化示意图,若在反应体系中加入催化剂,反应速率增大,E1的变化是 (填“增大”、“减小”或“不变”,下同),ΔH的变化是 。
(2)甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是①CH3OH(g)+H2O(g)=CO2(g)+3H2(g)ΔH=+49.0 kJ·mol-1;
②CH3OH(g)+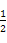 O2(g)=CO2(g)+2H2(g)ΔH=-192.9 kJ·mol-1。
O2(g)=CO2(g)+2H2(g)ΔH=-192.9 kJ·mol-1。
又知③H2O(g)=H2O(l) ΔH=-44 kJ·mol-1。
则甲醇蒸气完全燃烧生成液态水的热化学方程式为 。
写出甲醇质子交换膜燃料电池在酸性条件下的负极反应式: 。
查看答案和解析>>
科目:高中化学 来源:2014高考化学专题突破训练 专题3氧化还原反应 离子反应练习卷(解析版) 题型:选择题
下列表示对应化学反应的离子方程式正确的是( )
A.AlCl3溶液中加入过量的浓氨水:Al3++4NH3·H2O Al
Al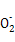 +4N
+4N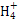 +2H2O
+2H2O
B.用FeCl3溶液腐蚀铜线电路板:Cu+2Fe3+ Cu2++2Fe2+
Cu2++2Fe2+
C.大理石溶于醋酸中的反应:CaCO3+2H+ Ca2++H2O+CO2↑
Ca2++H2O+CO2↑
D.钠与水反应:Na+2H2O Na++2OH-+H2↑
Na++2OH-+H2↑
查看答案和解析>>
科目:高中化学 来源:2014高考化学专题突破训练 专题2化学常用计量 溶液练习卷(解析版) 题型:选择题
下列有关说法正确的是( )
A.9.2 g NO2气体中含有分子数目为0.2NA
B.标准状况下,2.24 L SO3中含有氧原子数目为0.3NA
C.2 g 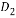 O中含中子、质子、电子数目均为NA
O中含中子、质子、电子数目均为NA
D.标准状况下2.24 L Cl2通入足量水中或NaOH溶液中,转移电子数目均为0.1NA
查看答案和解析>>
科目:高中化学 来源:2014高考化学专题突破训练 专题1物质的组成性质分类和化学用语练习卷(解析版) 题型:填空题
以下是依据一定的分类标准,对某些物质与水反应情况进行分类的图示。
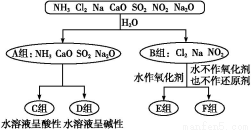
请根据你所学的知识,按要求填空:
(1)上述第一级分类标准(分成A、B组的依据)是 。
(2)F组中物质除了Cl2外还有 (填化学式)。
(3)A组中的CaO经常用作食品包装袋中的干燥剂,CaO所属的物质类型为 (用序号填空)。
①金属氧化物;②碱性氧化物;③碱;④碱性干燥剂
CaO可作干燥剂的理由是 (用化学方程式表示)。
(4)D组中NH3的水溶液呈弱碱性,用电离方程式表示其呈弱碱性的原因: 。
(5)由Al3+制备Al(OH)3,最好不选择D组中的NaOH溶液,说明理由: 。
查看答案和解析>>
科目:高中化学 来源:2014高考化学专题突破训练 专题1物质的组成性质分类和化学用语练习卷(解析版) 题型:选择题
分类法在化学学科的发展中起到重要作用。下列分类标准合理的是( )
A.根据分散系的稳定性大小将其分为溶液、胶体和浊液
B.根据反应的热效应将化学反应分为放热反应和吸热反应
C.根据溶液导电能力的强弱,将电解质分为强电解质和弱电解质
D.根据元素原子最外层电子数的多少将元素分为金属元素和非金属元素
查看答案和解析>>
科目:高中化学 来源:2014高考化学专题突破训练 专题13物质结构与性质选修3练习卷(解析版) 题型:填空题
A、B、C、D是元素周期表中前36号元素,它们的核电荷数依次增大。A原子L层的成对电子数和未成对电子数相等,B原子的最外层p轨道的电子为半充满结构,C是地壳中含量最多的元素。D是第四周期元素,其原子核外最外层电子数与氢原子相同,其余各层电子均充满。请回答下列问题:
(1)A、B、C的第一电离能由小到大的顺序是 (用对应的元素符号表示);基态D原子的电子排布式为 。
(2)A的最高价氧化物对应的水化物分子中,其中心原子采取 杂化;B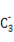 的空间构型为 (用文字描述)。
的空间构型为 (用文字描述)。
(3)1 mol AB-中含有的π键个数为 。
(4)如图是金属Ca和D所形成的某种合金的晶胞结构示意图,则该合金中Ca和D的原子个数比是 。
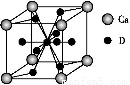
(5)镧镍合金与上述合金都具有相同类型的晶胞结构XYn,它们有很强的储氢能力。已知镧镍合金LaNin晶胞体积为9.0×10-23 cm3,储氢后形成LaNinH4.5合金(氢进入晶胞空隙,体积不变),则LaNin中n= (填数值);氢在合金中的密度为 。
查看答案和解析>>
科目:高中化学 来源:2014江苏省扬州市届高三上学期期末考试化学试卷(解析版) 题型:填空题
二甲醚(DME)被誉为“21世纪的清洁燃料”。由合成气制备二甲醚的主要原理如下:
① CO(g)+2H2(g)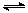 CH3OH(g) △H 1=-90.7 kJ·mol-1
CH3OH(g) △H 1=-90.7 kJ·mol-1
② 2CH3OH(g)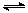 CH3OCH3(g)+H2O(g) △H 2=-23.5 kJ·mol-1
CH3OCH3(g)+H2O(g) △H 2=-23.5 kJ·mol-1
③ CO(g)+H2O(g)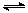 CO2(g)+H2(g) △H 3=-41.2kJ·mol-1
CO2(g)+H2(g) △H 3=-41.2kJ·mol-1
回答下列问题:
(1)则反应3H2(g)+3CO(g)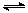 CH3OCH3(g)+CO2(g)的△H= kJ·mol-1。
CH3OCH3(g)+CO2(g)的△H= kJ·mol-1。
(2)下列措施中,能提高CH3OCH3产率的有 。
A.使用过量的CO B.升高温度 C.增大压强
(3)反应③能提高CH3OCH3的产率,原因是 。
(4)将合成气以n(H2)/n(CO)=2通入1 L的反应器中,一定条件下发生反应:
4H2(g)+2CO(g) 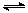 CH3OCH3(g)+H2O(g) △H,其CO的平衡转化率随温度、压强变化关系如图1所示,下列说法正确的是 。
CH3OCH3(g)+H2O(g) △H,其CO的平衡转化率随温度、压强变化关系如图1所示,下列说法正确的是 。
A.△H <0
B.P1<P2<P3
C.若在P3和316℃时,起始时n(H2)/n(CO)=3,则达到平衡时,CO转化率小于50%[
(5)采用一种新型的催化剂(主要成分是Cu-Mn的合金),利用CO和H2制备二甲醚。观察图2回答问题。催化剂中n(Mn)/n(Cu)约为 时最有利于二甲醚的合成。
(6)图3为绿色电源“二甲醚燃料电池”的工作原理示意图,a电极的电极反应式为 。
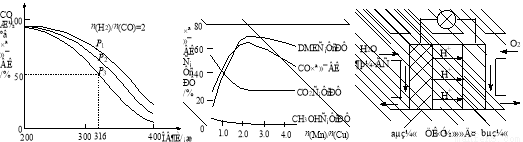
图1 图2 图3
(7)甲醇液相脱水法制二甲醚的原理是:CH3OH +H2SO4→CH3HSO4+H2O,
CH3 HSO4+CH3OH→CH3OCH3+H2SO4。与合成气制备二甲醚比较,该工艺的优点是反应温度低,转化率高,其缺点是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com