


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:2013-2014学年浙江省金华十校高考模拟考试理综化学试卷(解析版) 题型:选择题
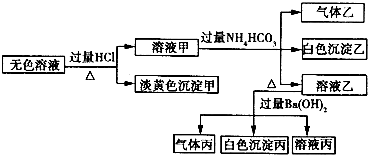
某废水中可能存在的离子如下:Na+、Ag+、Ba2+、Al3+、AlO2一、CO32-、S2一、SO32-、SO42-
现取该溶液进行有关实验,实验过程及现象如下:

? 下列说法正确的是
A.根据实验①中的现象可推出,气体A一定是纯净物,淡黄色沉淀一定是AgBr
B.根据实验②中的现象可推出,气体B是CO2,沉淀B是Al(OH)3,原溶液中一定含有Al3+
C.根据实验③中的现象可推出,气体C是NH3,沉淀C一定有BaCO3,可能有BaSO4
D.原溶液中肯定含有Na+、AlO2-、S2-,不能确定是否含有SO32-、SO42-
查看答案和解析>>
科目:高中化学 来源:2012年鲁科版高中化学必修1 4.2铝 金属材料练习卷(解析版) 题型:填空题
某无色溶液中只含有下列8种离子中的某几种: Mg2+、H+、Ag+、Na+、Cl-、HCO3-、OH-、NO3-,已知该溶液与铝反应放出氢气。试回答下列问题:
(1)若反应后生成Al3+,则溶液中可能存在的离子有_______________,一定存在的离子有________________,一定不存在的离子有_________________反应的离子方程式为________________。
(2)若反应后生成〔Al(OH)4〕-离子,则溶液中可能存在的离子有_______________,一定存在的离子有________________,一定不存在的离子有_________________反应的离子方程式为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)某温度(t℃)时,水的Kw=10-13 mol2·L-2,则该温度(填大于、小于或等于) 25℃,将此温度下pH=11的NaOH溶液aL与pH=1的H2SO4的溶液bL混合,若所得混合液的pH=2,则a∶b ;
(2) 已知某溶液中只含有OH-、H-、Na+、CH3COO-四种离子。(25℃)
① 用电离方程式或水解离子方程式表示出该溶液中可能存在的全部平衡体系,
。
② 若溶液中只溶解了一种溶质,则该溶质是 。
③ 若溶液能使甲基橙试液变红,则含有的溶质是 :Z
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com