
����Ŀ��һ���¶��½�0.2 mol����A����10 L�����ܱ������У����з�Ӧ2A(g)+ B(g)![]() 2C(g)��D(s) ��H<0��һ��ʱ���Ӧ�ﵽƽ�⡣�˷�Ӧ�����вⶨ���������±���ʾ��������˵����ȷ����
2C(g)��D(s) ��H<0��һ��ʱ���Ӧ�ﵽƽ�⡣�˷�Ӧ�����вⶨ���������±���ʾ��������˵����ȷ����
t/min | 2 | 4 | 6 | 8 | 10 |
n(A)/mol | 0.16 | 0.13 | 0.11 | 0.10 | 0.10 |
A. ��Ӧǰ2min��ƽ��������(C)=0.02mol��L��1��min-1
B. ƽ����¶ȣ���Ӧ�ﵽ��ƽ��ǰ��(��)> ��(��)
C. �����������䣬10min���ٳ���һ������A��ƽ�������ƶ���A��ת���ʱ�С
D. ���������������䣬��Ӧ�ں�ѹ�½��У�ƽ��ʱA����������������������ͬ
���𰸡�C
��������A���ɷ���ʽ��֪����Ӧǰ2 min����c��C��=��c��A��=0.2mol-0.16mol=0.04mol�������ݻ�Ϊ10L����v��C��= =0.002mol/��L��min������A����B������ӦΪ���ȷ�Ӧ�������¶�ƽ�������ƶ�����Ӧ�ﵽ��ƽ��ǰ�����棩��������������B����C�������������䣬10 min���ٳ���һ������A��A��Ũ������ƽ�������ƶ�����A��ת���ʱ�С����C��ȷ��D������ӦΪ�������ʵ�����С�ķ�Ӧ�����º�����ƽ��ʱѹǿ��С����Ч�ں��º�ѹ��ƽ������ϼ�Сѹǿ��ƽ�������ƶ����ʺ��º�����A�������������D����ѡC��
=0.002mol/��L��min������A����B������ӦΪ���ȷ�Ӧ�������¶�ƽ�������ƶ�����Ӧ�ﵽ��ƽ��ǰ�����棩��������������B����C�������������䣬10 min���ٳ���һ������A��A��Ũ������ƽ�������ƶ�����A��ת���ʱ�С����C��ȷ��D������ӦΪ�������ʵ�����С�ķ�Ӧ�����º�����ƽ��ʱѹǿ��С����Ч�ں��º�ѹ��ƽ������ϼ�Сѹǿ��ƽ�������ƶ����ʺ��º�����A�������������D����ѡC��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ά�ء����ᡢθ����ø�ĵ���ֱ��ǣ� ��
A. ��������ǡ����� B. �����ǡ������ᡢ������
C. �����ǡ������ᡢ������ D. ���ǡ������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1��AgNO3��ˮ��Һ��________�����������������������������ԣ�ʵ����������AgNO3����Һʱ������AgNO3���������ڽ�Ũ�������У�Ȼ����������ˮϡ�͵������Ũ�ȣ���____�������ٽ�����������������ˮ�⡣
��2����֪���ܵ����A�Ļ�ѧʽΪXnYm����Է�������ΪM������䱥����Һ���ܶ�Ϊ�� g/cm3��Xm����Ũ��Ϊc mol/L�����������XnYm���ܶȻ�����ΪKsp��________��
��3�����ʵ���Ũ����ͬ�Ĵ��������������Һ��Ϻ���Һ�д�������Ӻ�������Ũ����ȣ����Ϻ���Һ��_____�����������������������������ԣ����ʱ�������________��������������������������С����������������Һ�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ͨ��ָ�������еĵ�������(NOx)ת��Ϊ�������ʡ�
��1��ѡ���Դ���ԭ����(SCR)��Ŀǰ�����������������������ڽ������������£��û�ԭ��(��NH3)ѡ���Ե���NOx��Ӧ����N2��H2O��
����֪:4NH3(g)+5O2(g) ![]() 4NO(g)+6H2O(g) ��H=-905.5kJ��mol-1
4NO(g)+6H2O(g) ��H=-905.5kJ��mol-1
N2(g)+O2(g) ![]() 2NO(g) ��H=+l80kJ mol-1
2NO(g) ��H=+l80kJ mol-1
��ɸ÷�������Ҫ��Ӧ���Ȼ�ѧ����ʽ��
4NH3(g)+4NO(g)+O2(g) ![]() 4N2(g)+6H2O(g) ��H=___________��
4N2(g)+6H2O(g) ��H=___________��
�÷���Ӧ���Ʒ�Ӧ�¶���315400��֮�䣬��Ӧ�¶Ȳ��˹���Ҳ���˹��ߵ�ԭ����___________��
�۰�����[n(NH3)/n(NO)]��ֱ��Ӱ��÷����������ʣ�350��ʱ��ֻ�ı䰱����Ͷ��������Ӧ��X��ת�����백���ȵĹ�ϵ����ͼ��ʾ����X��______ (��ѧʽ)����������0.5���ӵ�1.0ʱ��������Ҫ��Ӧ��ƽ�⽫��____�����ƶ�����[n(NH3)/n(NO)>1.0ʱ��������NOŨ�ȷ���������Ҫԭ����_____��

��2��ֱ�ӵ������Ҳ��������һ�ַ�������6%��ϡ��������NOx����HNO2(��Ԫ����)���ٽ�����Һ������۵�⣬ʹ֮ת��Ϊ���ᡣ���װ��������ͼ��ʾ����ͼ��bӦ���ӵ�Դ��______����������������������)����a�缫��ӦʽΪ__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������[Ca(NO2)2]��ˮ���������Ӽ�����Ҫԭ�ϣ�ijѧϰС�����ʵ���Ʊ�������ƣ�ʵ��װ����ͼ��ʾ���г�װ����ȥ��:
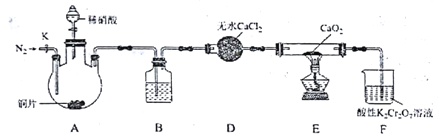
��֪�� 2NO+CaO2=Ca(NO2)2��2NO2+CaO2=Ca(NO3)2��
��ش��������⣺
��1������Һ©���е�ϡ�������������ƿ�еIJ���Ϊ�� __________���� __________��
��2����������ƿ�м���ϡ����֮ǰ��Ӧ��װ����ͨ��һ��ʱ���N2��ԭ��Ϊ���÷���ʽ��ʾ��____��
��3��װ��D������������________;װ��B�����Լ���_______��
��4��װ��F�У�����K2Cr2O7��Һ�ɽ�ʣ���NO������NO3-����Һ�ɳ�ɫ��Ϊ��ɫ(Cr3+)��������Ӧ�����ӷ���ʽ��__________________��
��5����֪��Ca(NO2)2��Һ��������NO���塣���ʵ��֤��װ��E��������������ɣ�__________��
��6����ҵ�Ͽ���ʯ��������Ṥҵ��β������NO��NO2����Ӧ�����ܾ���β�������ܻ��Ӧ�ù㷺��Ca(NO2)2����Ӧԭ��ΪCa(OH)2+NO +NO2=Ca(NO2)2+H2O��
����n( NO)��n(NO2��>l:l����ᵼ��____��
����n( NO)��n( NO2)����ᵼ��____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NaHCO3��NaHSO4����Һ��Ϻ�ʵ�ʲμӷ�Ӧ��������
A. H+��CO32 B. HCO3��HSO4
C. Na+��HCO3��H+ D. HCO3��H+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ȼ���(CdCl2)��һ�ֳ����ڱ�Ĥ̫���ܵ���ϵ����ʣ��������ж�����ѧ��ѡ������һ��������������������������
A. Si B. HClO4
C. MgCl2 D. SiO2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������Һ�У����������ʵ���Ũ�ȹ�ϵ��ȷ���ǣ�
A. 0.1mol��L-1��NaHCO3��Һ:c(Na+)��c(OH-)��c(HCO3-)��c(H+)
B. 0.1mol��L-1Na2CO3��Һ:c(OH-)-c(H+)=c(HCO3-)+c(H2CO3)
C. ��������0.01mol��L-1��(NH4)2SO4��Һ���� c(NH4+)��c(SO42-)��c(H+)�� c(OH-)
D. 25��ʱ��Ũ�Ⱦ�Ϊ0.1mol��L-1��CH3COOH��CH3COONa�����Һ����������c(CH3COO-)+ c(OH-)��c(CH3COOH)+c(H+)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����д�ʩ��Ϊ�˽��ͻ�ѧ��Ӧ���ʵ���
A. ��п�۴���пƬ��ϡ���ᷴӦ��ȡ���� B. ʳƷ���ڱ���������
C. �ϳɰ���ҵ��ʹ�ô��� D. ���Թ��н����������ᷴӦʱ��������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com