
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
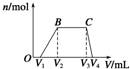 1L某混合溶液,可能含有的离子如下表:
1L某混合溶液,可能含有的离子如下表:| 可能大量含有的阳离子 | H+、K+、Mg2+、Al3+、NH
| ||||
| 可能大量含有的阴离子 | Cl-、Br-、I-、CO
|
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、C2H6 |
| B、C3H10O |
| C、C4H8O2 |
| D、C5H10O3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
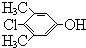 PCMX是一种安全、高效、广谱的防霉搞菌剂,已广泛应用于和皮肤接触的个人护理产品如洗手液、肥皂、去屑香波等产品中,可杀灭肠道致病菌、化脓性致病菌、和致病性酵母菌等.其分子结构如图所示,对于PCMX的描述中正确的是( )
PCMX是一种安全、高效、广谱的防霉搞菌剂,已广泛应用于和皮肤接触的个人护理产品如洗手液、肥皂、去屑香波等产品中,可杀灭肠道致病菌、化脓性致病菌、和致病性酵母菌等.其分子结构如图所示,对于PCMX的描述中正确的是( )| A、该物质属于酚类物质,易溶于水 |
| B、该物质在常温下是无色晶体,分子式为C8H6ClO |
| C、该物质不能长期跟皮肤接触,擦在手上后应立即洗净 |
| D、常温下,1mol该物质与足量NaOH溶液完全反应消耗NaOH 2mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com