
 阶梯计算系列答案
阶梯计算系列答案科目:高中化学 来源: 题型:阅读理解
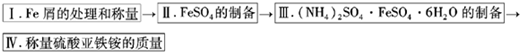
| 温度℃ | FeSO4?7H2O | (NH4)2SO4 | |
| 10 | 20.0 | 73.0 | 17.2 |
| 20 | 26.5 | 75.4 | 21.6 |
| 30 | 32.9 | 78,0 | 28.1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
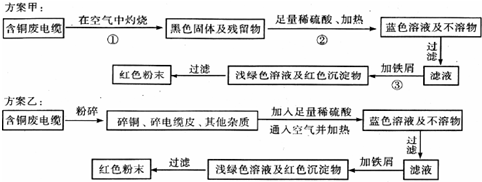
| 序号 | 实验操作 | 实验现象 | 离子方程式 |
| ① | 取适量的样品于试管内 | ||
| ② | 用滴管滴入足量硫酸溶液,并充分振荡试管 | ||
| ③ | 溶液先变黄色,滴入KSCN溶液后,溶液变红色 |
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
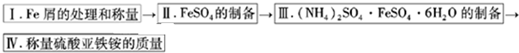
| 温度/℃ | FeSO4?7H2O | (NH4)2SO4 | (NH4)2SO4?FeSO4?6H2O |
| 10 | 20.0 | 73.0 | 17.2 |
| 20 | 26.5 | 75.4 | 21.6 |
| 30 | 32.9 | 78.0 | 28.1 |
查看答案和解析>>
科目:高中化学 来源:巢湖市一中2008-2009学年度第二学期第一次月考高二化学试卷 题型:013
|
用3 g铁屑与适量1 mol/L稀硫酸反应制取H2气体,若要增大反应速率,可采取的措施是: ①再加入适量1 mol/L硫酸 ②改用3 mol/L硫酸 ③改用3 g铁粉 ④适当升高温度 ⑤加几滴CuSO4溶液 ⑥用浓硫酸代替1 mol/L稀硫酸 | |
| [ ] | |
A. |
①②④⑤ |
B. |
②③④⑤ |
C. |
①③④⑤ |
D. |
②③④⑤⑥ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com