
�������⣨H2O2��O�Ļ��ϼ�Ϊ��1�ۣ��׳�˫��ˮ��ҽ������������ɱ��������������ϴ�˿ڡ��о������漰H2O2�ķ�Ӧ��������и��⣺
A��Ag2O+ H2O2��2Ag+O2 ��+ H2O
B��3H2O2+Cr2(SO4)3+10KOH��2K2CrO4+3K2SO4+8H2O
��1��д��һ��H2O2�����������������ֻ�ԭ�ԵĻ�ѧ��Ӧ����ʽ ��
��2�����������ʣ�H2O2��K2SO4��MnSO4��H2SO4��KMnO4��O2�Ļ�ѧʽ�ֱ����ڿհ״����һ��������ƽ�Ļ�ѧ����ʽ�� + +______ �� + + + H2O
�ٸ÷�Ӧ�еĻ�ԭ���� ��
�ڸ÷�Ӧ�У�������ԭ��Ӧ��Ԫ���� ��
��3�������ԣ�KMnO4_____K2CrO4���������������
��1��2H2O2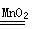 2H2O + O2�� ��2��H2O2+KMnO4+H2SO4��MnSO4+O2+K2SO4+ H2O
2H2O + O2�� ��2��H2O2+KMnO4+H2SO4��MnSO4+O2+K2SO4+ H2O
��H2O2 ��Mn ��3����
���������������1��H2O2�����������������ֻ�ԭ�ԣ���˵���÷�Ӧһ����˫��ˮ�ķֽⷴӦ����Ӧ�Ļ�ѧ����ʽΪ2H2O2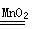 2H2O + O2����
2H2O + O2����
��2��������ؾ���ǿ�����ԣ���������ǿ��˫��ˮ�ģ����Ը�������ܰ�˫��ˮ����������������������صĻ�ԭ�����������̣���˸÷�Ӧ�ķ���ʽ���Ա�ʾΪH2O2+KMnO4+H2SO4��MnSO4+O2+K2SO4+ H2O��
��˫��ˮ����Ԫ�صĻ��ϼ۴ӣ�1�����ߵ�0�ۣ������������˫��ˮ�ǻ�ԭ����
�ڸ��������MnԪ�صĻ��ϼ۴ӣ�7�۽��͵���2�ۣ��õ����ӣ�����ԭ�����Ա���ԭ��Ԫ����Mn��
��3���ڷ�Ӧ3H2O2+Cr2(SO4)3+10KOH��2K2CrO4+3K2SO4+8H2O�У�˫��ˮ����������K2CrO4����������������������������ǿ����������Ŀ�֪����������˫��ˮǿ��K2CrO4���ڷ�ӦH2O2+KMnO4+H2SO4��MnSO4+O2+K2SO4+ H2O�У��������������������������ǿ��˫��ˮ�ģ����Ը�����ص�������ǿ��K2CrO4��
���㣺����������ԭ��Ӧ��Ӧ�á��ж�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��Ԫ�صĻ������ڹ�ũҵ�Լ������Ƽ�����;�㷺����Ҳ��Ի��������Ⱦ�������ˮ����������ɵĵ���Ⱦ�ѳ�Ϊһ�������ԵĻ������⡣
���������գ�
��1��ij������ģ�����ˮ�ѵ����̣�����Fe�ۺ�KNO3(aq)��Ӧ̽���ѵ�ԭ����ʵ��ǰ
����0.1mol��L-1H2SO4(aq)ϴ��Fe�ۣ���Ŀ���� ��Ȼ��������ˮϴ�������ԣ�
�ڽ�KNO3(aq)��pH����2.5��
��Ϊ��ֹ�����е� ��д��ѧʽ�����ѵ���Ӱ�죬Ӧ��KNO3��Һ��ͨ��N2��
��2��������Fe�ۻ�ԭ����KNO3(aq)�����У���Ӧ���������������Ũ�ȡ�pH��ʱ��ı仯��ϵ��ͼ��ʾ�������ͼ����Ϣд��t1ʱ��ǰ�÷�Ӧ�����ӷ���ʽ�� ��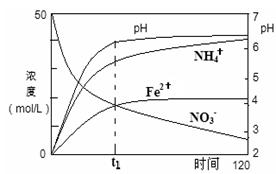
��3���������˷ɴ��Ļ���ƽ����г����£�N2H4����ȼ�ϡ�NH3��NaClO��Ӧ�ɵõ��£�N2H4�����÷�Ӧ�б������뱻��ԭ��Ԫ�ص�ԭ�Ӹ���֮��Ϊ �������Ӧ����5mol���ӷ���ת�ƣ��ɵõ��� g��
��4����������25mL 0.01mol/Lϡ�����л���ͨ��5.6 mL NH3����״������Һ����仯���Բ��ƣ�����Ӧ����Һ������Ũ���ɴ�С��˳���� ����ͨ��NH3�Ĺ�������Һ�ĵ������� ����д���������С���������䡱����
��5����������Һ�м���ͨ��NH3���ù���������Ũ�ȴ�С��ϵ������ȷ���� ��ѡ���ţ���
a��c(Cl-)=c(NH4+)��c(H+)=c(OH-) b��c(Cl-)��c(NH4+)=c(H+)��c(OH-)
c��c(NH4+)��c(OH-)��c(Cl-)��c(H+) d��c(OH-)��c(NH4+)��c(H+)��c(Cl-)
��6����������25mL��HCl 0.01mol����Һ�еμӰ�ˮ���������ù�����ˮ�ĵ���ƽ�� ����д����ƽ���ƶ�����������μӰ�ˮ��25mLʱ�������Һ��ˮ�ĵ���������ˮ��Ũ��Ϊ mol��L-1��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
������ԭ��Ӧ�������������о��й㷺����;���ᴩ�Ž�
��1����������������������з�����������ԭ��Ӧ���� ��
��2��ˮ���������Ҫ��ɲ��֣��������к�������һ�����ʡ��������ֻ�����Ӧ������������ԭ��Ӧ�Ĺ�ϵ��Ҳ������ͼ���
��д����ˮ�μӡ�ˮΪ��ԭ����Ϊ���͢���һ����ѧ����ʽ�� ��
��3��NaNO2��һ��ʳƷ���Ӽ��������°�������KMnO4��Һ��NaNO2��Ӧ�����ӷ���ʽ�ǣ�
���벹����������ƽ����ʽ���������ת�Ƶķ������Ŀ��
��ijͬѧ��ȡ��7.9 g KMnO4�����壬������100 mL��Һ���ش��������⣺
��ʵ���У�ʹ������ƿʱҪ����Ƿ�©ˮ��������� ��
�۲��淶��ʵ������ᵼ��ʵ�����������в�����ʹʵ����ƫС���� (�����)��
A�����ܽ������������Һ�彦���ձ���
B������ʱ��������ƿ�ϵĿ̶���
C�����ݺ�����ƿ��ҡ�Ⱥ��÷���Һ����ڿ̶��ߣ������ּ�������ˮ���̶���
��ijͬѧ��������õ�KMnO4��Һ�ζ�δ֪Ũ�ȵ�NaNO2��Һ��ȡ20 mLδ֪Ũ�ȵ�NaNO2��Һ����ƿ��ȡ������õ�KMnO4��Һ��________(���ʽ����ʽ��)�ζ��ܣ��ζ���ɺ�����KMnO4��Һ10 mL����NaNO2��Һ��Ũ��Ϊ________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
������KMnO4����ŨHCl�ķ�Ӧ����ʽ���£�2KMnO4 ��16HCl��Ũ��=2KCl��2MnCl 2��5Cl 2����8H2O
��1���á�˫���ŷ���������Ӧ�е���ת�Ƶķ������Ŀ��
��2������֪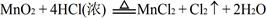 ��������Ϸ�Ӧԭ������MnO2��KMnO4��Cl2����������ǿ������˳���ǣ� ��
��������Ϸ�Ӧԭ������MnO2��KMnO4��Cl2����������ǿ������˳���ǣ� ��
��3������63.2g������زμӷ�Ӧ����������HCl�����ʵ���Ϊ mol��������Cl2�ڱ�״���µ����Ϊ L��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�����а�������Na��Mg2+��Fe2+��Fe3+��S2-��SO2��HCl��H2O����Ԫ�ػ��ϼ۵ĽǶȷ���������ֻ�������Ե���______ ��ֻ�л�ԭ�Ե���_____ _��
�������������л�ԭ�Ե���__________ _��
����֪�����������Ũ���ᷴӦ��ȡ�������仯ѧ����ʽ���£�
KClO3+6HCl=KCl+3Cl2��+ 3H2O
��������������������ʽ�б������ת�Ƶķ������Ŀ��
�Ʊ��������3��36LCl2��ת�Ƶ��ӵ����ʵ���Ϊ ����������������δ����������������֮��Ϊ �����������뻹ԭ�������ʵ���֮��Ϊ ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��1����ͼ�ǿα��С����ֻ�����Ӧ������������ԭ��Ӧ�Ĺ�ϵ��ͼ����H2+CuO  Cu+H2O����Ӧ����ͼ�е����� ������ţ������з�Ӧ����������7���� ��
Cu+H2O����Ӧ����ͼ�е����� ������ţ������з�Ӧ����������7���� ��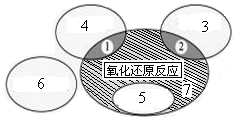
A��2H2+O2 2H2O 2H2O |
B��2NaHCO3 Na2CO3+H2O+CO2�� Na2CO3+H2O+CO2�� |
| C��Zn+H2SO4=ZnSO4+H2�� |
D��CuO+CO Cu+CO2 Cu+CO2 |
 N2+6NH4Cl
N2+6NH4Cl�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
ͨ����ģ�͡�ͼ�Ρ�ͼ���Ĺ۲죬�ܻ�ȡ�й���Ϣ�ǻ�ѧѧϰ��һ����Ҫ��������Ҫ��ش��������⡣
(1) �������ж�����Ԫ�����ʵIJ������ݣ�����X��ֵ�DZ�ʾ��ͬԪ�ص�ԭ���ڷ������������ӵ�������С����XֵԽ����ԭ��������������Խǿ�������γɵķ����г�Ϊ�������һ����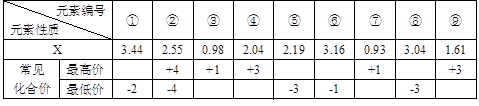
д�����б����������Ԫ�ط��ţ���____����____����____����____����____��
(2) ��֪4������������ˮ�к�Һ���е��ܽ��(g/100g�ܼ�)Ϊ��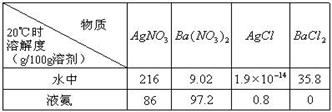
���ϱ������ݿ�֪����ˮ��Һ����������������ֽⷴӦ�Ļ�ѧ����ʽΪ______________________����Һ����Һ�з������ֽⷴӦ�Ļ�ѧ����ʽΪ______________________________________________��
(3) ijϡ��Һ�к���Fe(NO3)3��Cu(NO3)2��HNO3���������������ۣ���Һ��Fe2+��Ũ�Ⱥͼ������۵����ʵ���֮��Ĺ�ϵ����ͼ��ʾ���������ʺ���������Ӧ��˳��Ϊ___________����һ����Ӧ�����ӷ���ʽΪ________����ͼ��֪��Һ��Fe(NO3)3��Cu(NO3)2��HNO3���ʵ���Ũ��֮��Ϊ__________��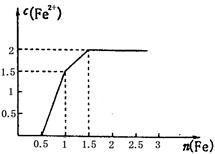
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��.±�����±�����ڹ�ҵ������������Ҫ�����á�ijС��Ϊ̽������һЩ�ε���
�ʣ��������ϲ�����ʵ�顣�����������£�
�� BrO3�� + 6I�� + 6H+ = 3I2 + Br��+ 3H2O �� 2BrO3�� + I2 = 2IO3�� + Br2
�� IO3�� + 5I�� + 6H+ = 3I2 + 3H2O �� 2IO3�� + 10Br��+ 12H+ = I2 + 5Br2 + 6H2O
ʵ�����£�
| ���� | ���� |
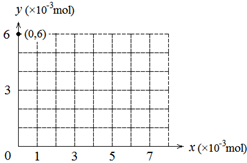
| ��.��ʢ��30 mL 0.2 mol��L-1 KI��Һ����ƿ�����ε��뼸�ε�����Һ������ϡ���ᣬ���õζ�����μ���KBrO3��Һ | ����KBrO3��Һ���룬��Һ����ɫ��Ϊ��ɫ������,���ձ��ֲ��� |
| ��.������������Һ�е���KBrO3��Һ | ��Һ����ɫ����ȥ |

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
��50 mL a mol��L-1��������Һ�У�����6��4g Cu��ȫ���ܽ⣬��������Ļ�ԭ����ֻ��NO2��NO������Ӧ����Һ������ˮϡ����100 mLʱ���c(NO3-)��3 mol��L-1��
(1)��ϡ�ͺ����Һ��H+�����ʵ���Ũ��
(2)��a��9�������ɵ�������NO2�����ʵ���
(3)��������������Ⱦ�ķ���֮һ����NaOH��Һ�������գ���Ӧԭ�����£�
NO2��NO��2NaOH��2NaNO2��H2O��2NO2��2NaOH��NaNO2��NaNO3��H2O������������NO2��NO�Ļ������ͨ��1 mol��L-1��NaOH��Һǡ�ñ����գ�����ҪNaOH��Һ�������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com