
����Ŀ��ԭ���������������X��Y��Z��Q��E����Ԫ���У�XԪ��ԭ�Ӻ��������ֲ�ͬ���ܼ��Ҹ����ܼ������ĵ�������ͬ��Z�ǵؿ��ں�����������������ߵ�Ԫ�أ�Qԭ�Ӻ����M����ֻ�����ԳɶԵ��ӣ�EԪ��ԭ������Ϊ29��
��Ԫ�ط��Ż�ѧʽ�ش��������⣺
(1)Y�����ڱ��е�λ��Ϊ__________________��
(2)��֪YZ2+��XO2��Ϊ�ȵ����壬��1mol YZ2+�к��Цм���ĿΪ___________��
(3)X��Z����Ԫ�ؿ��γɻ�����XH2Z��XH2Z������X���ӻ���ʽΪ_________________��
(4)Eԭ�ӵĺ�������Ų�ʽΪ__________��E�пɱ��̬������ij��̬��������Z���������γɾ���ľ�����ͼ��ʾ���ü�̬�Ļ�ѧʽΪ____________��
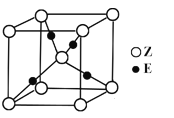
(5)��Ԫ�غ���Ԫ���ܹ��γɻ�����F���侧���ṹ��ͼ��ʾ�������徧������������ܶ�Ϊ��g����cm-3����ʽ���㾧���ı߳�Ϊa=______________cm��Ҫ���д���ʽ����

���𰸡� �ڶ����� ��VA�� 2NA��1.204��1024 sp2�ӻ� 1s22s22p63s13p23d63d104s1��[Ar]3d104s1 Cu2O 
��������XԪ��ԭ�Ӻ��������ֲ�ͬ���ܼ��Ҹ����ܼ������ĵ�������ͬ����XΪC��Z�ǵؿ��к�����ߵ�Ԫ�أ���ZΪO������Ϊԭ����������������YΪN��Qԭ�Ӻ����M����ֻ�����ԳɶԵ��ӣ���QΪS��E��ԭ������Ϊ29����EΪCu����1������Ԫ����Ԫ�����ڱ��е�λ�ã�Y��N��λ�ڵڶ�����VA�壻��2������ȵ�����ͦм��жϣ�YZ2��ΪNO2������CO2��Ϊ�ȵ����壬�ȵ�����Ľṹ���ƣ�CO2�ĽṹʽΪO=C=O�����1molNO2���к��Цм�����ĿΪ2NA������3�������ӻ����ͣ��γɵĻ�������HCHO������̼ԭ����sp2�ӻ�����4�������������Ų�ʽ��ͨ�������Ľṹȷ����ѧʽ��Cuλ�ڵ�������IB�壬��������Ų�ʽΪ1s22s22p63s13p23d63d104s1��[Ar]3d104s1 ��Oԭ��λ�ڶ�������ģ�����Ϊ8��1/8��1=2��Cuȫ��λ�����ģ���˻�ѧʽΪCu2O����5�����龧���ļ��㣬��������Ų���ͬʱ���뾶����ԭ�������������С������Ԫ��λ�ڶ�������ģ�����Ϊ8��1/8��6��1/2=4��NaԪ��λ�ھ����ڣ���8������˻�ѧʽΪNa2O������������Ϊ4��62/NAg�����������Ϊa3cm3�������ܶȵĶ��壬�Ц�=4��62/��NA��a3�������߳�Ϊ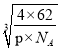 cm��
cm��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���⼰�仯�����ڿ��С�����ȷ����й㷺��;���ش��������⣺
(1)�����и����⣬������ʵ�����̿ɶԺ����е�ĺ������вⶨ��

ȡ0.0100 mol/L��AgNO3����Һװ����ɫ�ζ��ܣ�ȡ100.00 mL������ȡԭҺ���ζ��أ��õ��Ƶζ����ⶨ�⺬������õĵ綯��(E) ��ӳ��Һ��c(I��)�ı仯�������������±���
V(AgNO3)/mL | 15.00 | 19.00 | 19.80 | 19.98 | 20.00 | 20.02 | 21.00 | 23.00 | 25.00 |
E/mV | ��225 | ��200 | ��150 | ��100 | 50.0 | 175 | 275 | 300 | 325 |
�����պ���ʱ������Ҫ�����⣬����Ҫ�õ���ʵ��������____________ (�����)��
a���ձ� b�����ż� c���¶ȼ� d�������� e���ƾ��� f������ǯ
��ʹ����ɫ�ζ��ܵ�ԭ����_____________________��
�۸��ݱ������ݣ����㺣���е�İٷֺ���Ϊ____________��
(2)����������ࡱ��������ѧʵ��֮һ����ʵ�鷽���ǽ�Ũ���Ĺ���������Һ�����Һ��ϣ��ٵμ������⻯����Һ�����ɹ۲쵽��ĭ״��������Ȫһ����ӿ������
��֪��2H2O2(l)=2H2O(l)+O2(g) ��H=��196kJ/mol�����Ea=76kJ/mol������I����ʱ���Ea��=57kJ/mol��
����H2O2��Һ�м���KI��Һ����������Ӧ�����з���I����IO��֮���ת����������д��������Ӧ�����ӷ���ʽ��
��Ӧ�ף�______________________��
��Ӧ�ң�______________________��
�ڷ�Ӧ��Ϊ���ȷ�Ӧ���Ҽķ�Ӧ����С���ҵķ�Ӧ���ʣ�����ͼ�л�����H2O2��Һ�м���KI��Ӧ���̵������仯ͼ��_______

(3)HI���ȶ�����ˮ��Һ����ǿ���ԡ�����0.lmol/LKI��Һ��NH4I���塢pH��ֽ���ʵ����֤�������ʡ�����ʵ�鷽����
��ǿ���ԣ�__________________________��
�ڲ��ȶ��ԣ�___________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����10 L�ܱ������У�1 mol A��3 mol B��һ�������·�Ӧ��A(g)��xB(g)![]() 2C(g)��2 min��Ӧ�ﵽƽ��ʱ����û�����干3.4 mol������0.4 mol C�������м�������ȷ����
2C(g)��2 min��Ӧ�ﵽƽ��ʱ����û�����干3.4 mol������0.4 mol C�������м�������ȷ����
A. ƽ��ʱ�����ʵ���֮��n(A)��n(B)��n(C)��2��11��4
B. xֵ����3
C. A��ת����Ϊ20%
D. B��ƽ����Ӧ����Ϊ0.4 mol��L��1��min��1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ�������������·�Ӧ��ȡ����������NaNO2��NH4Cl===NaCl��N2����2H2O�����ڸ÷�Ӧ������˵����ȷ���ǣ� ��
A��ÿ����1 mol N2ת�Ƶĵ��ӵ����ʵ���Ϊ6 mol
B��N2���������������ǻ�ԭ��
C��NH4Cl�еĵ�Ԫ�ر���ԭ
D��NaNO2��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���绯ѧ���������������ڼ�����NH3�ĺ������乤��ԭ��ʾ��ͼ���¡�����˵������ȷ����( )
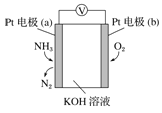
A����Һ��OH-��缫a�ƶ�
B��O2�ڵ缫b�Ϸ�����ԭ��Ӧ
C����Ӧ���ĵ�NH3��O2�����ʵ���֮��Ϊ 4:5
D���缫 a �ķ�ӦʽΪ 2NH3-6e-+6OH-��N2+6H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������л��ţ�-CH3��-OH��-COOH��-C6H6���������ɵ��л�����
A. 3�� B. 4�� C. 5�� D. 6��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������һ����Ҫ�Ļ���ԭ�ϣ���ҵ�������������Ҫ�����У���1����ӦN2��g��+3H2��g��![]() 2NH3��g����H<0 ������ʱ����N2��H2�Ļ���������2L�ܱ������У�10���Ӻ�Ӧ�ﵽƽ������ͼ������ȷ��ʾ�ù�����������ı仯����__________����ѡ����ĸ����
2NH3��g����H<0 ������ʱ����N2��H2�Ļ���������2L�ܱ������У�10���Ӻ�Ӧ�ﵽƽ������ͼ������ȷ��ʾ�ù�����������ı仯����__________����ѡ����ĸ����

(2)һ���¶��£����ܱ������г���1molN2��3molH2������Ӧ���������ݻ��㶨���ﵽƽ��״̬ʱ������������ʵ�����ԭ����7/10����N2��ת����a1=________��
������������ټ���1molN2��3molH2���ﵽƽ��״̬ʱ��N2��ת����Ϊa2����a2________a1���>������<����=������
��3��2NO��g��+O2��g��![]() 2NO2(g)��������������ͬʱ���ֱ���NO��ƽ��ת�����ڲ�ͬѹǿ��P1��P2�����¶ȱ仯�����ߣ���ͼ����
2NO2(g)��������������ͬʱ���ֱ���NO��ƽ��ת�����ڲ�ͬѹǿ��P1��P2�����¶ȱ仯�����ߣ���ͼ����

�ٱȽ�P1��P2�Ĵ�С��ϵ��P1____P2���>������<����=������
�����¶����ߣ��÷�Ӧƽ�ⳣ���仯��������__________��
��4�����᳧��������2�ַ�������β����
�ٴ���ԭ������������ʱ��H2��NO2��ԭΪN2��
��֪��2H2��g��+O2��g��=2H2O��g����H=-483.6kJ/mol
N2��g��+2O2��g��=2NO2��g����H=+67.7kJ/mol
��H2��ԭNO2����ˮ������Ӧ���Ȼ�ѧ����ʽ��________________________________��
�ڼ�Һ���շ�����Na2CO3��Һ����NO2����CO2����ÿ4.6gNO2��Na2CO3��Һ��Ӧʱת�Ƶ�����Ϊ0.05mol����Ӧ�����ӷ���ʽ��___________________________________________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com