
下列说法正确的是( )
A.离子化合物的熔点一定比共价化合物的高
B.二氧化碳分子中存在共价键和分子间作用力
C.非极性键也可以存在于化合物中
D.甲烷、氨和水都是由极性键结合而成的极性分子
科目:高中化学 来源:2014高考化学苏教版总复习 专题2从海水中获得的化学物质练习卷(解析版) 题型:选择题
某溶液中含有0.005 mol FeBr2及其他物质,向该溶液中通入134.4 mL(标准状况)Cl2,溶液中只有FeBr2与Cl2反应,则通入Cl2后溶液中可能大量存在的离子是( )
A.Fe2+、Fe3+、Br-、NO3-
B.Fe3+、H+、NO3-、K+
C.Fe3+、Br-、NO3-、Cl-
D.Fe2+、Br-、NO3-、Cl-
查看答案和解析>>
科目:高中化学 来源:2014高考化学苏教版总复习 专题13化学与技术练习卷(解析版) 题型:选择题
化学工业是国民经济的支柱产业。下列生产过程中不涉及化学变化的是( )
A.氮肥厂用氢气和氮气合成氨
B.钢铁厂用热还原法冶炼铁
C.硫酸厂用接触法生产硫酸
D.炼油厂用分馏法生产汽油
查看答案和解析>>
科目:高中化学 来源:2014高考化学苏教版总复习 专题12物质结构与性质练习卷(解析版) 题型:填空题
LED照明是我国制造业为人类做出的一大贡献。目前市售LED晶片,材质基本以GaAs(砷化镓)、AlGaInP(磷化铝镓铟)、InGaN(氮化铟镓)为主。已知镓是铝同族下一周期的元素。砷化镓的晶胞结构如下图。试回答:
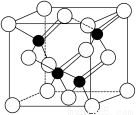
(1)镓的基态原子的电子排布式是__________。
(2)砷化镓晶胞中所包含的砷原子(白色球)个数为__________,与同一个镓原子相连的砷原子构成的空间构型为__________。
(3)N、P、As处于同一主族,其氢化物沸点由高到低的顺序是__________。(用氢化物分子式表示)
(4)砷化镓可由(CH3)3Ga和AsH3在700℃时制得。(CH3)3Ga中镓原子的杂化方式为__________。
(5)比较二者的第一电离能:As__________Ga(填“<”、“>”或“=”)。
(6)下列说法正确的是__________(填字母)。
A.砷化镓晶胞结构与NaCl相同
B.GaP与GaAs互为等电子体
C.电负性:As>Ga
D.砷化镓晶体中含有配位键
查看答案和解析>>
科目:高中化学 来源:2014高考化学苏教版总复习 专题12物质结构与性质练习卷(解析版) 题型:选择题
NH3、H2O等是极性分子,CO2、BF3、CCl4等是极性键构成的非极性分子。根据上述事实可推出ABn型分子是非极性分子的经验规律是( )
A.在ABn分子中A原子的所有价电子都参与成键
B.在ABn分子中A的相对原子质量应小于B的相对原子质量
C.在ABn分子中每个共价键的键长都相等
D.分子中不能含有氢原子
查看答案和解析>>
科目:高中化学 来源:2014高考化学苏教版总复习 专题11有机化学基础练习卷(解析版) 题型:填空题
已知烃B分子内C、H原子个数比为1∶2,相对分子质量为28,核磁共振氢谱显示分子中只有一种化学环境的氢原子,且有如下的转化关系:
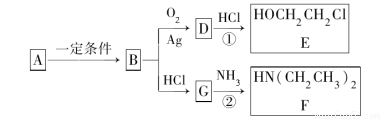
(1)B的结构简式是__________。
(2)A可能属于下列哪类物质__________。
a.醇 b.卤代烃 c.酚 d.羧酸
(3)反应①是D与HCl按物质的量之比1∶1的加成反应,则D的分子式是__________。反应②可表示为:G+NH3―→F+HCl(未配平),该反应配平后的化学方程式为______________________。
化合物E和F是合成药品普鲁卡因的重要中间体,普鲁卡因的合成路线如下
(4)甲的结构简式是__________。由甲苯生成甲的反应类型是__________。
(5)乙中有两种含氧官能团,反应③的化学方程式是____________________。
(6)普鲁卡因有两种水解产物丁和戊。
①戊与甲互为同分异构体,戊的结构简式是______________________。
②戊经聚合反应制成的高分子纤维广泛应用于通讯、宇航等领域。该聚合反应的化学方程式为______________________。
查看答案和解析>>
科目:高中化学 来源:2014高考化学苏教版总复习 专题11有机化学基础练习卷(解析版) 题型:选择题
下列物质分别与NaOH的醇溶液共热后,能发生消去反应,且生成物只有一种的是 ( )
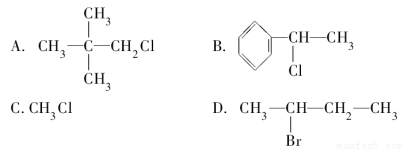
查看答案和解析>>
科目:高中化学 来源:2014高考化学苏教版总复习 专题10化学实验基础练习卷(解析版) 题型:实验题
已知某酸性土壤浸取液中除Fe3+外,还含有一定量Mg2+和Al3+。请设计合理实验检验该浸取液中的Mg2+、Al3+。
限选实验用品与试剂;烧杯、试管、玻璃棒、滴管、玻璃片、pH试纸;浸取液、20%KSCN、0.1 mol·L-1 NaOH、6 mol·L-1 NaOH、0.1 mol·L-1 HCl、蒸馏水。
必要时可参考:
沉淀物 | 开始沉淀时的pH | 沉淀完全时的pH |
Mg(OH)2 | 9.6 | 11.1 |
Fe(OH)3 | 2.7 | 3.7 |
根据你设计的实验方案,叙述实验操作、预期现象和结论。(测定溶液pH的具体操作可不写)
实验操作 | 预期现象和结论 |
步骤1: |
|
步骤2: |
|
步骤3: |
|
…… |
|
查看答案和解析>>
科目:高中化学 来源:2014高考化学名师选择题专练 离子反应练习卷(解析版) 题型:选择题
下列离子方程式表达正确的是( )
A.氢氧化铁溶于氢碘酸:Fe(OH)3+3H+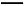 Fe3++3H2O
Fe3++3H2O
B.小苏打溶液呈碱性的原因:HC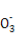 +H2O
+H2O H3O++C
H3O++C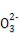
C.稀硝酸中加入足量的铁屑:3Fe+8H++2N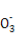
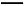 3Fe2++2NO↑+4H2O
3Fe2++2NO↑+4H2O
D.向硫酸铝铵[NH4Al(SO4)2]溶液中滴加少量Ba(OH)2溶液:N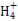 +Al3++2S
+Al3++2S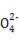 +2Ba2++5OH-
+2Ba2++5OH-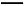 Al
Al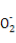 +2BaSO4↓+NH3·H2O+2H2O
+2BaSO4↓+NH3·H2O+2H2O
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com