
【题目】向2L的密闭容器中充入7.6mol NO和3.8mol O2 , 发生如下反应: ①2NO(g)+O2(g)2NO2(g)
②2NO2(g)N2O4(g)
测得NO2和N2O4的浓度变化如图所示,0~10min维持容器温度为T1℃,10min后升高并维持容器的温度为T2℃.下列说法正确的是( )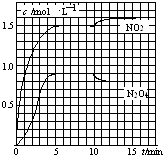
A.前5min反应的平均速率v(N2O4)=0.36mol(Lmin)﹣1
B.T1℃时反应②的化学平衡常数K=0.6
C.反应①、②均为吸热反应
D.若起始时向该容器中充入3.6mol NO2和2.0mol N2O4 , T1℃达到平衡时,N2O4的转化率为10%
【答案】D
【解析】解:A、前5min反应的平均速率v(N2O4)= ![]() =
= ![]() =0.18mol(Lmin)﹣1 , 故A错误; B、T1℃时反应②的化学平衡常数K=
=0.18mol(Lmin)﹣1 , 故A错误; B、T1℃时反应②的化学平衡常数K= ![]() =
= ![]() =0.4L/mol,故B错误;
=0.4L/mol,故B错误;
C、在该题中,升高温度后,二氧化氮的浓度增加,四氧化二氮的浓度减小,所以平衡②逆向移动,该反应是放热的,故C错误;
D、若起始时向该容器中充入3.6mol NO2和2.0mol N2O4 , 则Qc=0.31<K,所以反应正向进行,T1℃达到平衡时,
2NO2(g) | N2O4(g) | |
初始: | 1.8 | 1.0 |
变化: | 2x | X |
平衡: | 1.8-2x | 1.0+x |
则 ![]() =0.4,解得x=0.1,即N2O4的转化率为10%,故D正确.
=0.4,解得x=0.1,即N2O4的转化率为10%,故D正确.
故选D.
A、根据化学反应速率v= ![]() 来计算化学反应速率;
来计算化学反应速率;
B、化学平衡常数K= ![]() ,代入相关数据来计算即可;
,代入相关数据来计算即可;
C、根据温度对化学平衡移动的影响:升高温度,化学平衡向着吸热方向进行,反之向着放热方向进行,据此来判断反应的吸放热;
D、根据转化率= ![]() 来计算即可.
来计算即可.


科目:高中化学 来源: 题型:
【题目】迷迭香酸是从蜂花属植物中提取得到的酸性物质,其结构如图.下列叙述正确的是( ) 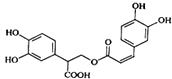
A.迷迭香酸属于芳香烃
B.1mol迷迭香酸最多能和8mol 氢气发生加成反应
C.迷迭香酸不可以发生加聚和缩聚反应
D.1mol迷迭香酸最多能和含6 mol NaOH的水溶液完全反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】辉铜矿主要成分Cu2S,此外还含有少量SiO2、Fe2O3等杂质,软锰矿主要含有MnO2 , 以及少量SiO2、Fe2O3等杂质.研究人员开发综合利用这两种资源,用同槽酸浸湿法冶炼工艺,制备硫酸锰晶体和碱式碳酸铜.主要工艺流程如图: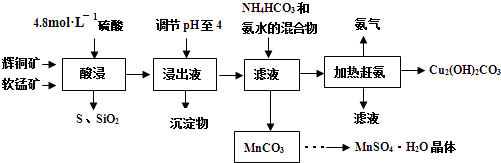
已知:
①MnO2有较强的氧化性,能将金属硫化物中的硫氧化为单质硫;
②[Cu(NH3)4]SO4常温稳定,在热水溶液中会分解生成NH3;
③部分金属阳离子生成氢氧化物沉淀的pH范围(开始沉淀和完全沉淀的pH):
Fe3+:1.5~3.2 Mn2+:8.3~9.8 Cu2+:4.4~6.4
④MnSO4H2O溶于1份冷水、0.6份沸水,不溶于乙醇.
(1)实验室配制250mL 4.8molL﹣1的稀硫酸,所需的玻璃仪器除玻璃棒、量筒、烧杯以外还需要 .
(2)酸浸时,为了提高浸取率可采取的措施有(任写一点).
(3)酸浸时,得到浸出液中主要含有CuSO4、MnSO4等.写出该反应的化学方程式: .
(4)调节浸出液pH=4的作用是 .
(5)本工艺中可循环使用的物质是(写化学式).
(6)获得的MnSO4H2O晶体需要进一步洗涤、干燥,洗涤时应用洗涤.
(7)测定MnSO4H2O样品的纯度:准确称取样品14.00g,加蒸馏水配成100mL溶液,取出25.00mL用标准的BaCl2溶液测定,完全反应后得到了4.66g沉淀,则此样品的纯度为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列科学家及对应的成就正确的是( )
A. 道尔顿—提出原子学说B. 阿伏伽德罗—提出元素概念
C. 门捷列夫—提出燃烧的氧化说D. 波义尔—提出分子学说
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图示为一种天然产物,具有一定的除草功效.下列有关该化合物的说法错误的是( ) 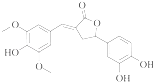
A.分子中含有三种含氧官能团
B.1 mol该化合物最多能与6molNaOH反应
C.既可以发生取代反应,又能够发生加成反应
D.既能与FeC13发生显色反应,也能和Na2CO3反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据所学知识,完成题目:
(1)Ⅰ含氮的化合物在化学反应中变化复杂.现用如图3所示仪器(夹持装置己省略及药品,探究亚硝酸钠与硫酸反应及气体产物的成分.
已知:①NO+NO2+2OH﹣═2NO2﹣+H2O
②气体液化的温度:NO2 21℃、NO﹣152℃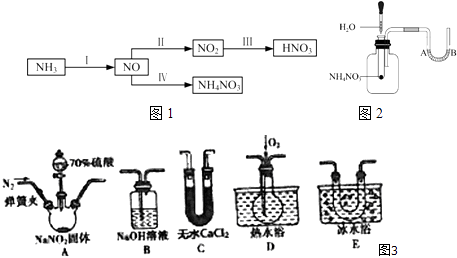
a.为了检验装置A中生成的气体产物,上述仪器的连接顺序(按左→右连接)为
b.反应前应打开弹簧夹,先通入一段时间氮气,排除装置中的空气,目的是:
c.在关闭弹簧夹,滴入70%硫酸后,A中产生红棕色气体.
①盛装70%浓硫酸的仪器名称是
②实验确认有NO的现象是
d.通过上述实验探究过程,可得出装置A中反应的化学方程式是 .
(2)Ⅱ.NH3经一系列反应可以得到HNO3和NH4NO3 , 如图1所示.【资料卡片】
①NH4NO3是一种白色晶体,易溶于水,微溶于乙醇.
②在230℃以上时,同时有弱光:2NH4NO3=2N2↑+O2↑+4H2O
③在400℃以上时,剧烈分解发生爆炸:4NH4NO3=3N2↑+2NO2↑+8H2O
a.如图2将水滴入盛有硝酸铵的试管中,观察到的A处液面上升,B处液面下降,产生该现象的原因 .
b.实验室可以用氯化铵和熟石灰反应来制备氨气,该反应的化学方程式是(填“能”或“不能”)用硝酸铵代替氯化铵.
c.在汽车发生碰撞时,NaN3会产生(填化学式)气体充满安全气囊来减轻碰撞事故中乘员伤害程度.
d.完成离子反应IV:NO+H2O=++H+ .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯吡格雷(Clopidogrel)是一种用于抑制血小板聚集的药物.以A为原料合成氯吡格雷的路线如下:
已知:R﹣CHO ![]()
![]() ,R﹣CN
,R﹣CN ![]() RCOOH
RCOOH
请回答下列问题:
(1)A中含氧官能团的名称为 , C﹣D的反应类型是 .
(2)Y的结构简式为 , 在一定条件下Y与BrCl(一氯化溴,与卤素单质性质相似)按物质的量1:1发生加成反应,生成的产物可能有种.
(3)C分子间可在一定条件下反应生成含有3个六元环的产物,该反应的化学方程式为 .
(4)由E转化为氯吡格雷时,生成的另一种产物的结构简式为 .
(5)写出A的所有同分异构体(芳香族化合物)的结构简式:(不考虑立体异构).
(6)请结合题中信息写出以 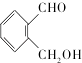 为有机原料制备化合物
为有机原料制备化合物 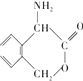 的合成路线流程图(无机试剂任选) . (合成路线流程图示例如下:CH3CH2OH
的合成路线流程图(无机试剂任选) . (合成路线流程图示例如下:CH3CH2OH ![]() CH=CH2
CH=CH2 ![]()
![]() )
)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于相同物质的量的SO2与SO3,下列说法正确的是( )
A.硫元素的质量比为5:4 B.原子总数之比为4:3
C.质量之比为1:1 D.分子数之比为1:1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com