
高一化学期终质量检测试题(卷)
2008.6
注意事项:
1.本试题分为第Ⅰ卷1至3页, 第Ⅱ卷4至6页。 满分100分。
2.答第Ⅰ卷前,考生务必将答题卡及第Ⅱ卷密封线内项目填写清楚。
3.考生答题时,必须将第Ⅰ卷上所有题的正确答案用2B铅笔涂在答题卡上所对应的信息点处,答案写在Ⅰ卷上无效。第Ⅱ卷答在答题卷上。
可能用到的相对原子质量:H
第Ⅰ卷 (选择题,共50分)
一.选择题(仅一个选项符合题意, 1-10题2分,11-20题3分,共50分)
1.通常用于衡量一个国家石油化工发展水平的标志是 ( )
A.石油的产量 B.乙烯的产量 C.天然气的产量 D.硫酸的产量
2.下列物质中,不属于有机物的是 ( )
A.苏打 B.酒精 C.尿素 D.塑料
3.下列有关环境保护的说法中错误的是 ( )
A.含氮、磷化合物的生活污水大量排放可使水体富营养化
B.各国工业大量排放二氧化硫是全球气候变暖的主要原因
C.劣质装修材料中的甲醛、苯、氡气等对人体有害
D.废旧电池中的汞、镉、铅等重金属盐对土壤和水源会造成污染
4.下列有关甲烷性质的叙述,正确的是 ( )
A.甲烷是一种无色,有臭味的气体
B.甲烷易溶于水
C.甲烷与氯气发生的化学反应类型属于置换反应
D.CH2Cl2没有同分异构体可以说明甲烷分子的空间结构是正四面体不是正方形
5.下列物质中加入金属钠不产生氢气的是 ( )
A.乙醇 B.乙酸 C.水 D.苯
6.下列物质中, 不能使酸性KMnO4溶液褪色的物质是 ( )
A. SO2 B. FeSO
7.下列相关结论不正确的是 ( )
A.降低温度能减小化学反应速率
B.催化剂能加快化学反应速率
C.反应物浓度越小,化学反应速率越快
D.反应物之间接触面积越大,化学反应速率越快
8.符合下列分子式的有机物没有同分异构现象的是 ( )
A.CH4 B.C4H
9.有关化学用语正确的是 ( )

10.下列物质不互为同分异构体的是 ( )
A. 葡萄糖和果糖 B.蔗糖和麦芽糖
C.正丁烷和异丁烷 D.淀粉和纤维素
11.下列物质不能发生水解反应的是 ( )
A.油脂 B.麦芽糖 C.葡萄糖 D.蛋白质
12.下列反应中能检验尿液中存在葡萄糖的是 ( )
A.加金属钠,看是否有氢气放出
B.与新制的Cu(OH)2悬浊液混合煮沸,观察有无红色沉淀生成
C.与醋酸和浓硫酸共热,看能否发生酯化反应
D.加入饱和碳酸钠溶液中看是否分层
13.下列有关说法正确的是 ( )
A.家用食盐是纯净物
B.乙烯、苯分子中所有原子共平面
C.实验室用苯、溴水、三氯化铁制备溴苯
D.硝基、羟基、氯原子、苯环、甲基都是官能团
14.可以用来鉴别甲烷和乙烯,还可以用来除去甲烷中乙烯的操作方法是 ( )
A.将混合气体通过盛有硫酸的洗气瓶
B.将混合气体通过盛有足量溴水的洗气瓶
C.将混合气体通过盛有水的洗气瓶
D.将混合气体通过盛有澄清石灰水的洗气瓶
15.市场上有一种加酶洗衣粉,它是在洗衣粉中加入少量的碱与蛋白酶制成的。蛋白酶的催化活性很强,衣物的汗渍、血迹及人体排放的蛋白质、油渍遇到它,都能水解而除去。下列衣料中,不能用加酶洗衣粉洗涤的是 ( )
①棉织品 ②毛织品 ③腈纶织品 ④丝织品
A.① B.② ③ C.① ③ D.② ④
16.下列选项中的哪种物质可以与氧化铁在高温下发生铝热反应 ( )
A.焦炭 B.一氧化碳 C.氧化铝 D.金属铝粉
17.用
A. 生成的水分子中含有18O B.生成的乙酸乙酯中含有18O
C.可能生成
18.1mol丙烯与氯气完全加成后所得产物再与氯气彻底取代,两个过程中共用氯气( )
A. 5mol B. 6mol C. 7mol D. 8mol
19.现有 ①乙酸乙酯和乙酸钠溶液、② 乙醇和丁醇、③ 溴化钠溶液和溴水的三组混合液,分离它们的正确方法依次是 ( )
A.分液、萃取、蒸馏 B. 萃取、蒸馏、分液
C. 分液、蒸馏、萃取 D.蒸馏、萃取、分液
20.某学生进行蔗糖的水解实验,并检验水解产物中是否含有葡萄糖。他的实验操作如下:取少量纯蔗糖加水配成溶液;在蔗糖溶液中加入3~5滴稀硫酸;将混合液煮沸几分钟、冷却;在冷却后的溶液中加入银氨溶液,在水浴中加热。实验结果没有银镜产生。其原因是 ( )
A.蔗糖尚未水解 B.蔗糖水解的产物中没有葡萄糖
C.加热时间不够 D.煮沸后的溶液中没有加碱,以中和作催化剂的酸
高一化学期终质量检测试题(卷)
第Ⅱ卷(非选择题 共50分)
请同学注意: 第Ⅱ卷答在第5―6页答题卷上
二.填空题(本题包括21题4分、22题5分、23题8分 共17分)
21.某校食堂中餐食谱如下:
主食:大米饭 配菜:红烧排骨 煎鸡蛋 炸鸡腿 豆腐汤 炒猪肝
主食和配菜中的营养物质主要含维生素 、 、 、无机盐和水等营养素,考虑到各种营养成分的均衡搭配,应该增加含VC的配菜是 。
22.有下列各组微粒或物质:
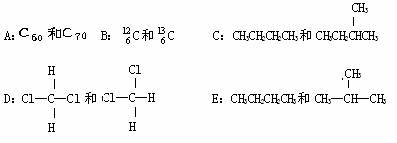
① 组两种微粒互为同位素; ② 组两种物质互为同素异形体;
③ 组两种物质属于同系物; ④ 组两物质互为同分异构体;
⑤ 组两物质是同一物质。
23.一种混合物由鸡蛋清溶液和淀粉溶液混合而成,如要检出其中含有淀粉,应取少量混合液,向其中滴加 ,现象为 ;如要检出其中的鸡蛋清,则应另取少量混合液,并向其中滴加 ,现象为 。
三.实验推断题(本题包括2小题,24题15分、25题10分 共25分)
24. 全球海水中溴的藏量丰富,约占地球溴总藏量的99%,故溴有“海洋元素”
之称,海水中溴含量为65mg/L。其工业提取方法有:
(1)空气吹出纯碱吸收法。方法是将氯气通入到富含溴离子的海水中,使溴置换出来,再用空气将溴吹出,用纯碱溶液吸收,最后用硫酸酸化,即可得到溴单质。该方法涉及到的反应有:① (写出离子方程式);②3Br2+3CO32―=BrO3―+ 5Br―+3CO2↑;③BrO3―+ 5Br―+6H+=3Br2+3H2O。其中反应②中氧化剂是 ;还原剂是 。
(2)空气吹出SO2吸收法。该方法基本同(1),只是将溴吹出后是用SO2来吸收的,使溴转化为氢溴酸,然后再用氯气氧化氢溴酸即得单质溴。写出溴与二氧化硫反应的离子反应方程式: 。
(3)溶剂萃取法。该法是利用单质溴在水中和溶剂中溶解度的不同的原理来进行的。实验室中萃取用到的实验仪器名称是 。下列可以用于海水中溴的萃取试剂是 。
①乙醇 ②四氯化碳 ③硝酸 ④裂化汽油
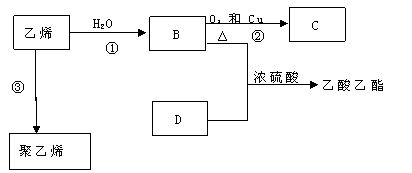 25.已知乙烯能发生以下转化:
25.已知乙烯能发生以下转化:
(1)乙烯的结构式为: 。
(2)写出下列化合物官能团的名称:B中含官能团名称 ;D中含官能团名称 ;
(3)写出反应的化学方程式
①: 反应类型:
②: 反应类型:
③: 反应类型:
4 : 反应类型:
四.计算题(本题包括1小题,8分)
26.海洋约占地球表面积的71%,具有十分巨大的开发潜力。某校研究性学习小组同学对经初步净化处理的浓缩海水(主要含NaCl和MgSO4)进行研究。
(1)实验时,若配制1000mL 0.20mol/L NaOH溶液,计算称量固体NaOH的质量。
(2)取初步净化处理的浓缩海水100mL,加入200mL 0.20mol/L NaOH溶液,恰好将其中的Mg2+完全沉淀,求浓缩海水中Mg2+的物质的量浓度。
(3)研究小组同学把上述沉淀过滤,向滤液中加入足量的氯化钡溶液,又能产生沉淀的量为多少?
高一化学期终质量检测试答题(卷)
2008.6
第Ⅱ卷(非选择题 共50分)
题 号
二
三
四
总 分
总分人
21
22
23
24
25
26
得 分
复核人
二.填空题(本题包括21题4分、22题5分、23题8分 共17分)
21. 、 、 、,
应该增加含VC的配菜是 。
22. ① 组两种微粒互为同位素; ② 组两种物质互为同素异形体;
③ 组两种物质属于同系物; ④ 组两物质互为同分异构体;
⑤ 组两物质是同一物质。
23. 滴加 ,现象为 ;
滴加 ,现象为 ;
三.实验推断题(本题包括2小题,24题10分、25题15分 共25分)
24.(1)① (写出离子方程式)
反应②中氧化剂是 ;还原剂是 。
(2)离子反应方程式: 。
(3)实验仪器名称是 。萃取试剂是 。
25.
(1)乙烯的结构式为: 。
(2)写出下列化合物官能团的名称:
B中含官能团名称 ;D中含官能团名称 ;
(3)写出反应的化学方程式
①: 反应类型:
②: 反应类型:
③: 反应类型:
4:B+D 反应类型:
四.计算题(本题包括1小题, 8)
26.解
2008.6
一、选择题(1―10题每空2分,11―20题每空3分;共50分)
1
2
3
4
5
6
7
8
9
10
B
A
B
D
D
C
C
A
A
D
11
12
13
14
15
16
17
18
19
20
C
B
B
B
D
D
A
C
C
D
二.填空题(21题4 分,22题 5分, 23题8分,共17分)
21. (每空1分,共4分)
糖类; 蛋白质; 油脂; 蔬菜
22.(每空1分 共5分)
B ; A; C; E; D
23.(每空2分 共8分)
碘水 、 溶液呈蓝色 ; 浓硝酸 、 有黄色凝聚物。
三.实验推断题(24题10分,25题15分。共25分)
24.(本题10分)
(1)Cl2+2Br-=2Cl-+Br2 ; Br2 Br2 (4分)
(2)Br2+SO2+2H2O=2HBr+H2SO4; (2分)
(3)分液漏斗 ②。 (4分)
25. (1)(1分)
(1)(1分)
(2)羟基 ; 羧基 (每空1分,共2分 )
(3)(共12分。化学方程式每空2分,化学式错误,没配平0分;
反应类型每空1分,错别字0分。)
 ①CH2==CH2+H2O CH3―CH2―OH
加成反应
①CH2==CH2+H2O CH3―CH2―OH
加成反应
 ②2CH3―CH2OH+O2
②2CH3―CH2OH+O2
 2CH3―CHO+2H2O 氧化反应
2CH3―CHO+2H2O 氧化反应


 ③nCH2==CH2 [CH2―CH2 ]n
聚合反应
③nCH2==CH2 [CH2―CH2 ]n
聚合反应
4CH3CH2OH+CH3COO CH3COOCH2CH3+H2O 酯化反应
CH3COOCH2CH3+H2O 酯化反应
四.计算题(8分)
26.解:⑴配制氢氧化钠溶液需
n(NaOH)=0.2mol/L*
m(NaOH)=0.2mol*
⑵海水中n(Mg2+)
=0.20mol/L *
c(Mg2+)= 0.02 mol/
⑶n(BaSO4) =n(SO42-)= n(Mg2+)=0.02 mol, (1分)
m(BaSO4)=
(其他合理答案参照给分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com