2006-2007学年度江苏省溧水县第一学期期中试卷
第Ⅰ卷(选择题,共25分)
可能用到的相对原子质量:H―l
C―12
N一14 O一16 Cl一35.5 K一39 Mn一55
一、选择题(每小题1分,本题共15分。每小题只有一个选项符合题意。)
1.下列变化中属于化学变化的是
( )
A.冰雪融化
B.木材燃烧
C.矿石粉碎
D.酒精挥发
试题详情
2.“墙角数枝梅,凌寒独自开。遥知不是雪,为有暗香来”(王安石《梅花》)。诗人在远处就能闻到淡淡的梅花香味的原因是
( )
A.分子很小
B.分子是可以再分
C.分子之间有间隔
D.分子在不断地运动
试题详情
3.下列常见物质中,属于纯净物的是
( )
A.新鲜空气
B.氧气
C.澄清的石灰水
D.河水
试题详情
试题详情
试题详情
5.以下是空气污染指数与质量级别、质量状况的对应关系:
空气污染指数
0--50
51-100
101-200
201--300
>300
空气质量状况
优
良
轻度污染
中度污染
重度污染
空气质量级别
I
Ⅱ
Ⅲ
Ⅳ
V
2005年6月3日,空气污染指数为82~93,根据以上信息,判断当天的空气质量级别和空气质量状况分别是 ( )
A.I级;优
B.Ⅱ级;良
C.Ⅲ级;轻度污染
D.V级;重度污染
试题详情
6.居里夫人在1898年从几吨的含铀废料中提炼出0.3克镭。已知镭元素的核电荷
数为88,相对原子质量为226,则镭原子的核外电子数为 ( )
A.226
B.138
C.88 D.314
试题详情
7.在我们的日常生活中,出现了含氟牙膏、高钙牛奶、加碘食盐、增铁酱油、富硒茶叶等商品,这些商品中的氟、钙、碘、铁、硒应理解为
( )
A.元素
B.分子
C.单质
D.原子
试题详情
8.航天飞船常用铝粉与高氯酸铵(NH4ClO4)的混合物作为固体燃料,高氯酸铵中Cl元素的化合价为
( )
A.+1
B.+3
C.+5
D.+7
试题详情
9.下列粒子在人体中起着重要的作用,其中属于阴离子的是
( )
试题详情
试题详情
试题详情
A.2KClO3 2KCl + 3O2↑
B.4P + 5O2 2P2O5
试题详情
试题详情
 C.Zn +CuSO4 Cu + ZnSO4
D.CH4
+ 2O2
CO2+2H2O
C.Zn +CuSO4 Cu + ZnSO4
D.CH4
+ 2O2
CO2+2H2O
试题详情
 11.在X+3O2 2CO2+3H2O中,根据质量守恒定律,X的化学式应为 ( )
11.在X+3O2 2CO2+3H2O中,根据质量守恒定律,X的化学式应为 ( )
A.C2H4O2 B.CH4O
C.C2H6O D.CH4
试题详情
12.为了探究水电解的微观过程,玉玲同学做了一些分子、原子的模型,其中能保持氢气化学性质的粒子模型是
( )
试题详情
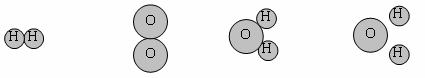
A、
B、 C、
D、
试题详情
13.下列对应关系错误的是
( )
A.氧气――供人呼吸
B.二氧化碳――造成酸雨
C.氮气――作保护气
D.稀有气体――做电光源
试题详情
14.下列实验现象的描述错误的是
( )
A.
铁丝在氧气中燃烧火星四射
B.
铁钉与硫酸铜溶液反应时铁钉表面有红色物质生成
C.
镁条在空气中燃烧发出耀眼的强光
D.
红磷在氧气中燃烧产生大量浓雾
试题详情
15.经调查我国是严重缺水国家,在全国600多个城市中有400多个城市供水不足,其中110个城市严重缺水。下列做法中有利于节约用水的是 ( )
A.洗脸、刷牙时,不间断地放水
B.洗澡擦肥皂时不关喷头,任水流淌
C.洗菜、淘米的水用来浇花、拖地、冲厕所
D.任由水龙头漏水而不及时修理
试题详情
二、选择题 (本题共10分。每小题有1~2个选项符合题意。按题意选对给2分,错选、多选不给分,少选且选对给1分)
16、下列气体中,常可以用于充入食品包装袋防腐的是 ( )
A.氧气、氩气
B.氢气、氦气
C.二氧化碳、氮气
D.二氧化硫、二氧化氮
试题详情
17.同学们喜欢的油炸食品中,含有一种叫丙烯醛(化学式C2H4O)的有毒物质。下列有关丙烯醛的说法正确的是
( )
A.它是由碳、氢、氧三种元素组成的
B.它的一个分子中含有两个氢分子
C.它的相对分子质量为56
D.丙烯醛中碳、氢、氧元素的质量比为2∶4∶1
试题详情
18.观察右图中的有关操作和现象,判断下列叙述正确的是
( )
试题详情
 A.
集气瓶中的气体可能是空气
A.
集气瓶中的气体可能是空气
B.
集气瓶中的气体可能是CO2
C.
集气瓶中的气体一定不是O2
D.
集气瓶中的气体一定是N2
试题详情
19.下列现象可用质量守恒定律解释的是
( )
A.
高锰酸钾受热完全分解后,残留固体质量变少了
B.
100g水受热后变成100g水蒸气
C.
蜡烛受热熔化,冷却后质量不变
D.
镁在空气中燃烧后,生成物的质量增加了
试题详情
20.下图表示宇宙飞船发动机内氢气和氧气燃烧生成水的微观过程。下列说法错误的是
( )
A.氢气、氧气和水都是由分子构成的
B.氢气和氧气燃烧生成水的过程中,分子种类发生了改变
C.氢气和氧气燃烧生成水的过程中,原子种类没有发生改变
D.氢气、氧气、水都是化合物
试题详情

第Ⅱ卷(非选择题,共55分)
试题详情
三、(本题共15分)
21.(4分)用化学符号填空。
2个水分子
3个氮原子
铝元素
试题详情
试题详情
22.(5分)⑴通过探究物质构成的奥秘,我们知道,物质是由原子等粒子构成的。请在下图方框中填写粒子名称,表示各种粒子是怎样构成物质的。
试题详情

Mg
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Na Al Si P S Cl Ar ①从原子结构示意图分析,此周期排列的依据是
; ②在此周期中,原子结构变化情况是
; ③在此周期中,元素化学性质的变化情况是
; ④在此周期中,元素种类的变化情况是
。 ⑤请预测原子序数为19的原子的电子层数是
。
试题详情
 23.(3分)右图所示是电解水的装置,反应一段时间以后。 23.(3分)右图所示是电解水的装置,反应一段时间以后。
⑴与正极相连的乙试管内产生的气体是
,检验该气体的方法是
; ⑵甲、乙两试管内汇集的气体体积比约为
。 试题详情
24.(3分)下列实验技能都是你必须具备的,你能作出正确回答吗? ⑴如何判断玻璃仪器已经洗涤干净?
。 ⑵加热氯酸钾制氧气,用排水法收集,何时开始?
。 ⑶洒出的酒精在桌上燃烧起来,如何处理? 。 试题详情
四、(本题共26分) 25.(6分)按要求写出下列反应的方程式,并注明反应的类型 ⑴用电解海水的方法来制取新能源氢气,是一种理想的提取能源的方法。
___________________
__________;(
)反应。 ⑵工业上的湿法冶金原理,就是用铁与硫酸铜溶液反应来置换铜。 _____________
___ ________;( )反应。 ⑶新制备的灰黑色铁粉暴露在空气中却能迅速燃烧生成红色的三氧化二铁粉末。 _____________
___
_________;(
)反应。 ⑷碱式碳酸铜[Cu2(OH)2CO3]受热后生成三种氧化物,其中一种是黑色粉末氧化铜,另一种是能使澄清石灰水变浑浊的气体。 _____________
___
_________;(
)反应。 试题详情
26.(5分)⑴铁中上的铁轨,每隔一段距离就有一条不小的“缝隙”;铺设好的水泥路面,必须用电锯每隔一段距离就割出一条“缝隙”。这些“缝隙”在夏季和冬季的宽度还不一样。请你用粒子(分子)知识解释,这些“缝隙”的作用。
。 试题详情
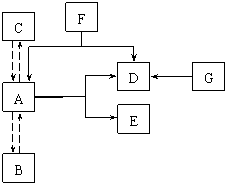 ⑵ 自然界中存在着氧循环、碳循环、水循环等。 ⑵ 自然界中存在着氧循环、碳循环、水循环等。
如右图所示, 其中A、B、C就是这些循环中的一 种化合物的三种自然状态,A为密度最大时的状态。 D具有助燃性和氧化性,能与许多物质发生剧烈地、 或缓慢地氧化反应。G是暗紫色固体,加热时生成 D和另二种固体, 其中一种可作F 分解反应的催 化剂。试回答下列问题:
图 物质变化的关系图 的名称
和化学式
。 ②写出F反应的化学方程式
。 ③写出已知的E物质的化学性质和反应现象
。
试题详情
27.(6分)⑴苏丹红是一种人工合成的红色染料。最新研究表明,其在人体内的代谢产物有强致突变性和致癌性,国家正在严查添加有苏丹红的食品。已知最常见的一种苏丹红的化学式为C16H12NO,试计算苏丹红的: ①相对分子质量:
;②各元素的质量比:
; ③苏丹红中氮元素的质量分数。 试题详情
⑵已知标准状况下氮气的密度为1.250g/L,氧气的密度为1.429g/L。请解答下列问题: ①空气中氮气和氧气的质量比约为
。 试题详情
②成年人每分钟大约吸入肺泡内氧气8L,有资料记载人呼出的气体中氧气仍有15.7%,通过计算回答:为获得这些氧气,每分钟需要吸入大约多少升空气? 试题详情
28.(9分)水是宝贵的自然资源,在工业生产和日常生活中有极其广泛的应用: ⑴小丽同学用烧杯分别取少量井水和蒸馏水,加入适量
,搅拌,发现蒸馏水中泡沫多,而井水中出现浮渣,结论: 是硬水。在日常生活中可以用 方法达到软化硬水的目的。 ⑵自来水厂的自来水生产过程中,在过滤池中放有活性炭层,活性炭起
作用,该过程发生的是
变化。 ⑶自然界中采集到的湖水、河水的水样,一般比较浑浊,可通过
(填一种操作)的方法,得到较澄清的水样。应选用的仪器有(填序号):
。 试题详情
⑷某化学兴趣小组的同学研究学校门前的小河净化问题,有人提出建议:①打开闸门,让河水直接流入长江;②在闸门上安装阻隔垃圾网;③教育附近居民不要往河里倒垃圾;④居民的用含磷的洗衣粉洗衣后的水可以直接排放到河里;⑤在河里适当种植水生植物,利用植物净水,你认为上述建议合理的是(填序号)
,不合理(只需说明某一方面)的原因是
。 五、(本题共14分) 试题详情
29、(4分)某化学兴趣小组根据下图装置进行实验室制取气体的探究。请你参与并回答: 试题详情
⑴用高锰酸钾制氧气的化学方程式为
,用A和E装置进行实验时,发现水槽中的水变成紫红色,原因是
。 ⑵停止加热时,为了防止水倒流,应进行的操作是
。 试题详情
 30、(5分)研究性学习小组的同学为探究空气中氧气的体积分数,设计了 30、(5分)研究性学习小组的同学为探究空气中氧气的体积分数,设计了
如下图所示装置。请根据图示实验回答下列问题: ⑴闭合电源开关,可观察到白磷________ _________。
⑵装置冷却到室温时,可观察到U形管内左侧液面________ __。 ⑶通过这个实验得出的结论是_____ ___
。 ⑷此实验还可推知反应后剩余气体的两点性质是:___________ __; _____________ ___。 试题详情
31、(5分)某校兴趣小组进行“氧气制备及其性质探究”的实验。请根据以下实验事实答题。 ⑴甲同学分别在右图所示的三个装置内,加入适量的二氧化锰,然后注入5%的双氧水,仔细观察、思考并记录如下: 试题详情
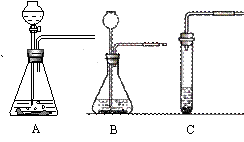 ①三支试管内都迅速产生大量气体,并有白雾出现。 ①三支试管内都迅速产生大量气体,并有白雾出现。
②C试管中反应最早停止。 ③B装置可通过长颈漏斗添加双氧水,使反应继续。 ④A装置可通过调节活塞,保持反应平稳持续进行。 ⑤用手握住三个容器的底部,感觉微热。 ⑥A装置能持续、稳定地产生O2,便于控制。 ⑦C装置一次产生O2量有限,不便于添加双氧水。 你认为甲同学的上述记录中,属于描述现象的是(填序号,下同)
,属于实验结论的是
。 ⑵乙同学称取等质量的氯酸钾和高锰酸钾,分别进行加热制取O2(在氯酸钾中加入适量二氧化锰),结果发现当操作基本相同的情况下,氯酸钾分解产生O2体积,远远多于高锰酸钾分解产生O2的体积。乙同学猜想:氯酸钾中氧元素质量分数大于高锰酸钾中氧元素质量分数。你认为乙同学的假设是(填:对或否)
;其原因是
。 ⑶丙同学用制取的两瓶氧气,分别进行木炭、蜡烛燃烧的实验,发现木炭、蜡烛在空气和氧气中燃烧,发光发热的现象有明显的不同。 根据丙同学上述实验现象,你能得出的结论是
。 试题详情
| | | | | |






 C.Zn +CuSO4 Cu + ZnSO4
D.CH4
+ 2O2
CO2+2H2O
C.Zn +CuSO4 Cu + ZnSO4
D.CH4
+ 2O2
CO2+2H2O 11.在X+3O2 2CO2+3H2O中,根据质量守恒定律,X的化学式应为 ( )
11.在X+3O2 2CO2+3H2O中,根据质量守恒定律,X的化学式应为 ( )
 A.
集气瓶中的气体可能是空气
A.
集气瓶中的气体可能是空气







 2个镁离子
2个镁离子