
2007年滨州市中等学校招生统一考试
理科综合试题化学试题
温馨提示:
1.本试题分第Ⅰ卷和第Ⅱ卷两部分。第Ⅰ卷1~6页为选择题,共52分;第Ⅱ卷7~l4页为非选择题,共98分。满分l50分。考试时间为150分钟。
2.请将第Ⅰ卷正确答案的字母代号用28铅笔涂在答题卡上,第Ⅱ卷答案用蓝黑色钢笔 或圆珠笔直接答在试卷上。
3.答题前,请将密封线内的项目填写清楚。
化学部分可能用到的相对原子质量:
H 1 C l2 N 14 0 16 Mg 24 S 32 C 135.5 Ca 40 Cu 64 Zn 65
第Ⅰ卷(选择题共52分)
一、选择题(以下各题的四个选项中只有一个正确答案,1~12题每小题l分,l3~32题每小题2分,共52分)
13.生活与化学有着密切的联系,下列在生产和生活中的变化属于物理变化的是
A.在家中,用稀醋酸除去热水瓶内壁上的水垢
B.在葡萄酒厂,把葡萄酿制成葡萄酒
C.在建筑上,把生石灰与水混合搅拌,制成石灰浆
D.在农业上,为缓解旱情,用干冰进行人工降雨
14.下列关于环境保护问题,描述错误的是
A.“白色污染”主要是指白色粉尘对环境造成的污染
B.将废旧电池集中回收,统一处理
C.公园里的大理石雕像被腐蚀,这主要是酸雨所致
D.不合格装饰材料中常含有甲醛、苯等致癌物,会导致室内空气污染
15.下列关于实验室制取氧气的说法中正确的是
A.先在试管中装入高锰酸钾,再检查装置的气密性
B 只有二氧化锰能作双氧水分解的催化剂
C.用双氧水与二氧化锰制取氧气的反应属于分解反应
D.用排水法收集氧气,先把导管伸入集气瓶中,再加热高锰酸钾
16.诺贝尔奖获得者丁肇中在实验中,曾用到我国研制的一种闪烁晶体材料BGO(化学式为: Bi4Ge3O12),其中锗(Ge)元素为+4价,则铋(Bi)元素的化合价为
A.+1价 B.+2价 C.+3价 D.+4价
17.图2形象地表示了某反应前后反应物与生成物分子及数目的变化,其中“◆◆”、
 ”分别表示A、B、C三种不同的分子,该反应的化学方程式中A、B、C
”分别表示A、B、C三种不同的分子,该反应的化学方程式中A、B、C
前的化学计量数之比为

A.3:1:2 B.4:1:4 C.5:1:2 D.5:1:4
18.下列关于金属的说法中,正确的是
A.合金是一种纯净物
B.在钢铁表面镀一层锌,可有效防止钢铁的生锈
C.地壳中含量最多的金属元素是铁元素
D.在任何条件下,不锈钢都不会生锈
19.在一定温度下,向100g饱和的NaCl溶液中加入100g水,所得溶液的有关叙述正确的是 A.溶液仍然饱和 B.溶质质量分数不变
C.溶液质量增加了一倍 D.该温度下,NaCl的溶解度变小了
20.下列关于pH的测定方法和有关说法正确的是
A.把pH试纸浸入待测试液中,测定溶液的pH
B.将玻璃棒用蒸馏水清洗后,立即蘸取待测试液滴在pH试纸上,测定溶液的pH
C.用pH试纸测得某食醋的pH为3.6
D.通常把pH小于5.6的降水称为酸雨,pH越小,雨水的酸性越强
21.将一根头发放在火上灼烧,闻到一股烧焦羽毛的气味。请你判断,头发的主要成分是 A.脂肪 B.蛋白质 C.维生素 D.纤维素
22.将50g镁、锌、铜的混合物与足量的稀硫酸充分反应后,过滤、干燥,得固体20g,再将滤液蒸干后,又得到174g固体(已换算成无水硫酸盐)。则反应产生氢气的质量是
A.2g B.3g C.3.5g D.4g
第Ⅱ卷(非选择题 共98分)
化学部分(共30分)
三、填空题(每空l分,共l4分)
39.用化学符号或化学式填空
(1)3个钙离子 . (2)小苏打
40.芬太奴是强有力的麻醉剂,在军事上作为“非致命武器”曾被用作解救人质,其化学式为C20H24N20。芬太奴 (填“是”或“不是”)有机化合物;在芬太奴中所含质量分数最小的元素是 (填元素符号)。
41.我们要了解生活中一些基本的化学图标,请写出图标“ ”为
标志。
”为
标志。
42.图l0是―瓶浓硫酸试剂瓶上的标签,现要配制lO0g20%的稀硫酸。
(1)计算需要该浓硫酸的体积为 mL(结果精确到小数点后l位)。
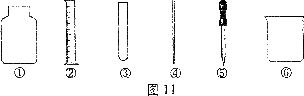
(2)配制时,在图11中须用到的仪器有 (填序号)。

43.写出Al与CuS04溶液反应的化学方程式 。小亮想验证Al与CuS04溶液的反应情况,他将一久置在空气中的铝片放人硫酸铜溶液中,一段时间后取出铝片,未观察到铝片表面有任何变化,原因可能是 ;要使实验成功,需要预先进行的操作是
44.一种优质打火机的燃料(其化学式用R代替)燃烧时发生的反应是:
R+5O2 3CO2+4H2O,由此可推知该打火机燃料的化学式为
3CO2+4H2O,由此可推知该打火机燃料的化学式为
45.酸、碱、盐溶解性表是学习化学的重要工具,下表列出了“部分酸、碱、盐在20%时的溶解性”。
 氢氧根离子或酸根离子
氢氧根离子或酸根离子
 溶解性
溶解性
氢离子或金属离子
OH-
Cl-
S02-4
CO2-3
PO3-4
H+
溶
挥
溶
溶
挥
溶
K+
溶
溶
溶
溶
溶
Ba2+
溶
溶
不
不
不
Cu2+
不
溶
溶
不
不
说明:“溶”表示此种物质可溶于水,“不”表示不溶于水,“微”表示微溶于水,“挥”表示挥发性。
请利用该表中的有关信息完成下列任务:
(1)查Ba3(P04)2的溶解性 ;
(2)写一种复合肥料的化学式 ;
 (3)写一种既生成不溶性碱又生成不溶性盐的复分解反应
。
(3)写一种既生成不溶性碱又生成不溶性盐的复分解反应
。
四、实验与探究题(46小题4分,47小题6分,共l0分)
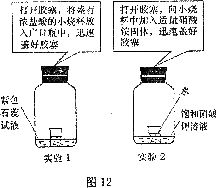
46.某化学兴趣小组做了如图l2的两个实验:
(1)“实验1”中广口瓶内液体的现象是 ;产生此现象的原因是 。
(2)“实验2”中广口瓶内液体的现象是 ;产生此现象的原因是 。
 47.实验课上,小华和小明两位同学合作探究碳酸钠粉末与稀盐酸的反应是否适合实验室制取二氧化碳。他们用图l3所示装置进行实验,先向试管中加入半药匙碳酸钠粉末,再注人2mL稀盐酸,观察到的现象是
;反应的化学方程式为
。
47.实验课上,小华和小明两位同学合作探究碳酸钠粉末与稀盐酸的反应是否适合实验室制取二氧化碳。他们用图l3所示装置进行实验,先向试管中加入半药匙碳酸钠粉末,再注人2mL稀盐酸,观察到的现象是
;反应的化学方程式为
。
小华根据反应的实际情况,认为碳酸钠粉末与稀盐酸不适合用于实验室制取二氧化碳气体,理由是 。
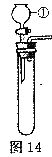 小明认真思考后,认为碳酸钠粉末与稀盐酸反应也可用于实验室制取二氧化碳。他将装置进行了改进,如图l4所示。实验时,他通过旋转仪器①上的活塞来控制盐酸的流量,从而达到控制反应速率的目的,实验最终取得了成功。请你写出仪器①的名称
。
小明认真思考后,认为碳酸钠粉末与稀盐酸反应也可用于实验室制取二氧化碳。他将装置进行了改进,如图l4所示。实验时,他通过旋转仪器①上的活塞来控制盐酸的流量,从而达到控制反应速率的目的,实验最终取得了成功。请你写出仪器①的名称
。
若将碳酸钠粉末换成碳酸钠的浓溶液,与稀盐酸反应制取二氧化碳气体,使用图l4所示装置,是否合适? (填“是”或“否”)
[反思与结论]:实验结论受实验装置、实验条件等的限制,改变实验装置或实验条件可能会得出不同的实验结论。
[拓展与应用]:请你举一通过改变实验条件得出不同实验结论的实例。
五、计算题(共6分)
48.某化学兴趣小组为了测定一批石灰石样品中碳酸钙的质量分数,取用25g石灰石样品,平均分成5份依次加人到60g稀盐酸中(样品中除碳酸钙外,其余的成分既不与盐酸反应,也不溶解于水),充分反应后经过滤、干燥等操作,最后称量,得实验数据如下表:
石灰石的用量
剩余固体的总质量
第一次加入5g
1g
第二次加人5g
2g
第三次加入5g
3g
第四次加入5g
8g
第五次加入5g
13g
(1)从表中数据可知,这五次实验中,第 次 石灰石样品中的碳酸钙与稀盐酸恰好完全反应。
(2)求石灰石样品中碳酸钙的质量分数;
(3)计算该化学兴趣小组所用稀盐酸中溶质的质量分数。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com