
题目列表(包括答案和解析)
下图是无机物A~H在一定条件下的转化关系(部分反应中参加反应的水未列出)。其中,A是一种带有结晶水的正盐,B是形成酸雨的主要物质,G是一种常见的二元强酸,E是一种红棕色粉末。
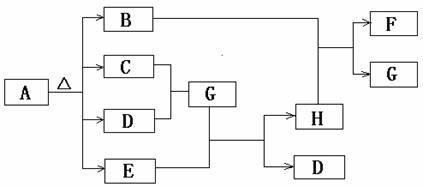
请填写下列空白:
(1)简述B形成的酸雨对环境的危害 (至少二点);
(2)配制F的溶液时要加 ;
(3)写出B+H→F+G的离子方程式 ;
(4)若A分解产生的B、C、D、E的质量比为16∶20∶63∶40,则A的化学式为 。
| ||
| ||
| ||
| ||
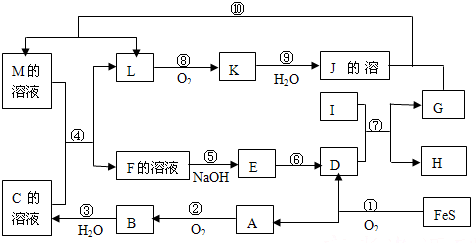
已知A、B、E是常见的非金属单质,C是导致酸雨的主要成分之一,Y是生活中常中的金属单质.D、K是重要的无机化工产品.X含有两种元素,具有摇篮式的分子结构,其球棍模型如图所示.H为白色沉淀.下列转化关系中部分反应条件和产物略去.


试回答下列问题
(1)X的化学式为:________;G的电子式________;
(2)反应④的化学方程式:________;反应③的离子方程式:________;
(3)①~⑥反应中属于氧化还原反应的是(填编号)________;
(4)已知在真空中,将A与CuO按物质的量1∶1反应可生成A2O.写出该反应的化学方程式:________;
(5)依据实验中的特征实验现象,可确定Y是何种金属,该实验现象为________.
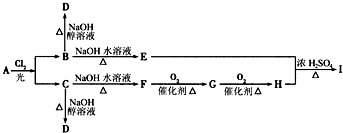

已知:有机物A的相对分子质量为134;经分析可知,其中氢和氧的质量分数之和为19.4%,其余为碳。有机物A、E中均含有苯环结构,且苯环上的一溴代物只有两种,它们都能与FeCl3溶液发生显色反应;有机物C能发生银镜反应。下图表示有机物A~H的转化关系。?

请回答下列问题:?
(1)化合物A中含有的碳原子数为 ,该化合物的分子式是 。?
(2)写出下列化合物的结构简式:?
A ,C ,E 。?
(3)写出由F发生臭氧化还原水解反应生成G的化学反应式(有机物写结构简式): 。
(4)化合物H(C7H6O2)的含有苯环且侧链无其他环的所有同分异构体共有______种。?
题号
1
2
3
4
5
6
7
8
答案
C
D
B
B
D
C
A
A
题号
9
10
11
12
13
14
答案
CD
AD
C
A
BD
B
15、(本题共10分)
(1)CO32-水解成碱性,Cu2+与OH‑结合生成Cu(OH)2 (合理给分)。 (2分)
(2)取最后一次洗涤液,滴加BaCl2溶液,无沉淀生成,说明已洗净。(2分)
(3)CuSO4、澄清石灰水 (每个1分,名称和化学式搞混不给分,共2分)
(4)B中无水硫酸铜变蓝,澄清石灰水不变浑浊(每点1分,共2分)
(5)装置中原有的空气有影响;实验结束后装置中残留的气体不能被吸收;石灰水可能会吸收空气中的CO2。(2分,说出二点即可)
16、(本题共8分)
(1)腐蚀建筑物、桥梁、工业设备、运输工具;直接破坏农作物、草原、森林;使土壤、湖泊酸化。(说出其中二点即可)(2分)
(2)铁粉和稀硫酸(2分)
(3) 2Fe3+ + SO2 +2 H2O = 2Fe2+ + SO42- + 4H+ (2分)
(4) FeSO4?7H2O (2分)
17、(本题共10分)
(1) A D (每个1分,共2 分,有错不给分)
(2) A
(3) X=2 (2分) , A (2分)
(4) 1/1620(或6.17×10-4) (2分)
18.(10分)
(1)重金属离子会使蛋白质变性(2分)
(2)① Cr2O72- + 6Fe2+ + 14H+ = 2Cr3+ + 6Fe3+ + 7H2O (2分)
② Cr3+ + 4OH- = CrO2- + 2H2O (2分)
③ 8~10 (2分)
(3)② (以下任意2条即可)(2分)
其它条件相同时,含铬废渣掺入的比例越大,Cr元素浸出的浓度越高;
酸性环境对Cr元素浸出有抑制作用;
冻融对Cr元素浸出影响不明显;
曝晒对Cr元素浸出影响不明显;
……
19、(共12分)
(1)消去反应 (1分)
(2) 、CH3CHO、 (每空1分,共3分)
(3)CH3COOCH2CH3、CH3CH2COOCH3、CH3CH2CH2COOH、(CH3)2CHCOOH
(对一个得1分,错一个倒扣1分,共4分)
(4)CH3CH(OH)CH(OH)CH3 +2C6H5COOHCH3CH(OOCC6H5)CH(OOCC6H5)CH3+2H2O(2分)
(5)(2分)
20.(10分)
⑴ 16.8 (2分)
⑵NO3―
(每个2分,共6分)
(3)解:3Fe2+ + NO3- + 4H+ = 3Fe3++NO↑+2H2O
0.3mol 0.6mol 0.2mol
Fe2+、NO3-过量,故产生NO气体:0.2mol÷4×22.4 L/mol=1.12L (2分)
21.(每小题2分,共12分)
(1)H2S、NH2- (2)A (3)BC
(4)3d104s1 Cr (5)共价键、配位键
(6)降低Cu(NH3)4SO4?H2O的溶解度
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com