
ƒø¡–±Ì(∞¸¿®¥∞∏∫ÕΩ‚Œˆ)
ƒ≥–£ªØ—ß—–æø–‘—ßœ∞–°◊È£¨‘⁄—ßœ∞Ω Ùµƒ“±¡∂“‘∫Û∂‘“ª—ıªØúªπ‘≠Ω Ù—ıªØŒÔµƒ µ—È∑«≥£∏––À»§£¨À˚√«≤È‘ƒ”–πÿ◊ ¡œ∫Û∑¢œ÷£¨“ª—ıªØúµƒ÷∆±∏ø…¿˚”√º◊À·∫Õ≈®¡ÚÀ·π≤»»µΩ60°´80 °Ê∑¢…˙Õ—ÀÆ∑¥”¶÷∆»°£∫
HCOOH CO°¸£´H2O
CO°¸£´H2O
«Î∏˘æð“‘œ¬∏˜Õº∞ÔÀ˚√«◊È◊∞≥…“ªÃ◊œý∂‘∫œ¿Ìµƒ µ—È◊∞÷√Õº(ƒ≥–©◊∞÷√ø…÷ÿ∏¥ π”√)°£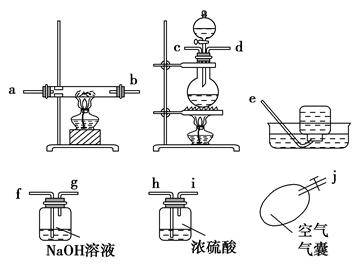
ªÿ¥“‘œ¬Œ £∫
(1)∫œ¿Ì µ—È◊∞÷√µƒ¡¨Ω”À≥–Ú «(–¥–°–¥◊÷ƒ∏) °£
(2)‘⁄∑¥”¶ ±“ª∂®“™œ»Õ®“ªª·“ª—ıªØú∆¯Ã£¨»ª∫Û‘Ÿµ„»ºº”»»—ıªØÃ˙µƒæ∆æ´µ∆£¨‘≠“Ú « °£
| A£Æ“ÚŒ™“ª∞„∑¥”¶¥”◊ÛµΩ”“Ω¯–– |
| B£Æ≈≈≥˝ÃÂœµƒ⁄µƒø’∆¯£¨ π∑¥”¶π˝≥Ã∏¸∞≤»´ |
| C£Æº◊À·”Î≈®¡ÚÀ·∑¥”¶ø…“‘≤˙…˙¥Û¡øµƒCO |
| D£Æ¥À∑¥”¶º”»» ±º‰≥§”–¿˚”⁄≤˙…˙CO |

 CO°¸+H2O «Î∏˘æð“‘œ¬∏˜ÕºΩ¯––—°‘Ò–Œ≥…“ªÃ◊œý∂‘ΩœŒ™∫œ¿Ìµƒ µ—È◊∞÷√Õº£®ƒ≥–©◊∞÷√ø…÷ÿ∏¥ π”√£©
CO°¸+H2O «Î∏˘æð“‘œ¬∏˜ÕºΩ¯––—°‘Ò–Œ≥…“ªÃ◊œý∂‘ΩœŒ™∫œ¿Ìµƒ µ—È◊∞÷√Õº£®ƒ≥–©◊∞÷√ø…÷ÿ∏¥ π”√£© 
 CO°¸£´H2O
CO°¸£´H2O
| A£Æ“ÚŒ™“ª∞„∑¥”¶¥”◊ÛµΩ”“Ω¯–– |
| B£Æ≈≈≥˝ÃÂœµƒ⁄µƒø’∆¯£¨ π∑¥”¶π˝≥Ã∏¸∞≤»´ |
| C£Æº◊À·”Î≈®¡ÚÀ·∑¥”¶ø…“‘≤˙…˙¥Û¡øµƒCO |
| D£Æ¥À∑¥”¶º”»» ±º‰≥§”–¿˚”⁄≤˙…˙CO |
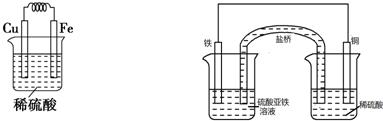

 ƒ≥–£ªØ—ß—–æø–‘—ßœ∞–°◊È”˚…˺∆ µ—È—È÷§Fe°¢CuµƒΩ ÙªÓ∂Ø–‘£¨À˚√«Ã·≥ˆ¡À“‘œ¬¡Ω÷÷∑Ω∞∏£Æ«Îƒ„∞Ô÷˙À˚√«ÕÍ≥…”–πÿ µ—ȜӃø£∫
ƒ≥–£ªØ—ß—–æø–‘—ßœ∞–°◊È”˚…˺∆ µ—È—È÷§Fe°¢CuµƒΩ ÙªÓ∂Ø–‘£¨À˚√«Ã·≥ˆ¡À“‘œ¬¡Ω÷÷∑Ω∞∏£Æ«Îƒ„∞Ô÷˙À˚√«ÕÍ≥…”–πÿ µ—ȜӃø£∫
“ª°¢—°‘Ò£®±æÂπ≤10∑÷£©£¨√ø–°Ã‚2∑÷£¨÷ª”–“ª∏ˆ’˝»∑—°œÓ°£
|