
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
| ЮяжЪ | ШМЩеШШЃЈkJ?mol-1ЃЉ |
| H2ЃЈgЃЉ | 285.8 |
| COЃЈgЃЉ | 283.0 |
| CH3CH2OHЃЈlЃЉ | 1365.5 |
| ЦЯЬбЬЧЃЈsЃЉ | 2800 |
| ађКХ | A | B | C | D | E |
| ЮлЫЎРраЭ | ЩњЛюЮлЫЎ | гЁШО | ЕчЖЦ | дьжН | СђЫсЙЄвЕЗЯЫЎ |
| CODжЕЃЈmg/LЃЉ | 520 | 870 | 20 | 960 | 120 |
ЃЈ10ЗжЃЉжТРфМСЪЧвЛжжвзБЛбЙЫѕЁЂвКЛЏЕФЦјЬхЃЌвКЛЏКѓдкЙмФкбЛЗЃЌеєЗЂЪБЮќЪеШШСПЃЌЪЙЛЗОГЮТЖШНЕЕЭЃЌДяЕНжТРфФПЕФЁЃШЫУЧдјВЩгУЙ§ввУбЁЂNH3ЁЂCH3ClЕШзїжТРфМС ЃЌЕЋЫќУЧВЛЪЧгаЖООЭЪЧвзШМЩеЁЃгкЪЧПЦбЇМвИљОндЊЫиаджЪЕФЕнБфЙцТЩРДПЊЗЂаТЕФжТРфМС ЁЃОнЯжгажЊЪЖЃЌФГаЉдЊЫиЛЏКЯЮяЕФвзШМадЁЂЖОадБфЛЏЧїЪЦШчЯТЃК
ЃЈ1ЃЉЧтЛЏЮяЕФвзШМадЃКЕкЖўжмЦкЃК______>______>H2O>HFЃЛЕкШ§жмЦкЃКSiH4> PH3>H2S>HClЁЃ
ЃЈ2ЃЉЛЏКЯЮяЕФЖОадЃКPH3>NH3;H2S_____H2O; CS2_____CO2; CCl4>CF4гкЪЧПЦбЇМвУЧПЊЪМАбзЂвтСІМЏжадкКЌFЁЂClЕФЛЏКЯЮяЩЯЁЃ
ЃЈ3ЃЉвбжЊCCl4ЕФЗаЕуЮЊ76.8ЁуCЃЌCF4ЕФЗаЕуЮЊ-128ЁуCЃЌаТЕФжТРфМСЕФЗаЕуЗЖЮЇгІНщгкЦфМфЁЃОЙ§НЯГЄЪБМфЗДИДЪдбщЃЌвЛжжаТЕФжТРфМСЗњРяАКCF2Cl2жегкЕЎЩњСЫЃЌЦфЫћРрЫЦЕФЛЙПЩвдЪЧ________________ЁЃвбжЊМзЭщЪЧе§ЫФУцЬхНсЙЙ,дђCF2Cl2_____ЃЈЬюгаЛђепЮоЃЉЭЌЗжвьЙЙЬхЁЃ
ЃЈ4ЃЉШЛЖјЃЌетжжжТРфМСдьГЩСЫЕБНёФГвЛЛЗОГЮЪЬтЪЧЦЦЛЕГєбѕВуЃЌЕЋЧѓжњгкжмЦкБэжадЊЫиМАЛЏКЯЮяЕФ__________________ЃЈЬюаДађКХЃЉБфЛЏЧїЪЦРДПЊЗЂжТРфМСЕФПЦбЇбЇЮЌЗНЗЈЪЧжЕЕУНшМјЕФЁЃЂйЖОад ЂкЗаЕу ЂлвзШМад ЂмЫЎШмад ЂнбеЩЋ
ЃЈ10ЗжЃЉжТРфМСЪЧвЛжжвзБЛбЙЫѕЁЂвКЛЏЕФЦјЬхЃЌвКЛЏКѓдкЙмФкбЛЗЃЌеєЗЂЪБЮќЪеШШСПЃЌЪЙЛЗОГЮТЖШНЕЕЭЃЌДяЕНжТРфФПЕФЁЃШЫУЧдјВЩгУЙ§ввУбЁЂNH3ЁЂCH3ClЕШзїжТРфМС ЃЌЕЋЫќУЧВЛЪЧгаЖООЭЪЧвзШМЩеЁЃгкЪЧПЦбЇМвИљОндЊЫиаджЪЕФЕнБфЙцТЩРДПЊЗЂаТЕФжТРфМС ЁЃОнЯжгажЊЪЖЃЌФГаЉдЊЫиЛЏКЯЮяЕФвзШМадЁЂЖОадБфЛЏЧїЪЦШчЯТЃК
ЃЈ1ЃЉЧтЛЏЮяЕФвзШМадЃКЕкЖўжмЦкЃК______>______>H2O>HFЃЛЕкШ§жмЦкЃКSiH4> PH3 >H2S>HClЁЃ
ЃЈ2ЃЉЛЏКЯЮяЕФЖОадЃКPH3>NH3; H2S_____H2O; CS2_____CO2; CCl4>CF4гкЪЧПЦбЇМвУЧПЊЪМАбзЂвтСІМЏжадкКЌFЁЂClЕФЛЏКЯЮяЩЯЁЃ
ЃЈ3ЃЉвбжЊCCl4ЕФЗаЕуЮЊ76.8ЁуCЃЌ CF4ЕФЗаЕуЮЊ-128ЁуCЃЌаТЕФжТРфМСЕФЗаЕуЗЖЮЇгІНщгкЦфМфЁЃОЙ§НЯГЄЪБМфЗДИДЪдбщЃЌвЛжжаТЕФжТРфМСЗњРяАКCF2Cl2жегкЕЎЩњСЫЃЌЦфЫћРрЫЦЕФЛЙПЩвдЪЧ________________ЁЃвбжЊМзЭщЪЧе§ЫФУцЬхНсЙЙ,дђCF2Cl2_____ЃЈЬюгаЛђепЮоЃЉЭЌЗжвьЙЙЬхЁЃ
ЃЈ4ЃЉШЛЖјЃЌетжжжТРфМСдьГЩСЫЕБНёФГвЛЛЗОГЮЪЬтЪЧЦЦЛЕГєбѕВуЃЌЕЋЧѓжњгкжмЦкБэжадЊЫиМАЛЏКЯЮяЕФ__________________ЃЈЬюаДађКХЃЉБфЛЏЧїЪЦРДПЊЗЂжТРфМСЕФПЦбЇбЇЮЌЗНЗЈЪЧжЕЕУНшМјЕФЁЃЂйЖОад ЂкЗаЕу ЂлвзШМад ЂмЫЎШмад ЂнбеЩЋ
жТРфМСЪЧвЛжжвзБЛбЙЫѕЁЂвКЛЏЕФЦјЬхЃЌвКЛЏКѓдкЙмФкбЛЗЃЌеєЗЂЪБЮќЪеШШСПЃЌЪЙЛЗОГЮТЖШНЕЕЭЃЌДяЕНжТРфФПЕФЁЃШЫУЧдјВЩгУЙ§ввУбЁЂNH3ЁЂCH3ClЕШзїжТРфМС ЃЌЕЋЫќУЧВЛЪЧгаЖООЭЪЧвзШМЩеЁЃгкЪЧПЦбЇМвИљОндЊЫиаджЪЕФЕнБфЙцТЩРДПЊЗЂаТЕФжТРфМС ЁЃОнЯжгажЊЪЖЃЌФГаЉдЊЫиЛЏКЯЮяЕФвзШМадЁЂЖОадБфЛЏЧїЪЦШчЯТЃК
ЃЈ1ЃЉЧтЛЏЮяЕФвзШМадЃКЕкЖўжмЦкЃК______>______>H2O>HFЃЛЕкШ§жмЦкЃКSiH4> PH3 >H2S>HClЁЃ
ЃЈ2ЃЉЛЏКЯЮяЕФЖОадЃКPH3>NH3; H2S_____H2O; CS2_____CO2; CCl4>CF4гкЪЧПЦбЇМвУЧПЊЪМАбзЂвтСІМЏжадкКЌFЁЂClЕФЛЏКЯЮяЩЯЁЃ
ЃЈ3ЃЉвбжЊCCl4ЕФЗаЕуЮЊ76.8ЁуCЃЌ CF4ЕФЗаЕуЮЊ-128ЁуCЃЌаТЕФжТРфМСЕФЗаЕуЗЖЮЇгІНщгкЦфМфЁЃОЙ§НЯГЄЪБМфЗДИДЪдбщЃЌвЛжжаТЕФжТРфМСЗњРяАКCF2Cl2жегкЕЎЩњСЫЃЌЦфЫћРрЫЦЕФЛЙПЩвдЪЧ________________ЁЃвбжЊМзЭщЪЧе§ЫФУцЬхНсЙЙ,дђCF2Cl2_____ЃЈЬюгаЛђепЮоЃЉЭЌЗжвьЙЙЬхЁЃ
ЃЈ4ЃЉШЛЖјЃЌетжжжТРфМСдьГЩСЫЕБНёФГвЛЛЗОГЮЪЬтЪЧЦЦЛЕГєбѕВуЃЌЕЋЧѓжњгкжмЦкБэжадЊЫиМАЛЏКЯЮяЕФ__________________ЃЈЬюаДађКХЃЉБфЛЏЧїЪЦРДПЊЗЂжТРфМСЕФПЦбЇбЇЮЌЗНЗЈЪЧжЕЕУНшМјЕФЁЃЂйЖОад ЂкЗаЕу ЂлвзШМад ЂмЫЎШмад ЂнбеЩЋ
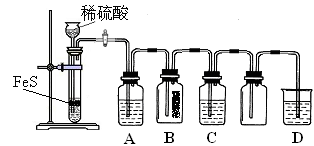
СђЛЏЧтЃЈH2SЃЉЪЧвЛжжОпгаГєМІЕАЦјЮЖЕФЮоЩЋЦјЬхЃЌгаОчЖОЃЛДцдкгкЖржжЩњВњЙ§ГЬвдМАздШЛНчжаЁЃдкШЫЬхЕФКмЖрЩњРэЙ§ГЬжавВЦ№зХживЊзїгУЁЃ
| зЪСЯЃКЂй H2SПЩШмгкЫЎЃЈдМ1ЃК2ЃЉЃЌЦфЫЎШмвКЮЊЖўдЊШѕЫсЁЃ Ђк H2SПЩгыаэЖрН№ЪєРызгЗДгІЩњГЩГСЕэЁЃ Ђл H2SдкПеЦјжаШМЩеЃЌЛ№бцГЪЕРЖЩЋЁЃ |
| | ЪЕбщВйзї | ЪЕбщЯжЯѓ |
| ЪЕбщ1 | НЋЕШХЈЖШЕФNa2SКЭNa2SO3ШмвКАДЬхЛ§БШ2ЁУ1ЛьКЯ | ЮоУїЯдЯжЯѓ |
| ЪЕбщ2 | НЋH2SЭЈШыNa2SO3ШмвКжа | ЮДМћУїЯдГСЕэЃЌдйМгШыЩйСПЯЁСђЫсЃЌСЂМДВњЩњДѓСПЧГЛЦЩЋГСЕэ |
| ЪЕбщ3 | НЋSO2ЭЈШыNa2SШмвКжа | гаЧГЛЦЩЋГСЕэВњЩњ |
 |  |  |  |
| A | B | C | D |
вЛЁЂбЁдёЬт
ЬтКХ
1
2
3
4
5
6
7
8
9
10
Д№АИ
C
B
D
D
C
D
C
C
B
B
ЖўЁЂбЁдёЬт
ЬтКХ
11
12
13
14
15
16
17
18
19
20
Д№АИ
D
A
D
C
D
B
D
D
A
C
Ш§ЁЂбЁдёЬт
ЬтКХ
21
22
23
24
25
26
27
28
29
30
Д№АИ
BC
BD
BD
D
B
C
C
A
BC
BD
ЬтКХ
31
32
33
34
Д№АИ
BC
B
AB
D
 ЫФЁЂЬюПеЁЂМђД№КЭМЦЫу
ЫФЁЂЬюПеЁЂМђД№КЭМЦЫу
 35. (1)
ЃЈ2ЃЉ
35. (1)
ЃЈ2ЃЉ
 |
ЃЈ3ЃЉ
ЃЈ4ЃЉBaCO3+2H+==Ba2++CO2Ёќ+H2O
 |
 ЃЈ5ЃЉCu+2H2SO4ЃЈХЈЃЉ===CuSO4+SO2Ёќ+2H2O
ЃЈ5ЃЉCu+2H2SO4ЃЈХЈЃЉ===CuSO4+SO2Ёќ+2H2O
36ЃЎ(1)Li дзгЪЇШЅвЛИіЕчзгКѓ, Li+вбОаЮГЩСЫЮШЖЈНсЙЙ,ДЫЪБдйЪЇШЅЕчзгКмРЇФбЁЃ
(2) C ЃЛ(3) ЂѓAзхЃЌЪЇШЅЕкЫФИіЕчзгЪБЫљашФмСПдЖдЖДѓгкЪЇШЅЧАШ§ИіЕчзгЫљашФмСП ЁЃ
37ЃЎЃЈ1ЃЉВњЩњАзЩЋГСЕэЃЌЪдвКБфГЩКьЩЋЃЛвђЮЊдкЫЎжаSO2КЭCl2ЗДгІЩњГЩбЮЫсКЭСђЫсЃЌЪЙЪЏШяЪдвКБфКьЩЋЃЌСђЫсгыBaCl2ШмвКЗДгІВњЩњBaSO4 ГСЕэЁЃ ЃЈ2ЃЉЂлЁЂSO3ЃЛЂкЁЂHClЃЛЂйЁЂSO2ЃЛЂлЁЂH2OЁЃ
38ЃЎ(14Зж)ЃЈ1ЃЉЬМЁЂбѕЁЂФЦЁЂСђЃЈ2ЃЉCO2+2OHЃ=H2O+CO32Ѓ
ЃЈ3ЃЉ
 ЁЃ
ЁЃ
39ЃЎЂХSiO2 Na2SiO3 H2SiO3
ЂЦ

40ЃЎ(1)
КЌгаSO ЛђSO
ЛђSO жаЕФвЛжжЛђСНжжЖМгаЁЃ
жаЕФвЛжжЛђСНжжЖМгаЁЃ
(2) BaCO3;ЃЈ3ЃЉ
BrЃЁЂS2Ѓ
; HCO (Г§SO
(Г§SO ЛђSO
ЛђSO вдЭт)
вдЭт)
41ЃЎЃЈ1ЃЉAlЃЛH2 ЃЛCl2ЃЈ2ЃЉЗЧН№ЪєЃЛ
ЁЁЁЁЃЈ3ЃЉбѕЛЏЮяЛђЧтЛЏЮяЃЛSiO2ЃЋ SiЃЋ2COЁќЛђO2+H2S
SiЃЋ2COЁќЛђO2+H2S 2H2O+SЃЈЦфЫќКЯРэД№АИОљПЩЃЉ
2H2O+SЃЈЦфЫќКЯРэД№АИОљПЩЃЉ
42ЃЎЃЈ1ЃЉ ЁЂ
ЁЂ ЃЛ
ЃЛ ЁЁЁЁЃЈ2ЃЉ
ЁЁЁЁЃЈ2ЃЉ ЃЛ
ЃЛ ЁЂ
ЁЂ ЁЁЃЈ3ЃЉ
ЁЁЃЈ3ЃЉ ЁЂ
ЁЂ ЃЛ
ЃЛ
43ЃЎНт: 0.5molYЕФРызгЕУЕН6.02ЁС1023ИіЕчзг(МД1molЕчзг)БЛЛЙдЮЊжааддзгЃЌЫљвд1molYгІЕУЕН2molЕчзгЛЙдЮЊжааддзгЃЌМДYРызггІДј2ИіДјЕчКЩЃЌдђЦфбѕЛЏЮяЕФЛЏбЇЪНгІЮЊYOЁЃ
YO + 2HClЃНYCl2+H2O
ЃЈY+16ЃЉg 2mol
Ёр ЃН
ЃН
ЁрYЃН24
гжЁпYКЫжажЪзгЪ§ЕШгкжазгЪ§ЃЌЁрYЕФжЪзгЪ§ЮЊ12ЃЌгІЪЧMgЃЌЮЛгкЕкШ§жмЦкЂђAзхЁЃ
MgO+2H+ЃНMg2++H2O
44ЃЎНтЃК
ЁЁЁЁгЩЗНГЬЪНПЩжЊЃК =nЃЈБЛЛЙдЕФ
=nЃЈБЛЛЙдЕФ ЃЉ
ЃЉ
ЁЁЁЁ
ЁЁЁЁ
45ЃЎ (1)aЁм2/3ЃЛ(2)aЁн2ЃЛ (3) 2/3<a<2, (1?a/2)mol
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com