
题目列表(包括答案和解析)
一定条件下铁可以和CO2发生反应:
Fe(s)+CO2(g)![]() FeO(s)+CO(g),已知该反应的平衡常数(K)与温度(T)的关系如图甲所示:
FeO(s)+CO(g),已知该反应的平衡常数(K)与温度(T)的关系如图甲所示:
 |
图乙
(1)一定温度下,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,反应过程中CO2气体和CO气体的浓度与时间的关系如图乙所示。8分钟内,CO的平均反应速率v(CO)= mol/(L·min)。
(2)下列措施中能使平衡时c(CO)/c(CO2)增大的是 (填序号)。
A.升高温度 B.增大压强 C.充入一定量CO D.再加入一些铁粉
(3)反应达到平衡后,若保持容器体积不变,再通入一定量的CO2气体,则CO2的转化率将 (填“增大”、“减小”、“不变”)。
(4)铁的重要化合物在生产生活中应用十分广泛。
①FeCl3溶液用于天然气脱硫,写FeCl3溶液与天然气中 反应的离子方程式: 。
②高铁酸钠(Na2FeO4)是一种新型饮用水消毒剂。高铁酸钠生产方法之一是在强碱性介质中用NaClO氧化Fe(OH)3生成高铁酸钠、氯化钠和水,该反应的离子方程式为 。
一定条件下铁可以和CO2发生反应:
Fe(s)+CO2(g)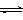 FeO(s)+CO(g),已知该反应的平衡常数(K)与温度(T)的关系如图甲所示:
FeO(s)+CO(g),已知该反应的平衡常数(K)与温度(T)的关系如图甲所示:
 |
图乙
(1)一定温度下,向某密闭容器中加入足量铁粉并充入一定量的CO2气体,反应过程中CO2气体和CO气体的浓度与时间的关系如图乙所示。8分钟内,CO的平均反应速率v(CO)= mol/(L·min)。
(2)下列措施中能使平衡时c(CO)/c(CO2)增大的是 (填序号)。
A.升高温度 B.增大压强 C.充入一定量CO D.再加入一些铁粉
(3)反应达到平衡后,若保持容器体积不变,再通入一定量的CO2气体,则CO2的转化率将 (填“增大”、“减小”、“不变”)。
(4)铁的重要化合物在生产生活中应用十分广泛。
①FeCl3溶液用于天然气脱硫,写FeCl3溶液与天然气中 反应的离子方程式: 。
②高铁酸钠(Na2FeO4)是一种新型饮用水消毒剂。高铁酸钠生产方法之一是在强碱性介质中用NaClO氧化Fe(OH)3生成高铁酸钠、氯化钠和水,该反应的离子方程式为 。
(10分)(1)一定条件下,发生反应CO (g)+H2O (g)  CO2(g) +H2 (g),向2 L密闭容器中通入2 mol CO (g)、1 mol H2O (g),2 min后反应达到平衡时,测得CO的物质的量为1.6mol,用H2O (g)表示该反应速率为________此温度下,该反应的平衡常数为________若往容器中再加入2 mol CO (g),则重新达到平衡时的CO总转化率________20%(填“>”、“<”或“=”)。
CO2(g) +H2 (g),向2 L密闭容器中通入2 mol CO (g)、1 mol H2O (g),2 min后反应达到平衡时,测得CO的物质的量为1.6mol,用H2O (g)表示该反应速率为________此温度下,该反应的平衡常数为________若往容器中再加入2 mol CO (g),则重新达到平衡时的CO总转化率________20%(填“>”、“<”或“=”)。
(2)在一密闭容器中发生反应 2 NO2 2NO+O2 ΔH>0,反应过程中NO2的浓度随时间变化的情况如下图所示。
2NO+O2 ΔH>0,反应过程中NO2的浓度随时间变化的情况如下图所示。
请回答:若曲线A、B分别表示的是该反应在某不同条件下的反应情况,则曲线B此条件可能是________(填“增大压强”、 “减小压强”“升高温度”“降低温度”或“使用催化剂”)。
(3)一定温度下,在密闭容器中N2O5可发生下列反应:
①2N2O5(g)  4NO2(g)+O2(g)
4NO2(g)+O2(g)
②2NO2(g)  2NO(g)+O2(g)
2NO(g)+O2(g)
若达平衡时,c(NO2)=0.6 mol/L,c(O2)=1.3 mol/L,则反应②中NO2的转化率为________
 CO2(g) +H2 (g),向2 L密闭容器中通入2 mol CO (g)、1 mol H2O (g),2 min后反应达到平衡时,测得CO的物质的量为1.6mol,用H2O (g)表示该反应速率为________此温度下,该反应的平衡常数为________若往容器中再加入2 mol CO (g),则重新达到平衡时的CO总转化率________20%(填“>”、“<”或“=”)。
CO2(g) +H2 (g),向2 L密闭容器中通入2 mol CO (g)、1 mol H2O (g),2 min后反应达到平衡时,测得CO的物质的量为1.6mol,用H2O (g)表示该反应速率为________此温度下,该反应的平衡常数为________若往容器中再加入2 mol CO (g),则重新达到平衡时的CO总转化率________20%(填“>”、“<”或“=”)。 2NO+O2 ΔH>0,反应过程中NO2的浓度随时间变化的情况如下图所示。
2NO+O2 ΔH>0,反应过程中NO2的浓度随时间变化的情况如下图所示。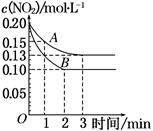
 4NO2(g)+O2(g)
4NO2(g)+O2(g) 2NO(g)+O2(g)
2NO(g)+O2(g)在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)![]() CO(g)+H2O(g)。其化学平衡常数K和温度T的关系如下表:
CO(g)+H2O(g)。其化学平衡常数K和温度T的关系如下表:
| T℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |

回答下列问题:
(1)该反应正向为ΔH 0;若该反应符合下图所示的关系,则在图中,Y轴是指 。
(2)能判断该反应达到化学平衡状态的依据是 (多选扣分)。
a.容器中压强不变 b.混合气体中c(CO)不变
c.v (H2) 正=v (H2O) 逆 d.c(CO2)=c(CO)
(3)某温度下,平衡浓度符合下式: 0.9·c(CO2)·c(H2)=c(CO)·c(H2O),由此可以判断此时的温度为 ℃。其它条件不变,升高温度,原化学平衡向 反应方向移动(填“正”或“逆”),容器内混合气体的密度 (填“增大”、“减小”或“不变”),气体平均相对分子质量 (填“增大”、“减小”或“不变”)。
(4)若在一密闭容器中,将一定量的CO与H2O混合加热到830℃下达到平衡。若反应开始时CO与H2O的浓度分别为0.200 mol/L和0.100 mol/L,平衡时CO的转化率 。
一、二选择题(共63分)
题号
1
2
3
4
5
6
7
8
9
答案
D
B
C
D
D
C
A
A
D
题号
10
11
12
13
14
15
16
17
18
答案
B
AD
B
BC
AB
A
BC
AD
D
19、(共12分) (1)增加反应物接触面积,提高反应速率和原料的利用率(2分)
 SrS+4CO↑(2分) 溶解、过滤(干燥)(2分)。
SrS+4CO↑(2分) 溶解、过滤(干燥)(2分)。
(2)碳酸锶的溶解度小于硫酸锶的溶解度(1分)
水浴(油浴、液体浴)加热、搅拌(各1分,共2分)
(3)方法一(1分)
(4)ABCD(2分,少答一个扣1分)
20、(共10分)(1)(每空1分)
实验编号
T/K
试管内取用液体
实验目的
①
298
食盐水
(Ⅱ)③
(Ⅲ)④(只要与前面③、④对应即可)
②
298
碳酸水
③
308
食盐水
④
298
植物油
(2) AC (2分)
21、(共12分)方案一:(1)取一片pH试纸放在表面皿(或玻璃片)上,用洁净的玻璃棒蘸取待测液滴到试纸上,当试纸颜色变化稳定后立即与标准比色卡对照。(3分)
(2)方案二:(1)赶走溶液中少量氧气,隔绝氧气;不正确(3分) (2)碱,不正确(2分)
(3)
实验方法
观察到的现象
取上述滴有酚酞的NaOH溶液慢慢加水稀释(或取上述NaOH溶液稀释后再加入酚酞溶液) (2分)
出现红色且不褪去 (2分)
22、(共12分) ⑴MgCl2(熔融)  Mg+Cl2↑ ⑵Na2S
Mg+Cl2↑ ⑵Na2S
⑶①CO32-+H2O HCO3-+OH-(或2H2SO4)或 HCO3-+H2O
HCO3-+OH-(或2H2SO4)或 HCO3-+H2O H2CO3 +OH-
H2CO3 +OH-
②降低含硫烟气的温度(或减小含硫烟气的流速)
③2H2SO3+O2=4H++2SO42-或2HSO3-+O2=2H++2SO42-
中和、稀释经氧气氧化后海水中生成的酸(H+),减少污染。(每空2分,共12分)
23、(共10分) ⑴
 ⑵66.7%或66.67% 作图要点:①起点(0,0.75) ②平衡点(8之后,0.25) ③走势逐渐减小(下弧线);(根据等效平衡理论或K计算)
⑵66.7%或66.67% 作图要点:①起点(0,0.75) ②平衡点(8之后,0.25) ③走势逐渐减小(下弧线);(根据等效平衡理论或K计算)
⑶A (因c(CO)/c(CO2)=k,只受温度影响)
⑷②2Fe(OH)3+3ClO-+4OH-=2FeO42-+3Cl-+5H2O (每空2分,共10分)
24、(共11分) (1)保护臭氧层 (2分)
(2)①2KHCO3  K2CO3+CO2↑+H2O(2分)
K2CO3+CO2↑+H2O(2分)
②CO2(g)+3H2(g)=CH3OH(g)+H2O(g);△H=―49.5kJ/mol (3分)
(3)Ba(OH)2 (或NaOH和BaCl2混合溶液)(2分) ; 生成沉淀的质量(2分)
25、(共10分)(1)取代反应、加成反应 (每空1分,共2分)
(2)
(2分,缺少乙酸不给分)
(3)C (2分)
(4)R―CH(CH3)OH + CO → R―CH(CH3)COOH (R代表左侧苯环部分) (2分);
(5) (2分)
(2分)
26、(共10分)
(1) CH3CHBrCH3 (1分); (2) 取代反应 (1分)
⑶ (2分)
(2分)
⑷ (2分)
(2分)
(5)HOCH2CH2CH2CHO、CH3CH(OH)CH2CHO或CH3CH2CH(OH)CHO
(CH3)2C(OH)CHO、HOCH2CH(CH2)CHO (写其中任意2个)(每空2分,共4分)
27、(共10分)⑴1s22s22p63s23p63d104s1 ⑵ 1:5
⑶①A、C ②平面正方型 ③9; 1 (每空2分)
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com