
题目列表(包括答案和解析)
4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g);ΔH=-905 kJ·mol-1
4NO(g)+6H2O(g);ΔH=-905 kJ·mol-1
2H2(g)+O2(g)![]() 2H2O;ΔH=-483.6 kJ·mol-1
2H2O;ΔH=-483.6 kJ·mol-1
则N2(g)+3H2(g)![]() 2NH3(g)的ΔH=________。
2NH3(g)的ΔH=________。
(2)工业上在一定温度下,将一定量的N2和H2通入到体积为
①增大压强②增大反应物的浓度③使用催化剂④降低温度
(3)当化学反应N2(g)+2H2(g) ![]() 2NH3(g)达到平衡后改变某些条件(不改变N2、H2和NH3的用量),反应速率与反应时间的关系如下图,其中表示平衡混合物中NH3的含量最高的一段时间是___________________。当温度为T ℃时,将
2NH3(g)达到平衡后改变某些条件(不改变N2、H2和NH3的用量),反应速率与反应时间的关系如下图,其中表示平衡混合物中NH3的含量最高的一段时间是___________________。当温度为T ℃时,将

(4)合成氨的原料氢气是一种新型的绿色能源,具有广阔的发展前景。现用氢氧燃料电池进行下图所示实验:

①请写出氢氧燃料电池中的电极反应式:
负极:____________________________________________________________;
正极:____________________________________________________________。
②上图装置中,某一铜电极的质量减轻了
下面涉及的是工业生产硝酸铵的过程。
(1)写出NO2和水反应的化学方程式,并标出电子转移的方向和数目。 。
(2)已知:
4NH3(g)+3O2(g)=2N2(g)+6H2O(g) △H= 一1266.8kJ/mol
N2(g)+O2(g)=2NO(g) △H= +180.5 kJ/mol
写出氨高温催化氧化的热化学方程式: ,
氨催化氧化生成NO反应的化学平衡常数表达式K= 。
(3)已知:N2(g)+3H2(g)
 2NH3(g) △H=-92 kJ/mol。为提高氢气的转化率,宜采取的措施有 。(填字母)
2NH3(g) △H=-92 kJ/mol。为提高氢气的转化率,宜采取的措施有 。(填字母)
A.升高温度 B.使用催化剂
C.及时移出氨 D.循环利用和不断补充氮气
(4)在一定温度和压强下,将H2和N2按3:1(体积比)在密闭容器中混合,当该反应达到平衡时,测得平衡混合气中NH3的气体体积分数为17.6%,此时H2的转化率为 。
(5)许多有机物在特定的装置内进行氧化的同时还可产生电能,这种装置即为燃料电池。
例如,乙烯被氧化生成乙醛的化学反应:2CH2=CH2 + O2 →2CH3CHO可设计成燃料电池:
正极为:O2+4H++4e-=2H2O 负极为:
电池工作时,负极附近溶液的pH (填“升高”、“降低”或“不变”)。
 2NH3(g) △H="-92" kJ/mol。为提高氢气的转化率,宜采取的措施有 。(填字母)
2NH3(g) △H="-92" kJ/mol。为提高氢气的转化率,宜采取的措施有 。(填字母)| A.升高温度 | B.使用催化剂 |
| C.及时移出氨 | D.循环利用和不断补充氮气 |

 2NH3(g) △H=-92 kJ/mol。为提高氢气的转化率,宜采取的措施有__________。(填字母)
2NH3(g) △H=-92 kJ/mol。为提高氢气的转化率,宜采取的措施有__________。(填字母) 下图是工业生产硝酸铵的流程。
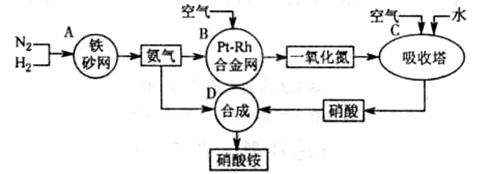
(1)吸收塔C中通入空气的目的是 。A、B、C、D四个容器中的反应,属于氧化还原反应的是 (填字母)。
(2)已知:4NH3(g) + 3O2(g) = 2N2(g) +6H2O(g) △H =-1266.8kJ/mol
N2(g) + O2(g) = 2NO(g) △H = +180.5 kJ/mol
写出氨高温催化氧化的热化学方程式: 。
(3)已知:N2(g) +3H2(g) ![]() 2NH3(g) △H=-92 kJ/mol。为提高氢气的转化率,宜采取的措施有 (填字母)。
2NH3(g) △H=-92 kJ/mol。为提高氢气的转化率,宜采取的措施有 (填字母)。
A.升高温度 B.使用催化剂 C.增大压强 D.循环利用和不断补充氮气
(4)在一定温度和压强下,将H2和N2按3 : 1(体积比)在密闭容器中混合,当该反应达到平衡时,测得平衡混合气中NH3的气体体积分数为17.6%,求此时H2的转化率?(要有完整的计算过程,结果保留三位有效数字)
选择题
题号
1
2
3
4
5
6
7
8
9
答案
B
D
B
C
A
D
A
A
C
题号
10
11
12
13
14
15
16
17
18
答案
BD
B
B
D
A
B
BD
C
BD
19、(12分)(1)碱性(1分) ClO- + H2O  HClO + OH-
(2分)
HClO + OH-
(2分)
(2)氧化性,漂白性,不稳定性(任写两个,每空1分)
(3)CO2等酸性气体、光和热 (2分)
(4)铁钉表面出现铁锈(或红褐色固体) (1分)
(5)铁钉可能未被腐蚀,也可能被腐蚀但无明显现象 (1分)
用试管取出少量浸泡后的溶液,滴加足量的稀硫酸酸化,再滴加几滴KSCN溶液。(3分)
20、(12分)
实验步骤
实验现象
实验结论(步骤2用离子方程式表示)
2IO3-+5HSO3-=== 3H++5SO42-+H2O+I2 (2分)
该食盐中含有碘元素 (1分)
(2)KIO3在加热或高温下易分解而变质。(1分)
(3)5I-+IO3-+6H+ = 3I2+3H2O (2分) 42.8 (2分) 合格 (1分)
(4)I-+ 3H2O-6e- = IO3-+6H+ (2分) 增大。(1分)
21、(10分)(1)NaOH溶液和稀硫酸(2分)
(2)在隔绝空气的条件下,蒸发浓缩、冷却结晶(2分);将滤渣F在空气中灼烧(1分)
(3)由滤液A制得氯化铝溶液不合理,所得氯化铝溶液中含有大量NaCl杂质。(2分)向滤液A中通入足量的CO2生成Al(OH)3沉淀,过滤,向Al(OH)3沉淀中加入盐酸至沉淀溶解(3分)
22、(14分)
(1)使NO全部转化成HNO3(2分);ABC(2分)
(2)4NH3(g)+5O2(g)=4NO(g)+6H2O(g) △H=-905.8kJ/mol (3分)
 (2分)
(2分)
(3)CDE (2分)
(4)30%(或29.9%)(3分)
23、(8分,每空2分)(1)8Fe(OH)2+NO3-+6H2O=8Fe(OH)3+NH3↑+OH-
(2)B,引入的Ca2+对人体无害,易被除去,并且价格便宜。
(3)c中还原剂来源广泛,氧化产物为水,既不污染环境又不会引入对人体有害的铝离子。
24、(12分,每空2分)(1)HgC142- ; HgC12
(2)Hg2++2H2O Hg(OH)2+2H+ ;在硝酸中配制
(3)①Cu+Hg2+
Cu2++Hg ;②1.6×10-47mol/L
25、(9分)(1)C和E(2分)
(2)  (2分)
(2分)
氧化反应(1分)
(4)C(1分)
|