
题目列表(包括答案和解析)
 A、B、C、D、E、F六种元素分属三个短周期,且原子序数依次增大,A的原子在周期表中半 径最小,A、D伺主族,可形成离子化合物DA;C、F同主族,可形成FC2,FC3两种分子B,D,E 三者的最高价氧化物对应的水化物两两之间均可反应生成可溶性盐和水,所得盐中均含C元 素.请填写下列空白:
A、B、C、D、E、F六种元素分属三个短周期,且原子序数依次增大,A的原子在周期表中半 径最小,A、D伺主族,可形成离子化合物DA;C、F同主族,可形成FC2,FC3两种分子B,D,E 三者的最高价氧化物对应的水化物两两之间均可反应生成可溶性盐和水,所得盐中均含C元 素.请填写下列空白:A 、B 、C 、D 、E 、F、G为原子序数依次增大的元素,其中前六种属于短周期元素。已知B 、C 、F 三种原子的最外层共有11 个电子,且这三种元素的最高价氧化物对应的水化物之间两两皆能反应并且生成盐和水。请完成下列问题:
(1)只根据以上条件一定能判断出的元素的及符合条件的离子的符号填写在下表空格处
| 编号 | A | B | C | D | E | F | G | 半径最小的离子 |
| 符号 |
 (2)写出B、C 的最高价氧化物对应的水化物间反
(2)写出B、C 的最高价氧化物对应的水化物间反
应的离子方程式____________
(3)己知D的单质在F单质中燃烧可生成X、Y两
种化合物并产生白色烟雾,写出X、Y中各原子
最外层均满足8 电子结构的分子的电子式___。
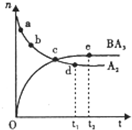
D、F的单质反应过程和能量关系如图所示(图
中的△H表示生成1mol产物的数据),写出指定
条件下两种单质作用生成Y时的热化学方程式
_______________________。
(4) G的单质是目前用途最广泛的一种金属材料,但在使用中受环境影响易被腐蚀,试写出发生腐蚀时的电极反应式_________________________________________。
(5)A与E能形成两种常见的化合物,这两种化合物中属于非极性分子的物质化学式_______
(10分)A、B、C、D、E、F、G、H、IJ分别表示中学化学中常见的一种物质,它们之间相互关系如下图所示(部分反应物、生成物没有列出),
且已知G为主族元素的固态氧化物,A、B、C、D、E、F六种物质中均含同一种元素。
请填写下列空白:
(1)A、B、C、D、E、F六种物质中所含同一种元素在周期表中位置第_______周期、第_______族 ;
(2)写出反应①的化学方程式___________ _________;
(3)写出反应④的离子方程式_____________ _______;
(4)写出反应③的电极方程式:
阳极:_______________ _____ 阴极:____________ __________
(5)从能量变化的角度看,①②③反应中属于△H<0的反应是___________。(填序号)
(10分)A、B、C、D、E、F、G、H、IJ分别表示中学化学中常见的一种物质,它们之间相互关系如下图所示(部分反应物、生成物没有列出),
且已知G为主族元素的固态氧化物,A、B、C、D、E、F六种物质中均含同一种元素。
请填写下列空白:
(1)A、B、C、D、E、F六种物质中所含同一种元素在周期表中位置第_______周期、第_______族;
(2)写出反应①的化学方程式___________ _________;
(3)写出反应④的离子方程式_____________ _______;
(4)写出反应③的电极方程式:
阳极:_______________ _____ 阴极:____________ __________
(5)从能量变化的角度看,①②③反应中属于△H<0的反应是___________。(填序号)
(10分)A、B、C、D、E、F、G、H、IJ分别表示中学化学中常见的一种物质,它们之间相互关系如下图所示(部分反应物、生成物没有列出),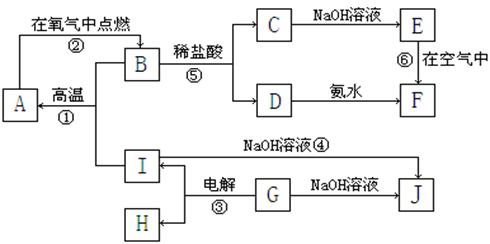
且已知G为主族元素的固态氧化物,A、B、C、D、E、F六种物质中均含同一种元素。
请填写下列空白:
(1)A、B、C、D、E、F六种物质中所含同一种元素在周期表中位置第_______周期、第_______族 ;
(2)写出反应①的化学方程式___________ _________;
(3)写出反应④的离子方程式_____________ _______;
(4)写出反应③的电极方程式:
阳极:_______________ _____ 阴极:____________ __________
(5)从能量变化的角度看,①②③反应中属于△H<0的反应是___________。(填序号)
第Ⅰ卷 (选择题共48分)
一、单项选择题:(本题包括8小题,每题3分,共24分。每小题只有一个选项符合题意)
1、C 2、B 3、B 4、A 5、C 6、A 7、D 8、D
二、不定项选择题(本题包括6小题,每小题4分,共24分。每小题只有一个或两个选项符合题意。若正确答案只包括一个选项,多选时,该题为0分;若正确答案包括两个选项,只选一个且正确的得2分,选两个且都正确的得满分,但只要选错一个,该小题就为0分)
9、D 10、BC 11、AD 12、A 13、C 14、B
第Ⅱ卷 (选择题共72分)
三、(本题包括1小题,共10分)
15.(10分) 每空2分
I AB
II(1)SiO2 (2)保持较大的C2O42-离子浓度,使Ca2+沉淀完全。
(3)降低CaC2O4在水中的溶解度,减少沉淀的损失,降低实验误差。
(4) 或
或 %
%
四、(本题包括2小题,共18分)
16.(8分)
(1)第三周期第VIIA族 (2分)
(2) 2SO2(g)+O2(g) 2SO3(g) △H=-196.6 kJ?mol-1 (2分)
2SO3(g) △H=-196.6 kJ?mol-1 (2分)
 (3)Al3++3AlO2-+6H2O=4Al(OH)3↓ (2分) (4) H2O (2分)错误!链接无效。
(3)Al3++3AlO2-+6H2O=4Al(OH)3↓ (2分) (4) H2O (2分)错误!链接无效。
17.(10分)
(1) (2分)
(2)8Al+3Fe3O4 4Al2O3+9Fe (2分)
4Al2O3+9Fe (2分)
(3)2Al+2OH-+2H2O=2AlO2-+3H2↑(2分)
(4)阳极:6O2--12e-=3O2↑;阴极:4Al3++12e-=4Al (每空1分)
(5)③ (2分)
五、(本题包括1小题,共10分)
18.(10分)(每空2分)
 (1) ③⑤
(1) ③⑤
(2)
(3) ①如2Na+2H2O=2Na++2OH-+H2↑;
②如CH3COOH+NH3×H2O=CH3COO-+NH4++H2O;
③如Al3++3H2O Al(OH)3+3H+;
Al(OH)3+3H+;
六、(本题包括1小题,共12分)
19.( 12分)每空2分
12分)每空2分
⑴过滤 低温蒸发结晶
⑵(如图或其他能防止氨气倒吸的装置)
⑶ 冷凝管
⑷ ① 2CaSO4
2CaO+2SO2↑+O2↑
2CaSO4
2CaO+2SO2↑+O2↑
② 95.6%
七、(本题包括1小题,共8分)
20.(8分)
解:(1)6Fe2++ClO3-+6H+=6Fe3++Cl-+3H2O (2分)
(2)n(Fe)=×2=0.035 mol
n(SO42-)==0.045 mol
n(OH-)=3×n(Fe3+)-2×n(SO42-)=3×0.035 mol-2×0.045 mol=0.015 mol (2分)
盐基度=×100%= ×100%=14.29% (2分)
(3)n(H2O)=
=0.054 mol
化学式: Fe35(OH)15(SO4)45?54H2O (2分)
八、(本题包括1小题,共14分)
21.(14分)
(1)相同 b (每空1分)
(2)B(2分)
(3)I.3d24S2 (2分) II.[TiCl(H2O)5]Cl2?H2O(2分)
(4)I.KO2 kJ?mol-1 (每空2分,共
射阳中学2009届高三上学期第二次月考
化 学 答 题 纸
三、(本题包括1小题,共10分)
15.(10分)
I
II(1)
(2)
(3)
(4)
四、(本题包括2小题,共18分)
16.(8分)
(1)
(2)
(3)
(4)
17.(10分)
(1)
(2)
(3)
(4)阳极 阴极
五、(本题包括1小题,共10分)
18.(10分)
(1)
(2) 
(3) 请在下列表格中用相应的“离子方程式”否定这些观点。
①所有的离子方程式均可以表示一类反应
②酸碱中和反应均可表示为:H++OH-=H2O
③离子方程式中凡是难溶性酸碱盐(产物)均要用“↓”
六、(本题包括1小题,共12分)
19.(12分)
(1)
(2) 
(3)
(4)①
②
七、(本题包括1小题,共8分)
20.(8分)
(1)
(2)
(3)
八、(本题包括1小题,共14分)
21.(14分)
(1)
(2)
(3)I II
(4) I II
 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com