
题目列表(包括答案和解析)
| ||

| 氢氧化物开始沉淀时的pH | 氢氧化物沉淀完全时的pH | |
| Fe3+ | 2.7 | 3.7 |
| Fe2+ | 7.6 | 9.6 |
| Cu2+ | 4.7 | 6.7 |
“熵”可看作是“体系混乱度”,它的符号是“S”。下列变化中,ΔS<0(“混乱度”减小)的肯定是
A.3Fe(s)+4H2O(g)→Fe3O4(s)+4H2(g)
B.2NO2(g)→N2O4(l)
C.2IBr(l)→I2(s)+Br2(g)
D.(NH4)2CO3(s)→2NH3(g)+CO2(g)+H2O(g)
捕碳技术(主要指捕获CO2)在降低温室气体排放中具有重要的作用。目前NH3和(NH4)2CO3已经被用作工业捕碳剂,它们与CO2可发生如下可逆反应:
反应Ⅰ:2NH3 (l)+ H2O (l)+ CO2 (g) (NH4)2CO3 (aq)??????????? △H1
(NH4)2CO3 (aq)??????????? △H1
反应Ⅱ:NH3 (l)+ H2O (l)+ CO2 (g) NH4HCO3 (aq)????????????? △H2
NH4HCO3 (aq)????????????? △H2
反应Ⅲ:(NH4)2CO3 (aq) + H2O (l)+ CO2 (g) 2NH4HCO3 (aq)???? △H3
2NH4HCO3 (aq)???? △H3
请回答下列问题:
(1)△H1与△H2、△H3之间的关系是:△H3=?????????????????? 。
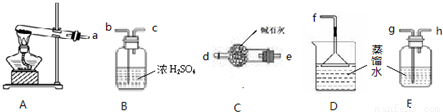
(2)为研究温度对(NH4)2CO3捕获CO2气体效率的影响,在温度为T1 、T2、T3、T4、T5的条件下,将等体积等浓度的(NH4)2CO3溶液分别置于等体积的密闭容器中,并充入等量的CO2气体,经过相同时间测得容器中CO2气体的浓度,得趋势图(下图1)。则:
①△H3______0? (填“>”、“=”或“<”)。
②温度高于T3,不利于CO2的捕获,原因是?????????????????????????????????????? 。
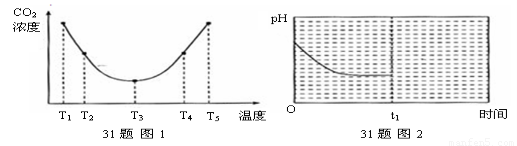
③反应Ⅲ在温度为K1时,溶液pH随时间变化的趋势曲线如下图2所示。当时间到达t1时,将该反应体系温度迅速上升到K2,并维持该温度。请在该图中画出t1时刻后溶液的pH变化趋势曲线。
(3)利用反应Ⅲ捕获CO2,在(NH4)2CO3初始浓度和体积确定的情况下,提高CO2吸收量的措施有(写出1个)??????????????????????????? 。
(4)下列物质中也可能作为CO2捕获剂的是???????? 。
A.NH4Cl?????? B.Na2CO3?????? C.HOCH2CH2OH?????? D.HOCH2CH2NH2
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com