
题目列表(包括答案和解析)

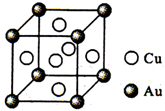 催化剂中毒是微量杂质和催化剂活性中心的某种化学成分作用,形成没有活性的物质.CO会使合成氨的催化剂(还原铁)中毒,CO易与Fe发生反应Fe+5CO═Fe(CO)5.除去CO的化学反应方程式(HAc表示醋酸):Cu(NH3)2Ac+CO+NH3═Cu(NH3)3(CO)Ac.
催化剂中毒是微量杂质和催化剂活性中心的某种化学成分作用,形成没有活性的物质.CO会使合成氨的催化剂(还原铁)中毒,CO易与Fe发生反应Fe+5CO═Fe(CO)5.除去CO的化学反应方程式(HAc表示醋酸):Cu(NH3)2Ac+CO+NH3═Cu(NH3)3(CO)Ac.![]()
填空或完成下列问题:
(1)若A为RCH=CHR′,B为RCH=CHR,试写出上述化学反应方程式:___________
__________________________________________。
(2)对上述反应有人提出两种反应机理(竖线表示断键位置)。
若机理a是: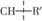
则机理b是:![]()
(6分)催化剂的研究使许多物质出现了新的化学反应。例如烯烃A在苯中用一种特殊催化剂处理时,生成两种新的烯烃:烯烃B、烯烃C,用反应式可表示为如下:2AB+C
(1)若A为R1CH=CHR2,B为R1CH=CHR1,试写出上述反应的化学方程式:
(2)对上述反应提出两种可能的反应机理(虚线表示断键位置):
机理a:R1CH=CH——R2
R1——CH=CHR2 B+C
你认为机理b是(用虚线标明具体的断键位置)
R1——CH=CH——R2 + R1——CH=CH——R2 B+C
(3)结合你所学,证明是机理a还是机理b,你采用的方法是:
催化剂在生产和科技领域起到重大作用。为比较Fe3+和Cu2+对H2O2分解的催化效果,某化学研究小组的同学分别设计了如图甲、乙所示的实验。请回答相关问题: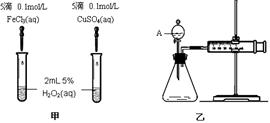
(1)定性分析:如图甲可通过观察 ,定性比较得出结论。同学乙观察甲中两支试管产生气泡的快慢,由此得出Fe3+和Cu2+对H2O2分解的催化效果,其结论__________(填“合理”或“不合理”),理由是____________________________。
(2)定量分析:如图乙所示,实验时均以生成40 mL气体为准,其它可能影响实验的因素均已忽略。实验中需要测量的数据是 。
(3)加入0.10 mol MnO2粉末于50 mL H2O2溶液中,在标准状况下放出气体的体积和时间的关系如下图所示。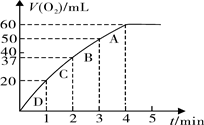
①实验时放出气体的总体积是 mL。
②放出1/3气体所需时间为 min。
③计算H2O2的初始物质的量浓度______。(请保留两位有效数字)
④A、B、C、D各点反应速率快慢的顺序为_____>____>___> ____。
⑤解释反应速率变化的原因 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com