
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
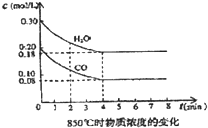 дквЛЬхЛ§ЮЊ10LЕФШнЦїжаЃЌЭЈШывЛЖЈСПЕФCOКЭH2OЃЌдк85ЁцЪБЗЂЩњШчЯТЗДгІЃКCOЃЈgЃЉ+H2OЃЈgЃЉ?CO2ЃЈgЃЉ+H2ЃЈgЃЉЁїH=-Q kJ/mol COКЭH2OХЈЖШБфЛЏШчЭМЃЌдђ
дквЛЬхЛ§ЮЊ10LЕФШнЦїжаЃЌЭЈШывЛЖЈСПЕФCOКЭH2OЃЌдк85ЁцЪБЗЂЩњШчЯТЗДгІЃКCOЃЈgЃЉ+H2OЃЈgЃЉ?CO2ЃЈgЃЉ+H2ЃЈgЃЉЁїH=-Q kJ/mol COКЭH2OХЈЖШБфЛЏШчЭМЃЌдђ| ЪБМф | CO | H2O | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | C1 | C2 | C3 | C3 |
| 4 | C1 | C2 | C3 | C3 |
| 5 | 0.116 | 0.216 | 0.084 | |
| 6 | 0.096 | 0.266 | 0.104 |
дквЛЬхЛ§ЮЊ10LЕФШнЦїжаЃЌЭЈШывЛЖЈСПЕФCOКЭH2OЃЌдк850ЁцЪБЗЂЩњШчЯТЗДгІЃК
CO(g) +H2O(g)  CO2(g) +H2 (g) ЁїH<0ЁЃ
CO2(g) +H2 (g) ЁїH<0ЁЃ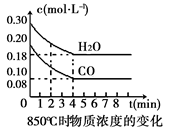
ЃЈ1ЃЉCOКЭH2OХЈЖШБфЛЏШчЩЯЭМЃЌдђдкИУЮТЖШЯТЃЌИУЗДгІЕФЦНКтГЃЪ§K= ЁЃ
0ЁЋ4minЕФЦНОљЗДгІЫйТЪv(CO)ЃН_____molЁЄL-1ЁЄmin-1ЁЃШєНЕЕЭЮТЖШЃЌИУЗДгІЕФKжЕНЋ ЃЌИУЗДгІЕФЛЏбЇЗДгІЫйТЪНЋ ЃЈЬюЁАдіДѓЁБЁАМѕаЁЁБЛђЁАВЛБфЁБЃЉЁЃ
ЃЈ2ЃЉдкЯрЭЌШнЦїжаЗЂЩњЩЯЪіЗДгІЃЌЕБЮТЖШИпгк850ЁцЪБЃЌ
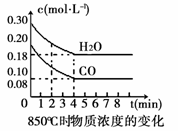
ШнЦїФкИїЮяжЪЕФХЈЖШБфЛЏШчЯТБэЁЃ
| ЪБМф(min) | CO | H2O | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | c1 | c2 | c3 | c3 |
| 4 | c1 | c2 | c3 | c3 |
| 5 | 0.116 | 0.216 | 0.084 | |
| 6 | 0.096 | 0.266 | 0.104 | |
дквЛЬхЛ§ЮЊ10LЕФШнЦїжаЃЌЭЈШывЛЖЈСПЕФCOКЭH2OЃЌдк850ЁцЪБЗЂЩњШчЯТЗДгІЃК
CO(g) +H2O(g)  CO2(g) +H2
(g) ЁїH<0ЁЃ
CO2(g) +H2
(g) ЁїH<0ЁЃ
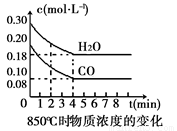
ЃЈ1ЃЉCOКЭH2OХЈЖШБфЛЏШчЩЯЭМЃЌдђдкИУЮТЖШЯТЃЌИУЗДгІЕФЦНКтГЃЪ§K= ЁЃ
0ЁЋ4minЕФЦНОљЗДгІЫйТЪv(CO)ЃН_____molЁЄL-1ЁЄmin-1ЁЃШєНЕЕЭЮТЖШЃЌИУЗДгІЕФKжЕНЋ ЃЌИУЗДгІЕФЛЏбЇЗДгІЫйТЪНЋ ЃЈЬюЁАдіДѓЁБЁАМѕаЁЁБЛђЁАВЛБфЁБЃЉЁЃ
ЃЈ2ЃЉдкЯрЭЌШнЦїжаЗЂЩњЩЯЪіЗДгІЃЌЕБЮТЖШИпгк850ЁцЪБЃЌ
ШнЦїФкИїЮяжЪЕФХЈЖШБфЛЏШчЯТБэЁЃ
|
ЪБМф(min) |
CO |
H2O |
CO2 |
H2 |
|
0 |
0.200 |
0.300 |
0 |
0 |
|
2 |
0.138 |
0.238 |
0.062 |
0.062 |
|
3 |
c1 |
c2 |
c3 |
c3 |
|
4 |
c1 |
c2 |
c3 |
c3 |
|
5 |
0.116 |
0.216 |
0.084 |
|
|
6 |
0.096 |
0.266 |
0.104 |
|
ЂйБэжа3minЁЋ4minжЎМфЗДгІДІгк_________зДЬЌЃЛ c 1Ъ§жЕ_________0.08 molЁЄL-1 (ЬюДѓгкЁЂаЁгкЛђЕШгк)ЁЃ
ЂкЗДгІдк4minЁЋ5minМфЃЌЦНКтЯђФцЗНЯђвЦЖЏЃЌПЩФмЕФдвђЪЧ_________
aЃЎдіМгЫЎеєЦј bЃЎНЕЕЭЮТЖШ
cЃЎЪЙгУДпЛЏМС dЃЎдіМгЧтЦјХЈЖШ
ЃЈ3ЃЉдкЯрЭЌЮТЖШЯТЃЈ850ЁцЃЉЃЌШєЦ№ЪМЪБcЃЈCOЃЉ=1molЁЄL-1ЃЌcЃЈH2OЃЉ=2molЁЄL-1ЃЌЗДгІНјаавЛЖЮЪБМфКѓЃЌВтЕУH2ЕФХЈЖШЮЊ0.5 molЁЄL-1ЃЌдђДЫЪБИУЗДгІЪЧЗёДяЕНЦНКтзДЬЌ ЃЈЬюЁАЪЧЁБгыЁАЗёЁБЃЉЃЌДЫЪБvЃЈе§ЃЉ vЃЈФцЃЉЃЈЬюЁАДѓгкЁБЁАаЁгкЁБЛђЁАЕШгкЁБЃЉЃЌФуХаЖЯЕФвРОнЪЧ ЁЃ
| ЪБМф | CO | H2O | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | C1 | C2 | C3 | C3 |
| 4 | C1 | C2 | C3 | C3 |
| 5 | 0.116 | 0.216 | 0.084 | |
| 6 | 0.096 | 0.266 | 0.104 |
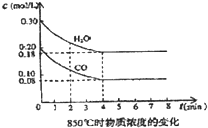
дквЛЬхЛ§ЮЊ10LЕФШнЦїжаЃЌЭЈШывЛЖЈСПЕФCOКЭH2OЃЌдк850ЁцЪБЗЂЩњШчЯТЗДгІЃК
 CO(g) +H2O(g)
CO(g) +H2O(g) ![]() CO2(g) +H2 (g) ЁїH<0ЁЃ
CO2(g) +H2 (g) ЁїH<0ЁЃ
ЃЈ1ЃЉCOКЭH2OХЈЖШБфЛЏШчгвЭМЃЌдђдкИУЮТЖШЯТЃЌИУЗДгІ
ЕФЦНКтГЃЪ§K= ЁЃ
0ЁЋ4minЕФЦНОљЗДгІЫйТЪv(CO)ЃН_____molЁЄL-1ЁЄmin-1ЁЃШєНЕЕЭЮТЖШЃЌИУЗДгІЕФKжЕНЋ ЃЌИУЗДгІЕФЛЏбЇЗДгІЫйТЪНЋ ЃЈЬюЁАдіДѓЁБЁАМѕаЁЁБЛђЁАВЛБфЁБЃЉЁЃ
ЃЈ2ЃЉдкЯрЭЌШнЦїжаЗЂЩњЩЯЪіЗДгІЃЌЕБЮТЖШИпгк850ЁцЪБЃЌ
ШнЦїФкИїЮяжЪЕФХЈЖШБфЛЏШчЯТБэЁЃ
| ЪБМф(min) | CO | H2O | CO2 | H2 |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | c1 | c2 | c3 | c3 |
| 4 | c1 | c2 | c3 | c3 |
| 5 | 0.116 | 0.216 | 0.084 | |
| 6 | 0.096 | 0.266 | 0.104 |
ЂйБэжа3minЁЋ4minжЎМфЗДгІДІгк_________зДЬЌЃЛ c 1Ъ§жЕ_________0.08 molЁЄL-1 (ЬюДѓгкЁЂаЁгкЛђЕШгк)ЁЃ
ЂкЗДгІдк4minЁЋ5minМфЃЌЦНКтЯђФцЗНЯђвЦЖЏЃЌПЩФмЕФдвђЪЧ_________
aЃЎдіМгЫЎеєЦј bЃЎНЕЕЭЮТЖШ
cЃЎЪЙгУДпЛЏМС dЃЎдіМгЧтЦјХЈЖШ
ЃЈ3ЃЉдкЯрЭЌЮТЖШЯТЃЈ850ЁцЃЉЃЌШєЦ№ЪМЪБcЃЈCOЃЉ=1molЁЄL-1ЃЌcЃЈH2OЃЉ=2molЁЄL-1ЃЌЗДгІНјаавЛЖЮЪБМфКѓЃЌВтЕУH2ЕФХЈЖШЮЊ0.5 molЁЄL-1ЃЌдђДЫЪБИУЗДгІЪЧЗёДяЕНЦНКтзДЬЌ ЃЈЬюЁАЪЧЁБгыЁАЗёЁБЃЉЃЌДЫЪБvЃЈе§ЃЉ vЃЈФцЃЉЃЈЬюЁАДѓгкЁБЁАаЁгкЁБЛђЁАЕШгкЁБЃЉЃЌФуХаЖЯЕФвРОнЪЧ ЁЃ
1
2
3
4
5
6
7
8
9
C
C
B
D
B
D
B
C
D
10
11
12
13
14
15
16
17
18
D
C
D
B
B
D
B
B
A
19
20
21
22
23
24
25
ЈDЈD
ЈDЈD
A
B
D
B
C
C
A
26ЁЂЃЈ14ЗжЃЉ
ЂХЕчНтГи ЃЌдЕчГи ЃЈ2ЗжЃЌИї1ЗжЃЉ
2H2O+2CuSO4 = 2Cu+O2Ёќ+2H2SO4 ЃЈ5ЗжЃЌЕквЛПе1ЗжЃЌЦфЫќИї2ЗжЃЉ
ЃЈ3ЃЉ0.02 ЃЌдіМг ЃЌ0.63 ЃЌ 1 ЁЃЃЈ7ЗжЃЌЕкЖўПе1ЗжЃЌЦфЫќИї2ЗжЃЉ
27ЁЂЃЈ10ЗжЃЉ
ЃЈ1ЃЉFe3+ЃЋ3H2O FeЃЈOHЃЉ3ЃЋ3H+ ЃЌНЋFeCl3ЯШШмгкбЮЫсЃЌШЛКѓдйМгЫЎЯЁЪЭ ЁЃ
FeЃЈOHЃЉ3ЃЋ3H+ ЃЌНЋFeCl3ЯШШмгкбЮЫсЃЌШЛКѓдйМгЫЎЯЁЪЭ ЁЃ
ЬМЫсИЦЯћКФСЫH+ЃЌЪЙFe3+ЫЎНтГЬЖШдіДѓЃЌаЮГЩFe(OH)3ГСЕэЁЃЃЈ6ЗжЃЌИї2ЗжЃЉ
ЃЈ2ЃЉАзЩЋаќзЧвКж№НЅзЊБфЮЊКкЩЋаќзЧвКЁЃ2AgClЃЈsЃЉЃЋS2ЈDЃНAg2SЃЈsЃЉЃЋ2ClЈDЁЃЃЈ4ЗжЃЌИї2ЗжЃЉ
28ЃЎ(9Зж)
(1)діДѓ ЃЈ2ЗжЃЉ(2) 15ЈD20minЁЂ25ЈD30min ЁЃЃЈ2ЗжЃЉ
(3) діДѓбѕЦјЕФХЈЖШЃЌaЁЂbЁЃЃЈ3ЗжЃЌЕкЖўПе2ЗжЃЌЖрбЁВЛИјЗжЃЉ
ЃЈ4ЃЉВЛ ЁЂЯђзѓЁЃЃЈ2ЗжЃЌИї1ЗжЃЉ
29ЃЎЃЈ11ЗжЃЉ
ЃЈ1ЃЉЂйзЊвЦЃЌЖЈШн ЂкЩеБЃЈЛђБэУцУѓЃЉЁЂвЉГзЁЃЃЈ4ЗжЃЌИї1ЗжЃЉ
ЃЈ2ЃЉЂйШмвКДгЮоЩЋЧЁКУБфЮЊКьЩЋ,ЧвАыЗжжгФкВЛЭЪШЅЁЃ
Ђк0.11mol?L-1 Ђл Бћ Ђм D ЃЈ7ЗжЃЌЕкШ§Пе1ЗжЃЌЦфЫќИї2ЗжЃЉ
30ЃЎЃЈ6ЗжЃЉЃЈ1ЃЉ0.04 mol?L-1?min-1ЁЂ80% ЃЈ2ЃЉ16%
ЃЈЫуГіЗДгІЫйТЪЧвЙ§ГЬе§ШЗЕФИј4ЗжЃЌзЊЛЏТЪКЭЬхЛ§ЗжЪ§ИїИј1ЗжЃЉ
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com