
题目列表(包括答案和解析)
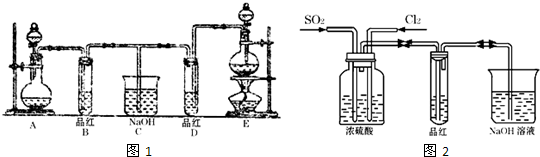
| ||
| ||
分解产物与浓盐酸在加热时涉及下列反应:
①![]() +16H+10Cl-====Mn2++5C12+8H2O
+16H+10Cl-====Mn2++5C12+8H2O
②□![]() +□Cl-+□H+====□Mn2++□Cl2+□H2O
+□Cl-+□H+====□Mn2++□Cl2+□H2O
③MnO2+4H++2Cl-![]() Mn2++Cl2
Mn2++Cl2![]() +2H2O
+2H2O
(1)试配平反应②的离子方程式,将化学计量数填入上述对应的方框内(如果是1,也必须填写)。
(2)a+b=_________(用含x的代数式表示)。
(3)当x=__________时,(a+b)取最小值,且最小值为_________。
(4)当a+b=0.09mol时,0.04mol KMnO4按上述操作反应后,将所得溶液稀释至1 L。该稀释后的溶液中c(H+)=_________mol·L-1。
| ||
| ||
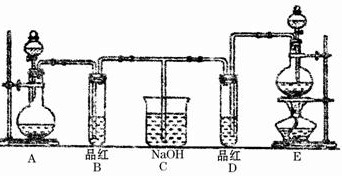
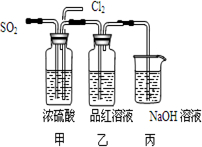
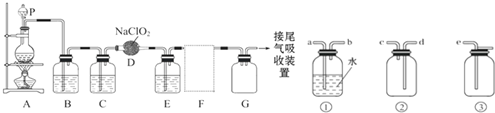
| ||
| ||

| ||
| ||
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com