
题目列表(包括答案和解析)
瑞典皇家科学院2007年10月10日宣布,将本年度诺贝尔化学奖授予德国马普学会弗里茨一哈勃研究所的格哈德?埃特尔教授,以表彰他在固体表面化学过程研究领域做出开拓性成就。格哈德?埃特尔的重要贡献之一是对哈伯一博施法合氨反应催化机理的研究。格哈德?埃特尔建立的某温度下合成氨反应机理的各步反应的能量变化如图所示,图中的能量单位为kJ?mol-1。(注:图中“吸表示在催化剂表面的吸附)
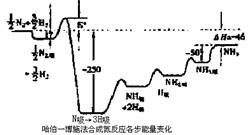
请回答下列问题:
(1)在合成氨反应中,决定反应速率的最主要的步骤是 (填字母)
A.氮分子解离为氢原子
B.氮原子的解离吸附
C.氢分子解离为氢原子
D.氨的解离吸附
(2)合成氨反应的机理为(用化学方程式表示)
① ;
②N2 ![]() N2吸
N2吸 ![]() 2N吸;
2N吸;
③ ;
④NH吸+H吸 ![]() NH3吸
NH3吸
⑤NH2吸+H吸![]() NH3吸
NH3吸 ![]() NH3
NH3
(3)某温度下合成氨反应的热化学方程式为 ;
(4)某温度下,合成氨反应Ke=3.0×103(mol?L-1)-2,该温度下,在体积恒定为10L的四个密闭容器中分别充入;(A)10mol、30mol H2和20molNH3(B)10molN2和30molH2(C)20molN2和60molH2(D)10molN2和28molH2(E)0.1molN2、0.3molH2和20MolNH3,则反应达到平衡后,N2的转化率最大的是 (填字母)。
(5)合成氨工业生产中所用的α―Fe催化剂的主要成分是FeO、Fe2O3,当催化剂中Fe3+与Fe3+的物质的量之比为1:2时,其催化剂活性最高,以Fe2O3为原料制备上述催化剂,可向其中加入适量炭粉。发生如下反应:2Fe2O3+C=4FeO+CO2,为制得该种活性最高的催化剂,应向480gFe2O3粉末加入炭粉的质量为 g.
第Ⅰ卷(选择题,共63分)
一二.选择题。(3’×9+4’×9)
题号
1
2
3
4
5
6
7
8
9
答案
A
C
D
B
D
C
B
B
C
题号
10
11
12
13
14
15
16
17
18
答案
D
AC
B
AC
BC
B
C
CD
A
第Ⅱ卷(非选择题,共83分)
三.(本题包括3小题,共32分)
19.(9分)(1)双氧水(1分),Na2O2(其它合理答案也可)(1分)(2)a(1分)
(3)吸收多余氯气,防止污染空气。(2分)
(4)洗气瓶.安全瓶(其它合理答案也可)(各2分,共4分)
20.(11分)(1)固体完全溶解,溶液呈血红色(2分) (2)ABC(3分)
(3) Fe2O3+6H+===2Fe3++3H2O Cu2O+2H+===Cu+Cu2++H2O 2Fe3++Cu===2Fe2++Cu2+(每个离子方程式2分,共6分)
21.(12分)(1)B.锌粒(1分) C.水(1分) D.浓硫酸(1分)
(2)检查气密性(1分) 将G弯管浸没在盛有水的烧杯中,关闭分液漏斗活塞,温热烧瓶B,观察G管口,若有气泡逸出,停止加热后,G管倒吸形成一段水柱,说明装置的气密性良好(2分)(3)先从A瓶逐滴滴加液体(1分) 检验H2的纯度(1分)
(4)氢气(1分) 在G管出口处点燃(1分)
(5)
 或
或  (2分)
(2分)
四.(本题包括3小题,共31分)
22.(8分)(1)14HNO3+3Cu2O = 6Cu(NO3)2+2NO↑+7H2O。(2分) (2)酸性;氧化性(2分) (3)0.6 mol(2分) (4)使用了较浓的硝酸,产物中有部分二氧化氮生成。(2分)
 23.(14分)(1)2Na+2H2O=2Na++2OH-+H2↑ (2分) (2)酸(1分) NH4++H2O
23.(14分)(1)2Na+2H2O=2Na++2OH-+H2↑ (2分) (2)酸(1分) NH4++H2O NH3?H2O+H+ (2分)
(3)CH4(g)+2O2(g)=CO2(g)+2H2O(l)ΔH=-890.3KJ/mol (2分)
(4)I.NO2(2分)Ⅱ.b (1分) Ⅲ.0.8(或0.8mol/L) (2分) Ⅳ.增大NO2的浓度(合理均可)(2分)
NH3?H2O+H+ (2分)
(3)CH4(g)+2O2(g)=CO2(g)+2H2O(l)ΔH=-890.3KJ/mol (2分)
(4)I.NO2(2分)Ⅱ.b (1分) Ⅲ.0.8(或0.8mol/L) (2分) Ⅳ.增大NO2的浓度(合理均可)(2分)
24.(9分)(1)
(2)氧化.2Cl-+2e-=Cl2↑;
CaCl2+2H2O=Ca(OH)2+Cl2↑+H2↑;
(3)①F极放出黄绿色气体,E极放出无色气体;
②E极附近溶液变为红色;
③溶液变浑浊
五.(本题包括1小题,共10分)
25.(10分)29.(1) E F(2分)(2) ①③(2分)
 (3)A.CH3CH=CH2 ,
I.
(3)A.CH3CH=CH2 ,
I. 。(4分)
。(4分)
(4)(2分)
六.(本题包括2小题,共10分,任意选做一题,如果两道题都做,则按第26题给分)
26.⑴酯基.碳碳双键.苯环(3分)⑵加成(加聚)(2分)⑶(3分)
|