
ĖâÄŋÁÐąí(°üĀĻīð°ļšÍ―âÎö)
 ĢĻ1ĢĐëÂĢĻN2H4ĢĐÓÖģÆÁŠ°ąĢŽĘĮŌŧÖÖŋÉČžÐÔĩÄŌšĖåĢŽŋÉÓÃŨũŧðžýČžÁÏĢŪŌŅÖŠÔÚ101kPaĘąĢŽ32.0gN2H4ÔÚŅõÆøÖÐÍęČŦČžÉÕÉúģÉĩŠÆøĢŽ·ÅģöČČÁŋ624kJĢĻ25ĄæĘąĢĐĢŽN2H4ÍęČŦČžÉÕ·īÓĶĩÄČČŧŊŅ§·―ģĖĘ―ĘĮ
ĢĻ1ĢĐëÂĢĻN2H4ĢĐÓÖģÆÁŠ°ąĢŽĘĮŌŧÖÖŋÉČžÐÔĩÄŌšĖåĢŽŋÉÓÃŨũŧðžýČžÁÏĢŪŌŅÖŠÔÚ101kPaĘąĢŽ32.0gN2H4ÔÚŅõÆøÖÐÍęČŦČžÉÕÉúģÉĩŠÆøĢŽ·ÅģöČČÁŋ624kJĢĻ25ĄæĘąĢĐĢŽN2H4ÍęČŦČžÉÕ·īÓĶĩÄČČŧŊŅ§·―ģĖĘ―ĘĮ
| ||
| ||
ĢĻ12·ÖĢĐĢĻ1ĢĐëÂĢĻN2H4ĢĐÓÖģÆÁŠ°ąĢŽĘĮŌŧÖÖŋÉČžÐÔĩÄŌšĖåĢŽŋÉÓÃŨũŧðžýČžÁÏĄĢŌŅÖŠÔÚ101kPaĘąĢŽ32.0gN2H4ÔÚŅõÆøÖÐÍęČŦČžÉÕÉúģÉĩŠÆøĢŽ·ÅģöČČÁŋ624kJĢĻ25ĄæĘąĢĐĢŽN2H4ÍęČŦČžÉÕ·īÓĶĩÄČČŧŊ·―ģĖĘ―ĘĮ ĄĢ
ĢĻ2ĢĐëÂŌŧŋÕÆøČžÁÏĩįģØĘĮŌŧÖÖžîÐÔČžÁÏĩįģØĢŽĩį―âÖĘČÜŌšĘĮ20%ĄŠ30%ĩÄ KOHČÜŌšĄĢ
ëÂĄŠŋÕÆøČžÁÏĩįģØ·ÅĩįĘąĢš
ÕýžŦĩÄĩįžŦ·īÓĶĘ―ĘĮ ĄĢ
ļšžŦĩÄĩįžŦ·īÓĶĘ―ĘĮ
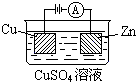
ĢĻ3ĢĐÓŌÍžĘĮŌŧļöĩįŧŊŅ§đýģĖĘūŌâÍžĄĢ

ĒŲÐŋÆŽÉÏ·ĒÉúĩÄĩįžŦ·īÓĶĘĮ ĄĢ
ĒÚžŲÉčĘđÓÃëÂŌŧŋÕÆøČžÁÏĩįģØŨũΊąūđýģĖÖÐĩÄĩįÔīĢŽÍÆŽĩÄÖĘÁŋąäŧŊ128gĢŽÔōëÂŌŧŋÕÆøČžÁÏĩįģØĀíÂÛÉÏÏûšÄąęąęŨžŨīŋöÏÂĩÄŋÕÆø LĢĻžŲÉčŋÕÆøÖÐŅõÆøĖåŧýšŽÁŋΊ20%ĢĐ
ĢĻ1ĢĐëÂĢĻN2H4ĢĐÓÖģÆÁŠ°ąĢŽĘĮŌŧÖÖŋÉČžÐÔĩÄŌšĖåĢŽŋÉÓÃŨũŧðžýČžÁÏĄĢŌŅÖŠÔÚ101kPaĘąĢŽ3.20gN2H4ÔÚŅõÆøÖÐÍęČŦČžÉÕÉúģÉĩŠÆøĢŽ·ÅģöČČÁŋ62.4kJĢĻ25ĄæĘąĢĐĢŽN2H4ÍęČŦČžÉÕ·īÓĶĩÄČČŧŊŅ§·―ģĖĘ―ĘĮ ĄĢ
ĢĻ2ĢĐëÂĄŠŋÕÆøČžÁÏĩįģØĘĮŌŧÖÖžîÐÔČžÁÏĩįģØĢŽĩį―âÖĘČÜŌšĘĮ20%~30%ĩÄKOHČÜŌšĄĢëÂĄŠŋÕÆøČžÁÏĩįģØ·ÅĩįĘąĢšÕýžŦĩÄĩįžŦ·īÓĶĘ―ĘĮ ĄĢļšžŦĩÄĩįžŦ·īÓĶĘ―ĘĮ _ _ĄĢ
ĢĻ3ĢĐÏÂÍžĘĮŌŧļöĩįŧŊŅ§đýģĖĘūŌâÍžĄĢ

ĒŲÐŋÆŽÉÏ·ĒÉúĩÄĩįžŦ·īÓĶĘĮ ĄĢ
ĒÚžŲÉčĘđÓÃëÂĄŠŋÕÆøČžÁÏĩįģØŨũΊąūđýģĖÖÐĩÄĩįÔīĢŽÍÆŽĩÄÖĘÁŋąäŧŊ128gĢŽÔōëÂŌŧŋÕÆøČžÁÏĩįģØĀíÂÛÉÏÏûšÄąęąęŨžŨīŋöÏÂĩÄŋÕÆø LĢĻžŲÉčŋÕÆøÖÐŅõÆøĖåŧýšŽÁŋΊ20%ĢĐĄĢ
ĢĻ4ĢĐīŦÍģÖÆąļëÂĩÄ·―·ĻĘĮŌÔNaClOŅõŧŊNH3ĢŽÖÆĩÃëÂĩÄÏĄČÜŌšĄĢļ÷īÓĶĩÄĀëŨÓ·―ģĖĘ―ĘĮ ĄĢ
ĢĻ1ĢĐëÂĢĻN2H4ĢĐÓÖģÆÁŠ°ąĢŽĘĮŌŧÖÖŋÉČžÐÔĩÄŌšĖåĢŽŋÉÓÃŨũŧðžýČžÁÏĄĢŌŅÖŠÔÚ101kPaĘąĢŽ3.20gN2H4ÔÚŅõÆøÖÐÍęČŦČžÉÕÉúģÉĩŠÆøĢŽ·ÅģöČČÁŋ62.4kJĢĻ25ĄæĘąĢĐĢŽN2H4ÍęČŦČžÉÕ·īÓĶĩÄČČŧŊŅ§·―ģĖĘ―ĘĮ ĄĢ
ĢĻ2ĢĐëÂĄŠŋÕÆøČžÁÏĩįģØĘĮŌŧÖÖžîÐÔČžÁÏĩįģØĢŽĩį―âÖĘČÜŌšĘĮ20%~30%ĩÄKOHČÜŌšĄĢëÂĄŠŋÕÆøČžÁÏĩįģØ·ÅĩįĘąĢšÕýžŦĩÄĩįžŦ·īÓĶĘ―ĘĮ ĄĢļšžŦĩÄĩįžŦ·īÓĶĘ―ĘĮ _ _ĄĢ
ĢĻ3ĢĐÏÂÍžĘĮŌŧļöĩįŧŊŅ§đýģĖĘūŌâÍžĄĢ
ĒŲÐŋÆŽÉÏ·ĒÉúĩÄĩįžŦ·īÓĶĘĮ ĄĢ
ĒÚžŲÉčĘđÓÃëÂĄŠŋÕÆøČžÁÏĩįģØŨũΊąūđýģĖÖÐĩÄĩįÔīĢŽÍÆŽĩÄÖĘÁŋąäŧŊ128gĢŽÔōëÂŌŧŋÕÆøČžÁÏĩįģØĀíÂÛÉÏÏûšÄąęąęŨžŨīŋöÏÂĩÄŋÕÆø LĢĻžŲÉčŋÕÆøÖÐŅõÆøĖåŧýšŽÁŋΊ20%ĢĐĄĢ
ĢĻ4ĢĐīŦÍģÖÆąļëÂĩÄ·―·ĻĘĮŌÔNaClOŅõŧŊNH3ĢŽÖÆĩÃëÂĩÄÏĄČÜŌšĄĢļ÷īÓĶĩÄĀëŨÓ·―ģĖĘ―ĘĮ ĄĢ
đúžĘŅ§ÐĢÓÅŅĄ - Á·Ï°ēáÁÐąí - ĘÔĖâÁÐąí
šþąąĘĄŧĨÁŠÍøÎĨ·ĻšÍēŧÁžÐÅÏĒūŲąĻÆ―ĖĻ | ÍøÉÏÓКĶÐÅÏĒūŲąĻŨĻĮø | ĩįÐÅÕĐÆūŲąĻŨĻĮø | ÉæĀúĘ·ÐéÎÞÖũŌåÓКĶÐÅÏĒūŲąĻŨĻĮø | ÉæÆóĮÖČĻūŲąĻŨĻĮø
ÎĨ·ĻšÍēŧÁžÐÅÏĒūŲąĻĩįŧ°Ģš027-86699610 ūŲąĻÓĘÏäĢš58377363@163.com