
ƒø¡–±Ì(∞¸¿®¥∞∏∫ÕΩ‚Œˆ)
¿Î◊”∑Ω≥Ã Ω’˝ŒÛ≈–∂œ◊®Ã‚£®’˝»∑µƒ—°A£¨¥ÌŒÛµƒ—°B£©
π˝¡øµƒNaHSO4”ÎBa(OH)2»Ð“∫∑¥”¶£∫Ba2£´£´2OH£≠£´2H£´£´SO42£≠=BaSO4°˝£´2H2O
NH4HCO3»Ð“∫”Îπ˝¡øNaOH»Ð“∫∑¥”¶£∫NH4£´£´OH£≠=NH3°¸£´H2O
±Ω∑”ƒ∆»Ð“∫÷–Õ®»Î…Ÿ¡ø£∫![]() £≠O£≠£´CO2£´H2O°˙
£≠O£≠£´CO2£´H2O°˙![]() £≠OH£´HCO3£≠
£≠OH£´HCO3£≠
FeBr2»Ð“∫÷–Õ®»Îπ˝¡øCl2£∫2Fe2£´£´2Br£≠£´2Cl2=2Fe3£´£´Br2£´4Cl£≠
≈®«‚—ıªØƒ∆»Ð“∫Œ¸ ’…Ÿ¡øSO2∆¯Ã£∫SO2+2OH£≠£ΩSO32£≠+H2O
¡ÚÀ·Õ≠»Ð“∫÷–Õ®»Î¡ÚªØ«‚ Cu2++H2S=CuS°˝+2H+
¬»ªØ¬¡»Ð“∫÷–º”»Îπ˝¡ø∞±ÀÆ Al3++4NH3°§H2O=AlO2£≠+4NH4++2H2O
úÀ·«‚ƒ∆»Ð“∫÷–º”»Îπ˝¡ø«‚—ıªØƒ∆»Ð“∫HCO3£≠+OH£≠=CO32£≠+H2O
œÚ±•∫ÕúÀ·«‚∏∆»Ð“∫÷–º”»Î±•∫Õ«‚—ıªØ∏∆»Ð“∫
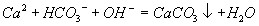
Ω Ù¬¡»Ð”⁄«‚—ıªØƒ∆»Ð“∫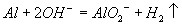
”√«‚—ıªØƒ∆»Ð“∫Œ¸ ’∂˛—ıªØú
Fe2(SO4)3µƒÀ·–‘»Ð“∫÷–Õ®»Î◊„¡ø¡ÚªØ«‚![]()
¥Œ¬»À·∏∆»Ð“∫÷–Õ®»Îπ˝¡ø∂˛—ıªØúCa2++2ClO-+H2O+CO2 == CaCO3↓+2HClO
úÀ·«‚√æ»Ð“∫÷–º”»Î◊„¡øµƒ…’ºÓ»Ð“∫£∫Mg2++2HCO3-+2OH-=MgCO3°˝+CO32-+2H2O
”√∞±ÀÆŒ¸ ’…Ÿ¡ø∂˛—ıªØ¡Ú£∫NH3°§H2O+SO2 == NH![]() +HSO
+HSO![]()
œıÀ·Ã˙»Ð“∫÷–º”π˝¡ø∞±ÀÆ£∫Fe3++3 NH3°§H2O == Fe(OH)3↓+3NH![]()
¡ÚªØƒ∆»Ð”⁄ÀÆ÷– S2£≠+2H2O H2S°¸+2OH£≠
µ—È “÷∆»°¬»∆¯ MnO2£´4H£´£´2Cl£≠ Mn2£´£´Cl2°¸£´2H2O
Õ≠”Îœ°œıÀ·∑¥”¶ 3Cu£´8H£´£´2NO3°™£Ω3Cu2£´£´2NO°¸£´4H2O
Ca(OH)2»Ð“∫÷–º”»Îµ»ŒÔ÷ µƒ¡øµƒNaHCO3
Ca2£´£´2HCO3£≠£´2OH£≠£ΩCaCO3°˝£´2H2O£´CO32£≠
NaHCO3µƒÀÆΩ‚£∫HCO3£≠£´H2O H3O£´ £´CO32£≠
H3O£´ £´CO32£≠
Ω Ù¬¡»Ð”⁄NaOH»Ð“∫£∫Al£´2OH£≠£ΩAlO2£≠£´H2°¸
∏÷Ã˙Œ¸—ı∏Ø ¥µƒ’˝º´∑¥”¶ Ω£∫4OH£≠£≠4e£≠£ΩO2£´2H2O
¡ÚÀ·—«Ã˙»Ð“∫”Îπ˝—ıªØ«‚»Ð“∫ªÏ∫œ£∫Fe2++2H2O2+4H+=Fe3++4H2O
–°À’¥Ú»Ð“∫”Îœ°¡ÚÀ·ªÏ∫œCO32£≠+2H+=CO2°¸+H2O
°°°°¥Û¿Ì Ø»ÐΩ‚”⁄¥◊À·CaCO3+2H+=Ca2++CO2°¸+H2O
»˝¬»ªØ¬¡»Ð“∫º”»»’Ù∏… Al3++3H2O=Al(OH)3°˝+3H+
¡ÚÀ·¬¡»Ð“∫÷–º”»Îπ˝¡ø∞±ÀÆ Al3++3OH°™®T®TAl(OH)3°˝
µÁΩ‚±•∫Õ ≥—ŒÀÆ 2Cl°™+2H2O H2°¸+C12°¸+20H°™
H2°¸+C12°¸+20H°™
úÀ·∏∆”ΗŒÀ·∑¥”¶ CaCO3+2H+®TCa2++CO2°¸ +H2O
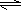 H2CO3+OH-«“HCO3-ÀÆΩ‚≥Ã∂»¥Û”⁄µÁ¿Î≥Ã∂»£¨π »Ð“∫≥ ºÓ–‘
H2CO3+OH-«“HCO3-ÀÆΩ‚≥Ã∂»¥Û”⁄µÁ¿Î≥Ã∂»£¨π »Ð“∫≥ ºÓ–‘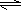 H2CO3+OH-«“HCO3-ÀÆΩ‚≥Ã∂»¥Û”⁄µÁ¿Î≥Ã∂»£¨π »Ð“∫≥ ºÓ–‘
H2CO3+OH-«“HCO3-ÀÆΩ‚≥Ã∂»¥Û”⁄µÁ¿Î≥Ã∂»£¨π »Ð“∫≥ ºÓ–‘A.98.3%¡ÚÀ·º”»ÎµΩœ°«‚—ıªØ±µ»Ð“∫÷–£∫H+(aq)+OH-(aq) ====H2O(aq);¶§H=-57.3 kJ°§mol-1
B.”√¡Ω∏ˆÕ≠µÁº´µÁΩ‚œ°—ŒÀ·£∫2H++2Cl-![]() H2°¸+Cl2°¸
H2°¸+Cl2°¸
C.Ω»Ð”⁄ÕıÀÆ≤˙…˙¥Û¡øµƒ![]() ∫ÕNO£¨Au+4H++4Cl-+
∫ÕNO£¨Au+4H++4Cl-+![]() ====
====![]() +NO°¸+2H2O
+NO°¸+2H2O
D.NaHCO3»Ð“∫”ÎNaAlO2»Ð“∫ªÏ∫œ≤˙…˙∞◊…´≥¡µÌ![]() +
+![]() +H2O====Al(OH)3°˝+CO2°¸
+H2O====Al(OH)3°˝+CO2°¸
“—÷™NaHCO3»Ð“∫∫ÕNaOH»Ð“∫∑¥”¶µƒ¿Î◊”∑Ω≥Ã ΩŒ™£∫HCO3£≠+OH£≠=CO32£≠+H2O£¨NaHCO3‘⁄ÀÆ÷–µƒµÁ¿Î∑Ω≥Ã ΩŒ™£∫NaHCO3= Na++HCO3£≠£¨œ¬¡–¿Î◊”∑Ω≥à Ω≤ª’˝»∑µƒ «£® £©
A.œıÀ·“¯»Ð“∫”ÎÕ≠£∫Cu+2Ag+=Cu2++2Ag
B.Ba(HCO3)2»Ð“∫∫Õ¡ÚÀ·ªÏ∫œ£∫Ba2++ SO42£≠+2H+ +2HCO3£≠=BaSO4°˝+ 2H2O+2CO2°¸
C.—ıªØÕ≠”ΗŒÀ·∑¥”¶£∫O2£≠+2H+=H2O
D.Cu(OH)2º”»ÎH2SO4£∫2H++Cu(OH)2 = Cu2+ +2H2O
µ⁄IæÌ —°‘ÒÂ
1.A 2.C 3.B 4.C 5.B 6. C 7.B 8.A 9. D 10. C 11. A 12.C 13.B
14. C 15 .A 16.B 17.ACD 18. BC 19.B 20. BD 21. AD
µ⁄IIæÌ ∑«—°‘ÒÂ
22 I 0.590 2.642
 √øø’2∑÷£¨π≤4∑÷°£
√øø’2∑÷£¨π≤4∑÷°£
¢Ú£®1£©E£ªC
£®2£©º◊
£®3£©¡¨Ω” µŒÔÕº
£®4£©¢Ÿ±‰¥Û ¢⁄10¶∏
£®1£©√øø’1∑÷£®2£©3∑÷£®3£©4∑÷£®4£©√øø’2∑÷°£
23£Æ
£®1£©”…–°ŒÔøÈ…œª¨π˝≥õƒÀŸ∂»®D ±º‰Õºœþ£¨ø…÷™£∫ £®3∑÷£©
£®3∑÷£©
 m/s2
£®1∑÷£©
m/s2
£®1∑÷£©
–°ŒÔøÈ≥Â…œ–±√Êπ˝≥Ã÷–º”ÀŸ∂»µƒ¥Û–°Œ™
£®2£©–°ŒÔøÈ Ð÷ÿ¡¶°¢÷ß≥÷¡¶°¢ƒ¶≤¡¡¶£¨—ÿ–±√ÊΩ®¡¢÷±Ω«◊¯±Íœµ£¨
 £®2∑÷£©
£®2∑÷£©
 £®2∑÷£©
£®2∑÷£©
 £®2∑÷£©
£®2∑÷£©
¥˙»Î ˝æðΩ‚µ√  £®2∑÷£©
£®2∑÷£©
£®3£©…ËŒÔøÈ≥Â…œ–±√ÊÀ˘ƒÐ¥ÔµΩµƒ◊Ó∏þµ„æý–±√ʵ◊∂Àæý¿ÎŒ™s£¨
œÚ…œ‘À∂ØΩ◊∂Œ  £®3∑÷£©
£®3∑÷£©
 £®1∑÷£©
£®1∑÷£©
24£ÆΩ‚£∫–°≥µ‘⁄∞Îæ∂Œ™Rµƒ‘≤÷Ð…œ◊˜‘≤÷БÀ∂Ø£¨¥¶”⁄‘≤÷Ðπϵ¿µƒ◊Ó∏þµ„ ±£¨–°≥µ∫Õ»ÀÀ˘ Ð÷ÿ¡¶÷Æ∫Õ÷π©œÚ–ƒ¡¶£¨…Ë–°≥µª¨––µΩDµ„ ±µƒÀŸ∂»Œ™u£¨∏˘æð≈£∂Ÿµ⁄∂˛∂®¬…
 £®4∑÷£©
£®4∑÷£©
µ√u= m
m
…Ë»À∫Õ–°≥µ“‘π≤Õ¨ÀŸ∂»v £¨¥”ÀÆ∆Ω√Ê‘À∂صΩDµƒπ˝≥Ã÷–ª˙–µƒÐ ÿ∫„£¨∏˘æðª˙–µƒÐ ÿ∫„∂®¬…µ√
 £®4∑÷£©
£®4∑÷£©
v=15m/s £®2∑÷£©
‘⁄»ÀΩ”¥•–°≥µ£¨≤¢ π–°≥µ∫Õ»À“ª∆«∞Ω¯µƒπ˝≥Ã÷–£¨ŒÞÀÆ∆Ω∑ΩœÚÕ‚¡¶◊˜”√£¨π ÀÆ∆Ω∑ΩœÚ…œ∂Ø¡ø ÿ∫„£¨µ√
 (4∑÷)
(4∑÷)
v0=20m/s £®3∑÷£©
25£Æ£®1£©÷ ◊”…‰»Î¥≈≥°∫Û◊ˆ‘»ÀŸ‘≤÷БÀ∂Ø£¨”–
evB=mv2/r £®3∑÷£©
ø…µ√v=eBr/m £®1∑÷£©
£®2£©÷ ◊”—ÿx÷·’˝œÚ…‰»Î¥≈≥°∫Ûæ≠1/4‘≤ª°∫Û“‘ÀŸ∂»v¥π÷±”⁄µÁ≥°∑ΩœÚΩ¯»ÎµÁ≥°£¨÷Ð∆⁄Œ™
 £®2∑÷£©
£®2∑÷£©
‘⁄¥≈≥°÷–‘À∂صƒ ±º‰
t1=T/4=¶–m/2eB £®1∑÷£©
Ω¯»ÎµÁ≥°∫Û◊ˆ≈◊ŒÔœþ‘À∂Ø£¨—ÿµÁ≥°∑ΩœÚ‘À∂Ør∫ÛµΩ¥Ôy÷·£¨“Ú¥À”–
 £®1∑÷£©
£®1∑÷£©
t2= £®1∑÷£©
£®1∑÷£©
À˘«Û ±º‰Œ™t=
t1+ t2=
 £®1∑÷£©
£®1∑÷£©
£®3£©÷ ◊”‘⁄¥≈≥°÷–◊™π˝120°„Ω«∫Û¥”Pµ„¥π÷±µÁ≥°œþΩ¯»ÎµÁ≥°£¨»ÁÕºÀ˘ æ°£°°°°
Pµ„æýy÷·µƒæý¿Î
x1=r+rsin30°„=1.5r°°°°°°  £®2∑÷£©
£®2∑÷£©
“Ú¥Àø…µ√÷ ◊”¥”Ω¯»ÎµÁ≥°÷¡µΩ¥Ôy÷·À˘–Ë ±º‰Œ™
 =
= £®2∑÷£©
£®2∑÷£©
÷ ◊”‘⁄µÁ≥°÷–—ÿy÷·∑ΩœÚ◊ˆ‘»ÀŸ÷±œþ‘À∂Ø£¨“Ú¥À”–
 £®2∑÷£©
£®2∑÷£©
÷ ◊”µΩ¥Ôy÷·µƒŒª÷√◊¯±ÍŒ™ º¥£®0£¨r+
º¥£®0£¨r+ £© (2∑÷)
£© (2∑÷)

Õº £®2∑÷£©
26£Æ£®10∑÷£©£®1£©N2 £®2∑÷£©
 |
£®2£© £®2∑÷£¨»Á–¥≥ˆCO’˝»∑µƒµÁ◊” Ω“≤∏¯∑÷£©
£®3£©¿Î◊”º¸°¢∑«º´–‘º¸°££®2∑÷£¨µ⁄∂˛ø’¥π≤º€º¸“≤∏¯∑÷£© ¢⁄¢Ð £®2∑÷£¨¥∞∏»´’˝»∑∏¯∑÷£©
£®4£©CS2+2H2O CO2+2H2S£®2∑÷£©
CO2+2H2S£®2∑÷£©
27£Æ£®18∑÷£©£®1£©Al+4OH-?3e- = AlO2-+2H2O(2∑÷)
£®2£©10-2?10-12 mol/L£¨ ªÚc(OH-)?c(H+) (2∑÷) < (2∑÷)
£®3£©∑Ò(1∑÷)£ª“ÚŒ™Aµƒ¬»ªØŒÔ»€∑–µ„µÕ£¨æð¥À≈–∂œÀ¸µƒæßÃÂŒ™∑÷◊”æß㨑⁄»€»⁄è ±≤ªµÁ¿Î£¨≤ªƒÐ±ªµÁΩ‚(2∑÷)°£
 |
£®4£©4NH3+5O2 4NO+6H2O £®2∑÷£¨Ãıº˛¥ÌŒÛø€1∑÷£©
|