
题目列表(包括答案和解析)
 4NO+6H2O
4NO+6H2O 4NO+6H2O
4NO+6H2O +HNO3(浓)
+HNO3(浓)| H2SO4(浓) |
| 50-60℃ |
 -NO2+H2O
-NO2+H2O +HNO3(浓)
+HNO3(浓)| H2SO4(浓) |
| 50-60℃ |
 -NO2+H2O
-NO2+H2O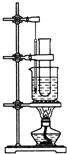 实验室用苯和浓硝酸、浓硫酸发生反应制取硝基苯的装置如下图所示.请回答下列问题:
实验室用苯和浓硝酸、浓硫酸发生反应制取硝基苯的装置如下图所示.请回答下列问题:

实验室用苯和浓硝酸、浓硫酸发生反应制取硝基苯的装置如图所示.回答下列问题:
(1)反应需在50℃~60℃的温度下进行,图中给反应物加热的方法是________,其优点是________和________;
(2)在配制混合酸时应将__________加入到________中去;
(3)该反应的化学方程式是___________________________________________;
(4)由于装置的缺陷,该实验可能会导致的不良后果是________.
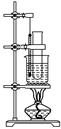
实验室用苯和浓硝酸、浓硫酸发生反应制取硝基苯的装置如下图所示。请回答下列问题:

(1) 反应需在55~60 °C的温度下进行,图中给反应物加热的方法是________,其优点是________________和________________;
(2) 在配制混合酸时应将__________加入到________中去;
(3) 该反应的化学方程式是__________________________________;
(4) 由于装置的缺陷,该实验可能会导致的不良后果是:________;
(5) 反应完毕后, 除去混合酸,所得粗产品用如下操作精制:
①蒸馏 ②水洗 ③用干燥剂干燥 ④用10% NaOH溶液洗 ⑤水洗
正确的操作顺序是________。
A.①②③④⑤ B.②④⑤③①
C.④②③①⑤ D.②④①⑤③
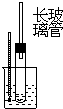 实验室制备少量硝基苯的主要步骤如下:
实验室制备少量硝基苯的主要步骤如下:命题:林文土
6~~12 B B D A A C C
23、(19分)(1)2、5、6、7(3分,多选1个倒扣1分)
(2)①250mL容量瓶 34.75 (各1分)
②取最后的洗涤液,测定洗涤液的pH,若洗涤液的pH等于7,说明已经洗涤干净(或取最后的洗涤液,向其中滴加BaCl2溶液,若无浑浊产生,则说明已经洗涤干净。) (2分) ③ab (2分)
(3)Ⅰ、关闭活塞a、b,将出气导管口浸没在液面以下,用手掌或热毛巾紧贴烧瓶外壁一小会儿,若出气导管口有气泡冒出,松手或拿走热毛巾后导管内回升一段水柱,证明A装置不漏气。(2分)
Ⅱ、ACBECF(2分);
Ⅲ、①氢氧化钠遇水放出大量热,温度升高,使氨的溶解度减小而放出;氢氧化钠电离出的OH-增大了氨水中OH-浓度,促使氨水电离平衡左移,导致氨气放出。(2分)
②4NH3十5O2 4NO+6H2O(2分)③说明氨的氧化反应是一个放热反应(2分)
4NO+6H2O(2分)③说明氨的氧化反应是一个放热反应(2分)
24、(13分)
Ⅰ(4分)(1)S2―>O2―>Na+ (2)SO2+Cl2+2H2O=2HCl+H2SO4(每空2分)
Ⅱ(4分)(1)Ag++e― =Ag,2H++2e―=H2↑ (2)2.24L(每空2分)
Ⅲ(2分)C(s)+O2(g)=CO2(g) △H=-393.5kJ?mol―1
Ⅳ NaNO2(1分) 8 (2分)
25、(每空2分,共14分)
(1)Cl2+2OH-=Cl-+ClO-+H2O w.w.w.k.s.5 u.c.o.m;(2)C、浓H2SO4
(3)MnO2+4H++2Cl-
 Mn2++Cl2↑+2H2O;(4)Na2SO4、O2
Mn2++Cl2↑+2H2O;(4)Na2SO4、O2
(5)AlCl3 NaAlO 2
2
(6)Cu+4HNO3(浓)=Cu(NO3)2+2NO2↑+2H2O[或3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O]
30、(共12分)
(1)1s22s22p63s23p63d84s2 (2分) (2) C≡O (2分) (3) 分子晶体(2分) 配位键(共价键)(2分) (4)MgCNi3 (2分) 12个(2分)
31、(共12分)(1) (2) (a) 消去反应 (b)
(2) (a) 消去反应 (b) 
(c) F中含碳碳双键,羟基氧化时可能会同时氧化碳碳双键,使最终不能有效、顺利地转化为B
(d)⑥
⑦
2009届安溪县高三年理综统练生物试卷参考答案
命题:黄文坚
1-5:CACBC
26.(每空2分,共24分)
 Ⅰ(14分)Aa1、a1a2、a2a2 (2)1/4 , 1/2
(3)2/3 (4)(6分,亲代表现型和后代表现型,以及表现型之比、亲代和子代基因型,配子各1分)
Ⅰ(14分)Aa1、a1a2、a2a2 (2)1/4 , 1/2
(3)2/3 (4)(6分,亲代表现型和后代表现型,以及表现型之比、亲代和子代基因型,配子各1分)
II、(10分)基因库 64% (2)自然选择 (3)发生了进化,因为只要种群基因频率改变,就是在进化;(4)没有产生新物种,只是种群基因频率改变,并没有产生生殖隔离。
27.(共16分)(1)温度、氧浓度、水分(2分)
(2)细胞中原来就存在这些特殊蛋白质基因,春化作用(低温处理)激活了这些基因(2分)
(3)细胞分化(2分)特定基因表达或抑制(2分)
(4)选取粒大饱满的冬小麦种子若干,浸种并使其萌芽,配制不同浓度梯度的赤霉素溶液。(2分)
对照组:冬小麦幼苗10株,不经低温和赤霉素处理(2分)
实验组A:冬小麦幼苗10株,低温处理(2分)
实验组B:不经低温,然后用不同浓度梯度的赤霉素溶液处理,每种浓度的赤霉素溶液处理10株冬小麦幼苗。(2分)(其它如表格形式等合理答案也可)
32.(共10分)(1) ①目的基因的检测与表达 ②DNA聚合 ③脱分化(1分) 再分化(1分) ④ABC (2)筛选和检测
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com