
题目列表(包括答案和解析)
工业合成氨与制备硝酸一般可连续生产,流程如下:

(1)工业生产时,制取氢气的一个反应为:CO+H2O(g) CO2+H2
①t℃时,往1L密闭容器中充入0.2mol CO和0.3mol水蒸气。反应建立平衡后,体系中c(H2)=0.12mol·L-1。该温度下此反应的平衡常数K=_____(填计算结果)。
②保持温度不变,向上述平衡体系中再加入0.1molCO,当反应重新建立平衡时,水蒸气的转化率α(H2O)=________。
 (2)合成塔中发生反应N2(g)+3H2(g)
2NH3(g);△H<0。下表为不同温度下该反应的平衡常数。由此可推知,表中
(2)合成塔中发生反应N2(g)+3H2(g)
2NH3(g);△H<0。下表为不同温度下该反应的平衡常数。由此可推知,表中
T1____573K(填“>”、“<”或“=”)。
 (3)NH3和O2在铂系催化剂作用下从145℃就开始反应:
(3)NH3和O2在铂系催化剂作用下从145℃就开始反应:
4NH3(g)+5O2(g) 4NO(g)+6H2O(g) △H=-905kJ·mol-1
不同温度下NO产率如图所示。温度高于900℃时,
NO产率下降的原因 。
(4)吸收塔中发生反应的化学方程式为:
。
(5)上述工业流程中,采用了循环操作工艺的是 (填序号)
(6)硝酸厂的尾气含有氮氧化物,如果不经处理直接排放将污染空气。目前科学家探索利用燃料气体中的甲烷等将氮氧化物还原为氮气和水,其反应机理为:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g); △H=-574kJ·mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g); △H=-1160kJ·mol-1
则甲烷直接将NO2还原为N2的热化学方程式为:_____________________________。
已知充分燃烧a g乙炔(C2H2)气体时生成1 mol CO2气体和液态水,并放出热量b kJ,则乙炔燃烧的热化学方程式正确的是
A、2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) ΔH=-4b kJ·mol-1
B、C2H2(g)+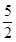 O2(g)=2CO2(g)+H2O(l) ΔH=2b kJ·mol-1
O2(g)=2CO2(g)+H2O(l) ΔH=2b kJ·mol-1
C、2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) ΔH=-2b kJ·mol-1
D、2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) ΔH=-b kJ·mol-1
已知乙炔与苯蒸气完全燃烧的热化学方程式如下所示:
① 2C2H2(g) + 5O2(g) 4CO2(g) + 2H2O(l) + 2600 kJ
4CO2(g) + 2H2O(l) + 2600 kJ
② 2C6H6(g) +15O2(g) 12CO2(g) + 6H2O(l) + 6590
kJ
12CO2(g) + 6H2O(l) + 6590
kJ
下列说法正确的是
A.2mol C2H2(g) 完全燃烧生成气态水时放热大于2600kJ
B.2mol C6H6(l) 完全燃烧生成液态水时放热小于6590kJ
C.相同条件下,等质量的C2H2(g)与C6H6(g)完全燃烧,C6H6(g)放热更多
D.C2H2(g) 三聚生成C6H6(g) 的过程属于放热反应
以NA代表阿伏罗德常数,则下列关于热化学方程式:
2C2H2(g)+5O2(g) ===4CO2(g) +2H2O(1);△H=-2600kJ·mol-1的说法正确的是
A.有10NA个电子转移时,该反应吸收1300kJ的能量
B.有NA个水分子生成且为液体时,吸收1300kJ的能量
C.有2NA个碳氧共用电子对生成时,放出1300kJ的能量
D.有8NA个碳氧共用电子对生成时,放出1300kJ的能量
已知充分燃烧a g乙炔气体时生成1mol二氧化碳气体和液态水,并放出热量b kJ,则乙炔燃烧的热化学方程式正确的是
A. 2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l); ΔH=-2b kJ??mol??1
B. C2H2(g)+5/2O2(g)=2CO2(g)+H2O(l); ΔH=2b kJ??mol??1
C. 2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l); ΔH=-4b kJ??mol??1
D. 2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l); ΔH=b kJ??mol??1
题号
1
2
3
4
5
6
答案
A
C
C
B
A
B
题号
7
8
9
10
11
12
13
答案
B
B
C
A
C
D
D
题号
14
15
16
17
18
19
20
21
答案
A
B
C
A
BCD
BD
BCD
CD
三、实验与探究。本题共1小题
 22答案:(1)3.715或
22答案:(1)3.715或
(2)①C、(2分) G、(2分)
②(5分)如图。
伏安法连接正确3分
变阻器连接正确2分
③设长度为l,截面外边长为a,电压为U,电流强度为I.
电阻 ,横截面积
,横截面积
故有 解得
解得 (5分)
(5分)
23解:(1)汽车的额定功率为P=fVm=0.1MgVm=80000(w) (2分)
在t3时刻 P=F1v3 (2分)
F1-f=Ma (2分)
解得a=
(2) 汽车从启动到速度达到最大值过程中根据动能定理
 (4分)
(4分)
解得t=16s(2分)
24.解:(1)带电粒子从原点射入匀强磁场,做匀速圆周运动,从O到P经历半个周期,即: (2分)
(2分)  (2分) 解出
(2分) 解出 (2分)
(2分)
(2)带电粒子在磁场中
 (2分) 得
(2分) 得 (2分)
(2分)
 以v=
以v= 的速度射入匀强电场,做类平抛运动,设电场强度大小为E,
的速度射入匀强电场,做类平抛运动,设电场强度大小为E,
 (2分)
(2分)
 (2分)
(2分)
 (2分)
(2分)
解得 (2分)
(2分)
25解:(1)从O→MN过程中棒做匀加速运动,设O→MN间距s
 (3分)
(3分)
从MN→P的过程中做匀减速运动,故F1大小不变,
 (3分)
(3分)
得 (2分)
(2分)
(2)棒从MN→P过程中能量守恒
 (4分)
(4分)
得: (2分)
(2分)
(3)在磁场中运动距离x后速度vx
 (3分)
(3分)
此时安培力 (3分)
(3分)
解得 (2分)
(2分)
26.(12分)(1)H:H、Fe2O3(各1分)
(2) 四 Ⅷ(各1分)
(3)先产生白色沉淀,逐渐变为灰绿色,最后变为红褐色。(2分)
 (4)4H2+Fe3O4
(4)4H2+Fe3O4
 3Fe+4H2O(2分)(合理均可给分) 2Fe+3Cl2 2FeCl3(2分)
3Fe+4H2O(2分)(合理均可给分) 2Fe+3Cl2 2FeCl3(2分)
(5)2Fe3+ + SO2 + 2H2O == 2Fe2+ + SO42- +4H+ (2分)
27.(14分) (1)醋酸钾(2分)
(2)Ba(OH)2+Na2SO4 === BaSO4 ↓ + 2NaOH(2分)
(3)Ba(OH)2(2分)
(4)= (2分)
(5)c(OH―)>c(Ba2+)=c(Cl―)>c(NH4+)>c(H+)
或c(OH―)>c(Cl―)=c(Ba2+)>c(NH4+)>c(H+) (3分)
(6)2:3 (3分)
28.(17分)(1)水浴, 酒精灯、烧杯、温度计 (4分)
(2) 洗涤晶体表面附着的杂质、减少阿司匹林因溶解而引起的损耗。(2分)
(3) 使阿司匹林转化为可溶性盐,而与不溶性的物质相互分离。(2分)
将阿司匹林的可溶性盐重新转化为阿司匹林。(2分)
(4) 向水中加入少量产品,然后滴加FeCl3溶液,若有紫色出现,产品中有水杨酸;
若无紫色出现,说明产品中不含水杨酸。(合理答案均可给分)(3分)
(5)0.80 或 80% (4分)
29.(15分)
(1)B  D
D (各2分)
(各2分)
(2)取代反应,加成反应或还原反应 (各1分) (3)C (2分) (4)C (2分)
 (5)
(5)
(各1分)
 (6)
(6)
(2分)
30.(20分)
(1)红眼(2分) (2)遵循(2分) 杂种子一代自交的后代发生性状分离,且分离比为3:1(2分)
(3)控制眼色性状的基因位于X染色体上,Y染色体上没有它的等位基因(2分)
(4)不能(2分)
 |
从上述图解中可以看出,不论基因在常染色体还是性染色体上,其后代均有两种表现型,且每种表现型的性别比率均为1:1(2分)
(5)实验二中的白眼雌蝇×红眼雄蝇交配(2分)
31、(24分,每空2分)
Ⅰ.(1)原核 无成形细胞核
(2)对照 无氧呼吸 有氧呼吸弱、无氧呼吸强
(3)0.2 (有氧呼吸反应式略)
Ⅱ.(1)表示光合作用强度等于呼吸作用强度
(2)温度适当增加 CO2的浓度适当增加
(3)多 (图)

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com