
题目列表(包括答案和解析)
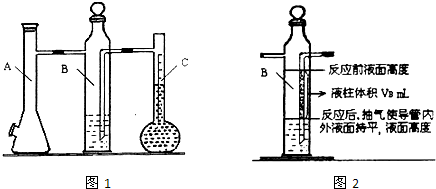
| 实验次数 | m(Mg)/g | 硫酸体积/mL | 液体量瓶中液体体积/mL | 抽出气体体积/mL | 氢气体积/mL | 计算1mol氢体积/L |
| 1 | 0.100 | 10.0 | 110.0 | 6.5 | X | |
| 2 | 0.115 | 10.0 | 121.0 | 8.0 |
| 实验次数 | m(Mg) g |
硫酸体积mL | 液体量瓶中液体体积mL | 抽出气体体积mL | B瓶的一段液柱体积mL | 水汽体积百分含量 | 计算1mol氢体积L |
| 1 | 0.100 | 10.0 | 110.0 | 6.5 | VB | a% |
用下图所示装置可进行测定![]() 转化为
转化为![]() 的转化率的实验。
的转化率的实验。

(1)根据实验的需要,(Ⅰ)、(Ⅱ)、(Ⅲ)处应连接合适的装置。请从A-E中选择合适的装置,将其序号填入以下空格内。
(Ⅰ)、(Ⅱ)、(Ⅲ)处所连接的装置分别为________、________、________。
(2)实验时,浓硫酸能顺利地滴入烧瓶中,甲仪器所起作用的原理是:________。
(3)从乙处均匀通入![]() ,为使
,为使![]() 有较高的转化率,实验时,在加热与滴加浓硫酸过程中,应采取的操作是:________。
有较高的转化率,实验时,在加热与滴加浓硫酸过程中,应采取的操作是:________。
(4)用大火加热烧瓶时,![]() 的转化率会________(填“提高”、“不变”或“降低”)。
的转化率会________(填“提高”、“不变”或“降低”)。
(5)用a
mol![]() 粉末与足量浓硫酸进行此实验,
当反应结束时, 继续通入
粉末与足量浓硫酸进行此实验,
当反应结束时, 继续通入![]() 一段时间后,
称得(Ⅲ)装置增重b
g, 则本实验中
一段时间后,
称得(Ⅲ)装置增重b
g, 则本实验中![]() 的转化率为________。
的转化率为________。
用图中所示实验装置证明氧化铜能加快约7%的双氧水的分解并与二氧化锰的催化效果进行比较(即比较反应速率)。用图示装置测量产生气体的体积,其他可能影响实验的因素均已忽略,相关数据如下: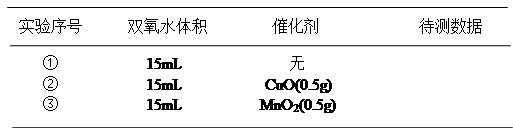
(1)从实验原理来看,实验中的“待测数据”可以指 、也可以指 。
(2)实验时气体收集在B中,B仪器名称是__________。若要检验产生的气体是O2,待气体收集结束后,用弹簧夹夹住B下端乳胶管,打开单孔橡皮塞, 。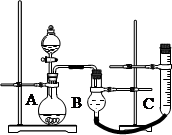
(3)为探究CuO在实验②中是否起催化作用,除与①比较外,还需补做下列实验不必写具体步骤):a.证明CuO的化学性质没有变化,b. 。
(4)为证明氧化铜的化学性质在加入双氧水前后没有发生改变,你设计验证的实验是 。
(5)实验开始时,当往容器中加入一定量的双氧水后,由于短时间内产生大量气体,分液漏斗内的液体不能顺利流下,为了解决这个问题,你采取的措施是
;
在测量生成的气体体积时,除了要注意视线与凹液面相平以外,还应注意
用图中所示实验装置证明氧化铜能加快约7%的双氧水的分解并与二氧化锰的催化效果进行比较(即比较反应速率)。用图示装置测量产生气体的体积,其他可能影响实验的因素均已忽略,相关数据如下:
(1)从实验原理来看,实验中的“待测数据”可以指 、也可以指 。
(2)实验时气体收集在B中,B仪器名称是__________。若要检验产生的气体是O2,待气体收集结束后,用弹簧夹夹住B下端乳胶管,打开单孔橡皮塞, 。

(3)为探究CuO在实验②中是否起催化作用,除与①比较外,还需补做下列实验不必写具体步骤):a.证明CuO的化学性质没有变化,b. 。
(4)为证明氧化铜的化学性质在加入双氧水前后没有发生改变,你设计验证的实验是 。
(5)实验开始时,当往容器中加入一定量的双氧水后,由于短时间内产生大量气体,分液漏斗内的液体不能顺利流下,为了解决这个问题,你采取的措施是
;
在测量生成的气体体积时,除了要注意视线与凹液面相平以外,还应注意
用图中所示实验装置证明氧化铜能加快约7%的双氧水的分解并与二氧化锰的催化效果进行比较(即比较反应速率)。用图示装置测量产生气体的体积,其他可能影响实验的因素均已忽略,相关数据如下:
(1)从实验原理来看,实验中的“待测数据”可以指、也可以指 。
(2)实验时气体收集在B中,B仪器名称是__________。若要检验产生的气体是O2,待气体收集结束 后,用弹簧夹夹住B下端乳胶管,打开单孔橡皮塞, 。
(3)为探究CuO在实验②中是否起催化作用,除与①比较外,还需补做下列实验不必写具体步骤):a.证明CuO的化学性质没有变化,b. 。
(4)为证明氧化铜的化学性质在加入双氧水前后没有发生改变,你设计验证的实验是 。
(5)实验开始时,当往容器中加入一定量的双氧水后,由于短时间内产生大量气体,分液漏斗内的液体不能顺利流下,为了解决这个问题,你采取的措施是 ;在测量生成的气体体积时,除了要注意视线与凹液面相平以外,还应注意
第Ⅰ卷 (共66分)
一、(本题共10分)
1.B 2.A 3.D 4.C 5.D
二、(本题共36分)
6.A 7.C 8.D 9.B 10.B 11.D 12.C 13.A 14.B 15.D 16.C 17.B
三、(本题共20分)
18.A、B 19.C、D 20.A、B 21.C 22.A、D
四、(本题共24分)
23.(本题共8分)
(1)氢(1分)
(2)第二周期、ⅣA(1分)1s22s22p63s23p5(各1分)
(3)Cl(1分)
(4)B、C(2分)
(5)B、D(2分)
24.(本题共8分)
(1)+2Sn,Fe2(SO4)3(各1分)
 (2)SnCl2→SnCl4(各1分)
(2)SnCl2→SnCl4(各1分)
(3)
(4)2:1(2分)
25.(本题共8分)
(2)放热(1分)
(3)逆 增大 增大 不变(各1分)
(4)B、C(2分)
五、(本题共24分)
26.(本题共14分)
(1)储液瓶(B瓶)内导管中液面会上升,观察上升液面在1分钟内明显下降(2分)
(2)品红(1分)Mg+2H+→Mg2++H2↑(2分)
(3)① 106.5(1分) ② 25.5(2分) ③ 4.08%(1分) ④ C(1分)
(4)① ②(2分) 0.243(106.5―VB)(1―a%)(2分)
27.(本题共10分)
(1)A、C(2分)
(2)除去AlO2杂质(1分)
(3)2CrO42-+2H+→Cr2O72-+H2O(2分)
(4)① 将混合物放入烧杯中,加水,充分搅拌直到固体不再溶解。(2分)
② 蒸发(1分) ④ 冷却,结晶(2分)
六、(本题共20分)
28.(本题共9分)
(1)醛基(酚)羟基 醚键(2分)
(2)(a)取代反应(1分)
 |
(b)
(3) (1分+1分+2分)
29.(本题共11分)
(1)羧基(1分) 氧化反应(1分)
 CH3CHO+2Cu(OH)
2 CH3COOH+Cu2O↓+2H2O(2分)
CH3CHO+2Cu(OH)
2 CH3COOH+Cu2O↓+2H2O(2分)
 |
(3)
 |
(2分)
(4)四(2分); (1分)
七、(本题共16分)
30.(本题共7分)
(2)0.43(或43%)(2分)
31.(本题共9分)
(1)NaOH 1.50×10-3mol Na2CO3 5.00×10-4mol(2分)
(2)8.00mL(2分)
(3)0.201mg CO2/(g?h)(3分)
本资料由《七彩教育网》www.7caiedu.cn 提供!
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com