
ƒø¡–±Ì(∞¸¿®¥∞∏∫ÕΩ‚Œˆ)
”–ø…ƒÊ∑¥”¶£∫Fe£®s£©£´CO2£®g£©FeO£®s£©£´CO£®g£©°£“—÷™938K ±∆Ω∫‚≥£ ˝K£Ω1£Æ47£¨1173K ±∆Ω∫‚≥£ ˝K£Ω2£Æ15°£
£®1£©∏√∑¥”¶µƒ∆Ω∫‚≥£ ˝±Ì¥Ô Ω____________________£¨ «____________£®ÃÓ°∞Œ¸»»°±ªÚ°∞∑≈»»°±£©∑¥”¶°£
£®2£©»Ù∏√∑¥”¶‘⁄ê˝∫„∂®µƒ√б’»ð∆˜÷–Ω¯––£¨‘⁄“ª∂®Ãıº˛œ¬¥ÔµΩ∆Ω∫‚◊¥Ã¨£¨»Áπ˚∏ƒ±‰œ¬¡–Ãıº˛£¨∑¥”¶ªÏ∫œ∆¯Ãµƒ∆Ωæ˘œý∂‘∑÷◊”÷ ¡ø»Á∫Œ±‰ªØ£®ÃÓ°∞‘ˆ¥Û°±°¢°∞ºı–°°±ªÚ°∞≤ª±‰°±£©°£
¢Ÿ…˝∏þŒ¬∂»_________________£ª¢⁄‘ŸÕ®»ÎCO__________________°£
£®3£©∏√∑¥”¶µƒƒÊ∑¥”¶ÀŸ¬ ÀÊ ±º‰±‰ªØµƒπÿœµ»ÁÕº£∫

¢Ÿ¥”Õº÷–ø…“‘ø¥≥ˆ£¨∑¥”¶t2 ±¥ÔµΩ∆Ω∫‚£¨‘⁄
t1 ±∏ƒ±‰ƒ≥÷÷Ãıº˛£¨∏√Ãıº˛ø…ƒÐ «_______°£
A£Æ…˝∏þŒ¬∂»
B£Æ‘ˆ¥ÛCO2≈®∂»
C£Æ π”√¥þªØº¡
¢⁄»Áπ˚‘⁄t3 ±¥”ªÏ∫œŒÔ÷–∑÷¿Î≥ˆ≤ø∑÷CO£¨t4°´t5 ±º‰∂Œ∑¥”¶¥¶”⁄–¬µƒ∆Ω∫‚◊¥Ã¨£¨«Î‘⁄Õº…œ
ª≠≥ˆt3°´t5µƒ¶‘£®ƒÊ£©±‰ªØ«˙œþ°£
(13∑÷)¢Ò.(1)∑¥”¶I2+2S2O32°™=2I°™+S4O62°™≥£”√”⁄æ´—Œ÷–µ‚∫¨¡ø≤‚∂®°£ƒ≥Õ¨—ß¿˚”√∏√∑¥”¶ÃΩæø≈®∂»∂‘∑¥”¶ÀŸ¬ µƒ”∞œÏ°£ µ—È ±æ˘º”»Î1mLµÌ∑€»Ð“∫◊ˆ÷∏ 溡£¨»Ù≤ªæ≠º∆À„£¨÷±Ω”Õ®π˝Õ …´ ±º‰µƒ≥§∂Ã≈–∂œ≈®∂»”Î∑¥”¶ÀŸ¬ µƒπÿœµ£¨œ¬¡– ‘º¡÷–”¶—°‘Ò______(ÃÓ–Ú∫≈)°£
¢Ÿ1mL 0.01 mol?L°™1µƒµ‚ÀÆ ¢⁄1mL 0.001 mol?L°™1µƒµ‚ÀÆ
¢€4mL 0.01 mol?L°™1µƒNa2S2O3»Ð“∫ ¢Ð4mL 0.001 mol?L°™1µƒNa2S2O3»Ð“∫
(2)»Ùƒ≥Õ¨—ß—°»°¢Ÿ¢€Ω¯–– µ—È£¨≤‚µ√Õ …´ ±º‰Œ™4s,º∆À„v(S2O32°™)=_______________°£
¢Ú.∫œ≥…∞±À˘–˵ƒ«‚∆¯ø…”√√∫∫ÕÀÆ◊˜‘≠¡œæ≠∂ý≤Ω∑¥”¶÷∆µ√£¨∆‰÷–µƒ“ª≤Ω∑¥”¶Œ™£∫CO(g)£´H2O(g) 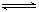 CO2(g)£´H2(g) ¶§H <0,200°Ê ±£¨∏√∑¥”¶µƒ∆Ω∫‚≥£ ˝Œ™1/2.25,∏√Œ¬∂»œ¬£¨Ω´“ª∂®¡øµƒCO∫ÕH2Õ∂»Îƒ≥10L√б’»ð∆˜£¨5min ±¥Ô∆Ω∫‚£¨∏˜ŒÔ÷ ≈®∂»(mol?L°™1)±‰ªØ»Áœ¬£∫
CO2(g)£´H2(g) ¶§H <0,200°Ê ±£¨∏√∑¥”¶µƒ∆Ω∫‚≥£ ˝Œ™1/2.25,∏√Œ¬∂»œ¬£¨Ω´“ª∂®¡øµƒCO∫ÕH2Õ∂»Îƒ≥10L√б’»ð∆˜£¨5min ±¥Ô∆Ω∫‚£¨∏˜ŒÔ÷ ≈®∂»(mol?L°™1)±‰ªØ»Áœ¬£∫
| | 0min | 5min | 10min |
| CO | 0.01 | | 0.0056 |
| H2O | 0.01 | | 0.0156 |
| CO2 | 0 | | 0.0044 |
| H2 | 0 | | 0.0044 |
”–ø…ƒÊ∑¥”¶£∫Fe£®s£©£´CO2£®g£©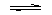 FeO£®s£©£´CO£®g£©°£“—÷™938K ±∆Ω∫‚≥£ ˝K£Ω1£Æ47£¨1173K ±∆Ω∫‚≥£ ˝K£Ω2£Æ15°£
FeO£®s£©£´CO£®g£©°£“—÷™938K ±∆Ω∫‚≥£ ˝K£Ω1£Æ47£¨1173K ±∆Ω∫‚≥£ ˝K£Ω2£Æ15°£
£®1£©∏√∑¥”¶µƒ∆Ω∫‚≥£ ˝±Ì¥Ô Ω____________________£¨ «____________£®ÃÓ°∞Œ¸»»°±ªÚ°∞∑≈»»°±£©∑¥”¶°£
£®2£©»Ù∏√∑¥”¶‘⁄ê˝∫„∂®µƒ√б’»ð∆˜÷–Ω¯––£¨‘⁄“ª∂®Ãıº˛œ¬¥ÔµΩ∆Ω∫‚◊¥Ã¨£¨»Áπ˚∏ƒ±‰œ¬¡–Ãıº˛£¨∑¥”¶ªÏ∫œ∆¯Ãµƒ∆Ωæ˘œý∂‘∑÷◊”÷ ¡ø»Á∫Œ±‰ªØ£®ÃÓ°∞‘ˆ¥Û°±°¢°∞ºı–°°±ªÚ°∞≤ª±‰°±£©°£
¢Ÿ…˝∏þŒ¬∂»_________________£ª¢⁄‘ŸÕ®»ÎCO__________________°£
£®3£©∏√∑¥”¶µƒƒÊ∑¥”¶ÀŸ¬ ÀÊ ±º‰±‰ªØµƒπÿœµ»ÁÕº£∫
 ¢Ÿ¥”Õº÷–ø…“‘ø¥≥ˆ£¨∑¥”¶t2 ±¥ÔµΩ∆Ω∫‚£¨‘⁄
¢Ÿ¥”Õº÷–ø…“‘ø¥≥ˆ£¨∑¥”¶t2 ±¥ÔµΩ∆Ω∫‚£¨‘⁄
t1 ±∏ƒ±‰ƒ≥÷÷Ãıº˛£¨∏√Ãıº˛ø…ƒÐ «_______°£
A£Æ…˝∏þŒ¬∂»
B£Æ‘ˆ¥ÛCO2≈®∂»
C£Æ π”√¥þªØº¡
¢⁄»Áπ˚‘⁄t3 ±¥”ªÏ∫œŒÔ÷–∑÷¿Î≥ˆ≤ø∑÷CO£¨t4°´t5 ±º‰∂Œ∑¥”¶¥¶”⁄–¬µƒ∆Ω∫‚◊¥Ã¨£¨«Î‘⁄Õº…œ
ª≠≥ˆt3°´t5µƒ¶‘£®ƒÊ£©±‰ªØ«˙œþ°£
(13∑÷)¢Ò.(1)∑¥”¶I2+2S2O32°™=2I°™+S4O62°™≥£”√”⁄æ´—Œ÷–µ‚∫¨¡ø≤‚∂®°£ƒ≥Õ¨—ß¿˚”√∏√∑¥”¶ÃΩæø≈®∂»∂‘∑¥”¶ÀŸ¬ µƒ”∞œÏ°£ µ—È ±æ˘º”»Î1mLµÌ∑€»Ð“∫◊ˆ÷∏ 溡£¨»Ù≤ªæ≠º∆À„£¨÷±Ω”Õ®π˝Õ …´ ±º‰µƒ≥§∂Ã≈–∂œ≈®∂»”Î∑¥”¶ÀŸ¬ µƒπÿœµ£¨œ¬¡– ‘º¡÷–”¶—°‘Ò______(ÃÓ–Ú∫≈)°£
¢Ÿ1mL 0.01 mol•L°™1µƒµ‚ÀÆ ¢⁄1mL 0.001 mol•L°™1µƒµ‚ÀÆ
¢€4mL 0.01 mol•L°™1µƒNa2S2O3»Ð“∫ ¢Ð4mL 0.001 mol•L°™1µƒNa2S2O3»Ð“∫
(2)»Ùƒ≥Õ¨—ß—°»°¢Ÿ¢€Ω¯–– µ—È£¨≤‚µ√Õ …´ ±º‰Œ™4s,º∆À„v(S2O32°™)=_______________°£
¢Ú.∫œ≥…∞±À˘–˵ƒ«‚∆¯ø…”√√∫∫ÕÀÆ◊˜‘≠¡œæ≠∂ý≤Ω∑¥”¶÷∆µ√£¨∆‰÷–µƒ“ª≤Ω∑¥”¶Œ™£∫CO(g)£´H2O(g)  CO2(g)£´H2(g) ¶§H <0,200°Ê ±£¨∏√∑¥”¶µƒ∆Ω∫‚≥£ ˝Œ™1/2.25,∏√Œ¬∂»œ¬£¨Ω´“ª∂®¡øµƒCO∫ÕH2Õ∂»Îƒ≥10L√б’»ð∆˜£¨5min ±¥Ô∆Ω∫‚£¨∏˜ŒÔ÷ ≈®∂»(mol•L°™1)±‰ªØ»Áœ¬£∫
CO2(g)£´H2(g) ¶§H <0,200°Ê ±£¨∏√∑¥”¶µƒ∆Ω∫‚≥£ ˝Œ™1/2.25,∏√Œ¬∂»œ¬£¨Ω´“ª∂®¡øµƒCO∫ÕH2Õ∂»Îƒ≥10L√б’»ð∆˜£¨5min ±¥Ô∆Ω∫‚£¨∏˜ŒÔ÷ ≈®∂»(mol•L°™1)±‰ªØ»Áœ¬£∫
|
|
0min |
5min |
10min |
|
CO |
0.01 |
|
0.0056 |
|
H2O |
0.01 |
|
0.0156 |
|
CO2 |
0 |
|
0.0044 |
|
H2 |
0 |
|
0.0044 |
(1) «Î∑÷±º∆À„CO°¢H2O°¢CO2°¢H2µƒ∆Ω∫‚≈®∂»__________,_________,________,_______°£
(2)COµƒ∆Ω∫‚◊™ªØ¬ Œ™____________,”˚÷∏þCOµƒ◊™ªØ¬ £¨œ¬¡–¥Î ©÷–ø…––µƒ «_____(ÃÓ–Ú∫≈)°£
a£Æ‘ˆº”—π«ø b£ÆΩµµÕŒ¬∂»
c£Æê˝≤ª±‰£¨‘Ÿ≥‰»ÎCO d£Æ∏¸ªª¥þªØº¡
e£Æê˝≤ª±‰£¨‘Ÿ≥‰»Î0.1molH2O
(3) »Ù5min°´10min÷ª∏ƒ±‰¡Àƒ≥“ªÃıº˛£¨∏√Ãıº˛ «__________,»Á∫Œ∏ƒ±‰µƒ___________°£
”–ø…ƒÊ∑¥”¶£∫Fe£®s£©£´CO2£®g£© FeO£®s£©£´CO£®g£©°£“—÷™938K ±∆Ω∫‚≥£ ˝K£Ω1£Æ47£¨1173K ±∆Ω∫‚≥£ ˝K£Ω2£Æ15°£
FeO£®s£©£´CO£®g£©°£“—÷™938K ±∆Ω∫‚≥£ ˝K£Ω1£Æ47£¨1173K ±∆Ω∫‚≥£ ˝K£Ω2£Æ15°£
£®1£©∏√∑¥”¶µƒ∆Ω∫‚≥£ ˝±Ì¥Ô Ω____________________£¨ «____________£®ÃÓ°∞Œ¸»»°±ªÚ°∞∑≈»»°±£©∑¥”¶°£
£®2£©»Ù∏√∑¥”¶‘⁄ê˝∫„∂®µƒ√б’»ð∆˜÷–Ω¯––£¨‘⁄“ª∂®Ãıº˛œ¬¥ÔµΩ∆Ω∫‚◊¥Ã¨£¨»Áπ˚∏ƒ±‰œ¬¡–Ãıº˛£¨∑¥”¶ªÏ∫œ∆¯Ãµƒ∆Ωæ˘œý∂‘∑÷◊”÷ ¡ø»Á∫Œ±‰ªØ£®ÃÓ°∞‘ˆ¥Û°±°¢°∞ºı–°°±ªÚ°∞≤ª±‰°±£©°£
¢Ÿ…˝∏þŒ¬∂»_________________£ª¢⁄‘ŸÕ®»ÎCO__________________°£
£®3£©∏√∑¥”¶µƒƒÊ∑¥”¶ÀŸ¬ ÀÊ ±º‰±‰ªØµƒπÿœµ»ÁÕº£∫

¢Ÿ¥”Õº÷–ø…“‘ø¥≥ˆ£¨∑¥”¶t2 ±¥ÔµΩ∆Ω∫‚£¨‘⁄
t1 ±∏ƒ±‰ƒ≥÷÷Ãıº˛£¨∏√Ãıº˛ø…ƒÐ «_______°£
A£Æ…˝∏þŒ¬∂»
B£Æ‘ˆ¥ÛCO2≈®∂»
C£Æ π”√¥þªØº¡
¢⁄»Áπ˚‘⁄t3 ±¥”ªÏ∫œŒÔ÷–∑÷¿Î≥ˆ≤ø∑÷CO£¨t4°´t5 ±º‰∂Œ∑¥”¶¥¶”⁄–¬µƒ∆Ω∫‚◊¥Ã¨£¨«Î‘⁄Õº…œ
ª≠≥ˆt3°´t5µƒ¶‘£®ƒÊ£©±‰ªØ«˙œþ°£
π˙º —ß–£”≈—° - ¡∑œ∞≤·¡–±Ì - ‘¡–±Ì
∫˛±± °ª•¡™Õ¯Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®∆Ωî | Õ¯…œ”–∫¶–≈œ¢æŸ±®◊®«¯ | µÁ–≈’©∆≠柱®◊®«¯ | …Ê¿˙ ∑–ÈŒÞ÷˜“”–∫¶–≈œ¢æŸ±®◊®«¯ | …Ê∆Û«÷»®æŸ±®◊®«¯
Œ•∑®∫Õ≤ª¡º–≈œ¢æŸ±®µÁª∞£∫027-86699610 柱®” œ‰£∫58377363@163.com