
МвДҝБРұн(°ьАЁҙр°ёәНҪвОц)
 mol-1
mol-1 mol-1
mol-1 mol-1
mol-1 ТСЦӘЈәCO(g)Ј«H2O(g)![]() H2(g)Ј«CO2(g)ЖҪәвіЈКэЛжОВ¶ИөДұд»ҜИзПВұнЈә
H2(g)Ј«CO2(g)ЖҪәвіЈКэЛжОВ¶ИөДұд»ҜИзПВұнЈә
![]()
(1)ЙПКцХэПт·ҙУҰКЗЈә________·ҙУҰ(МоЎ°·ЕИИЎұ»тЎ°ОьИИЎұ)
(2)ФЪ800Ўж·ўЙъЙПКц·ҙУҰЈ¬ТФұнЦРөДОпЦКөДБҝН¶ИләгИЭ·ҙУҰЖчЈ¬ЖдЦРПтХэ·ҙУҰ·ҪПтТЖ¶ҜөДУР________(СЎМоAЎўBЎўCЎўDЎўE)Ј®

КФ»ШҙрПВБРОКМв
(3)ТСЦӘФЪТ»¶ЁОВ¶ИПВЈ¬C(s)Ј«CO2(g)![]() 2CO(g)ЖҪәвіЈКэKЈ»
2CO(g)ЖҪәвіЈКэKЈ»
C(s)Ј«H2O(g)![]() CO(g)Ј«H2(g)ЖҪәвіЈКэK1Ј»
CO(g)Ј«H2(g)ЖҪәвіЈКэK1Ј»
CO(g)Ј«H2O(g)![]() H2(g)Ј«CO2(g)ЖҪәвіЈКэK2
H2(g)Ј«CO2(g)ЖҪәвіЈКэK2
ФтKЎўK1ЎўK2Ц®јдөД№ШПөКЗЈә________Ј®
(4)ИфФЪ500ЎжКұҪшРРЈ¬ЙиЖрКјКұCOәНH2OөДЖрКјЕЁ¶ИҫщОӘ0.020 mol/LЈ¬ФЪёГМхјюПВЈ¬COөДЖҪәвЧӘ»ҜВКОӘЈә________Ј®
(5)Иф·ҙУҰФЪ800ЎжҪшРРЈ¬ЙиЖрКјКұCOәНH2O(g)№ІОӘ5 molЈ¬Л®ХфЖшөДМе»э·ЦКэОӘxЈ»ЖҪәвКұCOЧӘ»ҜВКОӘyЈ¬ФтyЛжxұд»ҜөДәҜКэ№ШПөКҪОӘЈәyЈҪ________Ј®
(6)ФЪVLГЬұХИЭЖчЦРНЁИл10 molЎЎCOәН10 molЛ®ХфЖшЈ¬ФЪTЎжҙпөҪЖҪәвЈ¬И»әујұЛЩНЁ№эјоКҜ»ТЈ¬Ҫ«ЛщөГ»мәПЖшМеИјЙХЈ¬ІвөГ·ЕіцөДИИБҝОӘ2842 kJ(ТСЦӘCOИјЙХОӘ283 kJ/molЈ¬H2ИјЙХИИОӘ286/kJmol)Ј¬ФтTЎжЖҪәвіЈКэKЈҪ________Ј®
 ОпЦКAЎўBЎўCУРИзНј1ЧӘ»Ҝ№ШПөЈә
ОпЦКAЎўBЎўCУРИзНј1ЧӘ»Ҝ№ШПөЈәЈЁ15·ЦЈ©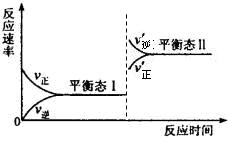
ОпЦКAЎўBЎўCУРИзПВЧӘ»Ҝ№ШПөЈә
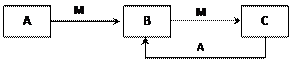 |
 6H2O+5N2ЎЈФЪТ»¶ЁМхјюПВЈ¬ёГ·ҙУҰҙпөҪЖҪәвМ¬IәуЈ¬ЙэёЯОВ¶ИЖҪәв·ўЙъТЖ¶ҜЈ¬ҙпөҪЖҪәвМ¬IIөД·ҙУҰЛЩВКЛжКұјдұд»ҜөД№ШПөНјИзУТЎЈёГ·ҙУҰОӘ ЎЎЎЎ ЈЁМоЎ°ОьИИЎұ»тЎ°·ЕИИЎұЈ©·ҙУҰЈ»ЙэёЯОВ¶ИЈ¬ёГ·ҙУҰөДЖҪәвіЈКэKЦөЎЎЎЎЎЎЎЎЎЎЈЁМоЎ°ФцҙуЎұЎўЎ°јхРЎЎұ»тЎ°І»ұдЎұЈ©
6H2O+5N2ЎЈФЪТ»¶ЁМхјюПВЈ¬ёГ·ҙУҰҙпөҪЖҪәвМ¬IәуЈ¬ЙэёЯОВ¶ИЖҪәв·ўЙъТЖ¶ҜЈ¬ҙпөҪЖҪәвМ¬IIөД·ҙУҰЛЩВКЛжКұјдұд»ҜөД№ШПөНјИзУТЎЈёГ·ҙУҰОӘ ЎЎЎЎ ЈЁМоЎ°ОьИИЎұ»тЎ°·ЕИИЎұЈ©·ҙУҰЈ»ЙэёЯОВ¶ИЈ¬ёГ·ҙУҰөДЖҪәвіЈКэKЦөЎЎЎЎЎЎЎЎЎЎЈЁМоЎ°ФцҙуЎұЎўЎ°јхРЎЎұ»тЎ°І»ұдЎұЈ©өЪIҫнЈЁұШЧцЈ¬№І88·ЦЈ©
Т»ЎўСЎФсМвЈЁұҫМв°ьАЁ15РЎМвЈ¬ГҝРЎМв4·ЦЈ¬№І60·ЦЈ©
1ЁD5 CDCBB 6ЁD10 ACBAC 11ЁD15 CCBDD
¶юЎўСЎФсМвЈЁұҫМв°ьАЁ7РЎМвЈ¬ГҝРЎМвёшіцөДЛДёцСЎПоЦРЈ¬УРөДЦ»УРТ»ёцСЎПоХэИ·Ј¬УРөДУР¶аёцСЎПоХэИ·Ј¬И«СЎ¶ФөДөГ4·ЦЈ¬СЎ¶Фө«І»И«өДөГ2·ЦЈ¬УРСЎҙнөДөГ0·ЦЈ©
16Ј®C 17Ј®B 18Ј®AB 19Ј®A 20Ј®D 21Ј®BC 22Ј®AD
өЪIIҫнЈЁұШЧц120·Ц+СЎЧц32·ЦЈ¬№І152·ЦЈ©
[ұШЧцІҝ·Ц]
 23Ј®ЈЁ12·ЦЈ©
23Ј®ЈЁ12·ЦЈ©
ЈЁ1Ј©НјПЯИзНјЛщКҫЈ¬9.4~9.6
ЈЁ2Ј©УЙ өГЈә
өГЈә УЙҙЛҝЙЦӘЈ¬
УЙҙЛҝЙЦӘЈ¬
НјПЯІ»№эФӯөгЈ¬Ц»УРөұ әЬҙуКұЈ¬ІЕҪьЛЖУР
әЬҙуКұЈ¬ІЕҪьЛЖУР
 Ј¬ұҫКөСйҙпІ»өҪХвТ»МхјюЈ¬№КНјПЯІ»№эФӯөгЎЈ
Ј¬ұҫКөСйҙпІ»өҪХвТ»МхјюЈ¬№КНјПЯІ»№эФӯөгЎЈ
ЈЁ3Ј©0.033 0.032
24Ј®ЈЁ15·ЦЈ©
ҪвЈәЈЁ1Ј©іөНЈЦ№ФЛ¶ҜәуИЎРЎОпҝйОӘСРҫҝ¶ФПуГнЖдөҪҙпіөУТ¶ЛКұөДЛЩ¶ИОӘv1Ј¬
УЙ¶ҜДЬ¶ЁАнөГ ўЩ
ўЩ
ҪвөГЈә ўЪ
ўЪ
ёХҪшИлФІ№мөАКұЈ¬ЙиОпҝйКЬөҪөДЦ§іЦБҰОӘNЈ¬УЙЕЈ¶ЩөЪ¶ю¶ЁВЙөГЈә
 ўЫ
ўЫ
УЙЕЈ¶ЩөЪИэ¶ЁВЙ ўЬ
ўЬ
УЙўЩўЫўЬөГ Ј¬·ҪПтКъЦұПтПВЎЈ ўЭ
Ј¬·ҪПтКъЦұПтПВЎЈ ўЭ
ЈЁ2Ј©ИфРЎОпҝйДЬөҪҙпФІ№мөАЧоёЯөгЈ¬ФтУЙ»ъРөДЬКШәгЈә
 ўЮ
ўЮ
ҪвөГЈә ўЯ
ўЯ
ЗЎДЬ№эЧоёЯөгөДЛЩ¶ИОӘv3
 ўа
ўа
Тт Ј¬№КРЎОпҝйҙУФІ№мөАЧоёЯөгЧцЖҪЕЧФЛ¶ҜЈ¬
Ј¬№КРЎОпҝйҙУФІ№мөАЧоёЯөгЧцЖҪЕЧФЛ¶ҜЈ¬
 ўб
ўб
 ўв
ўв
УЙўЯўбўвБӘБўҪвөГx=
№КРЎОпҝйҫаіөЧу¶Л ЈЁ11Ј©
ЈЁ11Ј©
ЖА·ЦұкЧјЈәўЩўЫўЮўбГҝКҪ2·ЦЈ¬ЖдУаГҝКҪ1·ЦЎЈ
25Ј®ЈЁ18·ЦЈ©
ҪвЈәЈЁ1Ј©ИЎөјМеҝтОӘСРҫҝ¶ФПуЈ¬ҙУt0КұҝМҝӘКјАӯБҰәг¶ЁЈ¬№КөзВ·ЦРөзБчәг¶ЁЈ¬ЙиabұЯЦРөзБчОӘI1Ј¬cdұЯЦРөзБчОӘI2Ј¬
УЙКЬБҰЖҪәвЈә ўЩ
ўЩ
 ўЪ
ўЪ
 ўЫ
ўЫ
ҪвөГЈә ўЬ
ўЬ
ЈЁ2Ј©ЙиЧЬөзБчОӘIЈ¬УЙұХәПВ·Е·Д·¶ЁВЙЈә ўЭ
ўЭ
 ўЮ
ўЮ
 ўЯ
ўЯ
I1+I2=I ўа
¶ш
ҪвөГЈә ўб
ўб
ЈЁ3Ј©УЙөз¶Ҝ»ъөДЗЈТэ№ҰВКәг¶Ё
P=F?v ўв
¶ФөјМе°фЈә ЈЁ11Ј©
ЈЁ11Ј©
УЙТФЙПёчКҪБӘБўҪвөГЈә ЈЁ12Ј©
ЈЁ12Ј©
ЖА·ЦұкЧјЈәўЩўЭўбўвЈЁ11Ј©ЈЁ12Ј©ГҝКҪ2·ЦЈ¬ЖдУаГҝКҪ1·ЦЎЈ
 26Ј®ЈЁ16·ЦЈ¬іэЧўГчНвЈ¬ГҝҝХ2·ЦЈ©
26Ј®ЈЁ16·ЦЈ¬іэЧўГчНвЈ¬ГҝҝХ2·ЦЈ©



ЈЁ1Ј©»щТт
ЈЁ2Ј©BbXAXa
BbXAY
ЈЁ3Ј©1/4
ЈЁ4Ј©КөСйјЩЙиЈәЗЧҙъҙЖКуЙъЦіПё°ыЦРXИҫЙ«МеЙПөД»щТтіцПЦБЛТюРФН»ұдЈЁ»тҙЖКуХэіЈОІРФЧҙКЗУЙ»·ҫіТэЖрөДЈ©
КөСйЛјВ·ЈәСЎФсёГХэіЈОІҙЖКуУлНдЗъОІРЫКуФУҪ»ЈЁ»тХЯУлХэіЈОІРЫКуФУҪ»Ј©Ј¬№ЫІмәуҙъХэіЈОІәННдЗъОІіцПЦөДұИАэЎЈ
ФӨЖЪҪб№ыЈәИфәуҙъҙЖРФ¶јКЗНдЗъОІЈ¬РЫРФ¶јКЗХэіЈОІЈ¬ФтЦӨГчКЗЗЧҙъҙЖКуЙъЦіПё°ыЦРXИҫЙ«МеЙПөД»щТтіцПЦБЛТюРФН»ұдЈ»ИфәуҙъИ«КЗНдЗъОІ»тХЯЦ»УРРЫРФіцПЦХэіЈОІЈ¬ҙЖРФ¶јКЗНдЗъОІЈ¬ФтЦӨГчҙЖКуХэіЈОІРФЧҙКЗУЙ»·ҫіТэЖрөДЎЈЈЁ»тХЯИфәуҙъ¶јКЗХэіЈОІЈ¬ФтЦӨГчКЗЗЧҙъҙЖКуЙъЦіПё°ыЦРXИҫЙ«МеЙПөД»щТтіцПЦБЛТюРФН»ұдЈ»ИфәуҙъҙЖРЫИ«КЗНдЗъОІ»тҙЖРЫЦРХэіЈОІЎўНдЗъОІ¶јУРЈ¬ФтЦӨГчҙЖКуХэіЈОІРФЧҙКЗУЙ»·ҫіТэЖрөДЈ©ЈЁ4·ЦЈ©
27Ј®ЈЁ17·ЦЈ¬іэЧўГчНвЈ¬ГҝҝХ2·ЦЈ©
ЈЁ1Ј©№в·ҙУҰЛЩ¶ИұИ°ө·ҙУҰҝм
ЈЁ2Ј©ПВҪө ЙПЙэ
ЈЁ3Ј©№в·ҙУҰКН·ЕO2өДЛЩВКөИУЪ°ө·ҙУҰОьКХCO2өДЛЩВК >
ЈЁ4Ј©ўЩЧиЦ№УР»ъОпҪшіцТ¶Ж¬ ўЪәфОьЧчУГПыәДУР»ъОпөДЛЩВК
ўЫЙъІъЛЩВК ЈЁ3·ЦЈ©
ЈЁ3·ЦЈ©
|