
题目列表(包括答案和解析)
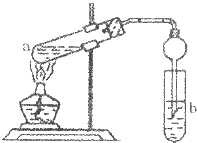 “酒是陈年的香”是因为酒在储存中会生成有香味的乙酸乙酯.在实验室我们可以用如图所示装置来制取乙酸乙酯:在试管a中先加入3mL的无水乙醇和2mL浓硫酸混合液,冷却后再加入2mL冰醋酸,混合均匀后将试管固定在铁架台上,在试管b中加入7mL饱和碳酸钠溶液.装置连接好后,用酒精灯对试管a加热,当试管b中收集到较多的乙酸乙酯时停止实验.请回答下列问题:
“酒是陈年的香”是因为酒在储存中会生成有香味的乙酸乙酯.在实验室我们可以用如图所示装置来制取乙酸乙酯:在试管a中先加入3mL的无水乙醇和2mL浓硫酸混合液,冷却后再加入2mL冰醋酸,混合均匀后将试管固定在铁架台上,在试管b中加入7mL饱和碳酸钠溶液.装置连接好后,用酒精灯对试管a加热,当试管b中收集到较多的乙酸乙酯时停止实验.请回答下列问题: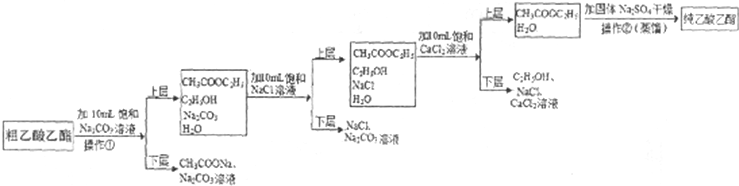
请回答下列问题:?
(1)铁屑表面少量的铁锈(主要成分为Fe2O3·aH2O)对制取硫酸亚铁有无影响 (填“有”或“无”)。其原因是: 。如有影响将如何操作? (若无影响,此问可以不答)。
(2)FeSO4在不同温度下的溶解度如下表所示:
温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
溶解度/g | 18.5 | 20.8 | 26.3 | 32.8 | 40.1 | 48.4 | 52.4 | 50.9 | 43.7 |
由于废铁屑含有C、Si等杂质,为了使FeSO4溶液的浓度增大,便于反应后分离溶液和残渣,该小组实验时采取了水浴加热和趁热过滤的方法。这样做的主要目的是为了防止 。你认为实验时的水浴温度最好控制在 ℃?左右。??
(3)测定晶体中结晶水含量所用的实验仪器除托盘天平(或物理天平)、研钵、坩埚、坩埚钳、三脚架、泥三角、酒精灯、药匙外,还有 ;判断晶体中结晶水完全失去的实验操作是 。?
(4)计算硫酸亚铁晶体化学式中x的实验值表达式为x= ?。(已知:硫酸亚铁晶体中结晶水的质量为m g、硫酸亚铁晶体的质量为w g)?
(5)由于铁屑或铁丝与硫酸反应速率慢,实验过程中有的同学提出采用电解的方法,可以加快制取FeSO4溶液的反应速率,该方法的电解质溶液是 ,阳极的电极反应方程式为: 。?
请你再写出一种(不包括改变温度和硫酸的浓度)以铁单质为反应物,能加快制取FeSO4溶液反应速率的方法: 。?


“酒是陈年的香”是因为酒在储存中会生成有香味的乙酸乙酯。在实验室我们可以用下图所示装置来制取乙酸乙酯:在试管a中先加入3mL的无水乙醇和2mL浓硫酸混合液,冷却后再加入2mL冰醋酸,混合均匀后将试管固定在铁架台上,在试管b中加入7mL饱和碳酸钠溶液。装置连接好后,用酒精灯对试管a加热,当试管b中收集到较多的乙酸乙酯时停止实验。请回答下列问题:

(1)在试管a中混合乙醇和浓硫酸的操作是__________;
(2)在实验中球形干燥管除导气、冷凝作用外,另一个重要作用是__________;
(3)b试管中选择饱和Na2CO3溶液而不选用饱和氢氧化钠溶液的原因是__________; (用化学方程式说明)
(4)生成乙酸乙酯的反应比较缓慢,为了提高该反应的速率,本实验中采用的措施是__________、__________;
(5)上述b试管得到的乙酸乙酯含有很多杂质(粗乙酸乙酯),必须进行提纯才能得到纯乙酸乙酯,其流程如下:

①操作①的名称__________,进行操作②时需要将混合液转移到__________仪器中。
②加10mLCaCl2溶液洗涤乙酸乙酯时,要先加饱和NaCl溶液洗涤的原因是__________。
| A、用作“钡餐”的物质主要成分是硫酸钡 | B、采用催化设施,将汽车尾气中CO和NO转化为无害气体 | C、常温下,可以用铁制容器来盛装冷的浓硫酸 | D、S02具有氧化性,可用于漂白纸浆 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com