
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
ЃЈ12ЗжЃЉВщдФгаЙиТШЛЏТСЕФвЛаЉзЪСЯЃЌЕУЕНШчЯТвЛаЉаХЯЂЃКЂйНЋТШЛЏТСМгШШЃЌдк180ЁцЪБПЊЪМЩ§ЛЊЃЛЂкдк2.02ЁС105PaЬѕМўЯТЃЌТШЛЏТСЕФШлЕуЮЊ190ЁцЃЛЂлдк500KКЭ1.01ЁС105PaЪБЃЌЫќЕФеєЦјУмЖШ(ЛЛЫуГЩБъзМзДПіЪБ)ЮЊ11.92g/LЃЛЂмТШЛЏТСЕФНсЙЙжаКЌгаХфЮЛМќЁЃ
ЧыЛиД№ЯТСаЮЪЬтЃК
ЃЈ1ЃЉЧыФуОЭТШЛЏТСЪЧЁАРызгЛЏКЯЮяЁБЛЙЪЧЁАЙВМлЛЏКЯЮяЁБЬсГівЛжжВТЯыЃЌВЂаДГівЛЬѕВТЯыЕФРэгЩЁЃФуЕФВТЯыЪЧ ЃЌРэгЩЪЧ ЁЃ
ЃЈ2ЃЉЭЈЙ§МЦЫуШЗЖЈТШЛЏТСЕФЛЏбЇЪНЮЊ ЃЌНсЙЙЪНЮЊ ЁЃ
ЃЈ3ЃЉгУЮоЫЎТШЛЏТСНјааЪЕбщЪБЃЌЗЂЯжЫќдкГБЪЊПеЦјжаЧПСвЕиЁАЗЂбЬЁБЁЃНјвЛВНВщдФзЪБэУїЃЌЦфдвђЪЧТШЛЏТСгыПеЦјжаЕФЫЎЗЂЩњСЫИДЗжНтЗДгІЁЃЧыаДГіЗДгІЕФЛЏбЇЗНГЬЪН ЁЃ
ЃЈ4ЃЉЧыФуЩшМЦвЛЪЕбщЗНАИЃЌжЄУїТШЛЏТСЪЧЁАРызгЛЏКЯЮяЁБЛЙЪЧЁАЙВМлЛЏКЯЮяЁБЁЃаДГіЪЕбщФкШнЁЂЯжЯѓКЭНсТл ЁЃ
ВщдФгаЙиТШЛЏТСЕФвЛаЉзЪСЯЃЌЕУЕНШчЯТвЛаЉаХЯЂЃКЂйНЋТШЛЏТСМгШШЃЌдк180ЁцЪБПЊЪМЩ§ЛЊЃЛЂкдк2.02ЁС105PaЬѕМўЯТЃЌТШЛЏТСЕФШлЕуЮЊ190ЁцЃЛЂлдк500KКЭ1.01ЁС105PaЪБЃЌЫќЕФеєЦјУмЖШ(ЛЛЫуГЩБъзМзДПіЪБ)ЮЊ11.92g/LЃЛЂмТШЛЏТСЕФНсЙЙжаКЌгаХфЮЛМќЁЃ
ЧыЛиД№ЯТСаЮЪЬтЃК
ЃЈ1ЃЉЧыФуОЭТШЛЏТСЪЧЁАРызгЛЏКЯЮяЁБЛЙЪЧЁАЙВМлЛЏКЯЮяЁБЬсГівЛжжВТЯыЃЌВЂаДГівЛЬѕВТЯыЕФРэгЩЁЃФуЕФВТЯыЪЧ ЃЌРэгЩЪЧ ЁЃ
ЃЈ2ЃЉЭЈЙ§МЦЫуШЗЖЈТШЛЏТСЕФЛЏбЇЪНЮЊ ЃЌНсЙЙЪНЮЊ ЁЃ
ЃЈ3ЃЉгУЮоЫЎТШЛЏТСНјааЪЕбщЪБЃЌЗЂЯжЫќдкГБЪЊПеЦјжаЧПСвЕиЁАЗЂбЬЁБЁЃНјвЛВНВщдФзЪБэУїЃЌЦфдвђЪЧТШЛЏТСгыПеЦјжаЕФЫЎЗЂЩњСЫИДЗжНтЗДгІЁЃЧыаДГіЗДгІЕФЛЏбЇЗНГЬЪН ЁЃ
ЃЈ4ЃЉЧыФуЩшМЦвЛЪЕбщЗНАИЃЌжЄУїТШЛЏТСЪЧЁАРызгЛЏКЯЮяЁБЛЙЪЧЁАЙВМлЛЏКЯЮяЁБЁЃаДГіЪЕбщФкШнЁЂЯжЯѓКЭНсТл ЁЃ
| дЊЫи | гаЙиаХЯЂ |
| A | зюИпМлбѕЛЏЮяЖдгІЕФЫЎЛЏЮягыЦфЧтЛЏЮяЗДгІЩњГЩРызгЛЏКЯЮя |
| B | ЕиПЧжаКЌСПзюЖрЕФдЊЫи |
| C | ЕЅжЪаыБЃДцдкУКгЭжаЃЌгыDаЮГЩЕФЛЏКЯЮяЪЧЩњЛюжазюГЃгУЕФЕїЮЖЦЗ |
| D | ЕЅжЪгыNaOHШмвКЗДгІПЩгУгкЩњВњЦЏАзвК |
| E | ЕЅжЪЪЧЩњЛюжагУСПзюДѓЕФН№ЪєЃЌЦфжЦЦЗдкГБЪЊПеЦјжавзБЛИЏЪДЛђЫ№ЛЕ |

| дЊЫи | гаЙиаХЯЂ |
| A | зюИпМлбѕЛЏЮяЖдгІЕФЫЎЛЏЮягыЦфЧтЛЏЮяЗДгІЩњГЩРызгЛЏКЯЮя |
| B | ЕиПЧжаКЌСПзюЖрЕФдЊЫи |
| C | ЕЅжЪаыБЃДцдкУКгЭжа |
| D | ЕЅжЪгыNaOHШмвКЗДгІПЩгУгкЩњВњЦЏАзвК |
| E | ЕЅжЪЪЧЩњЛюжагУСПзюДѓЕФН№ЪєЃЌЦфжЦЦЗдкГБЪЊПеЦјжавзБЛИЏЪДЛђЫ№ЛЕ |


 NH4++OH-
NH4++OH- NH4++OH-
NH4++OH-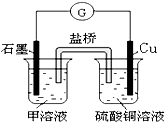
ЙњМЪбЇаЃгХбЁ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com