
题目列表(包括答案和解析)
硼及其化合物在耐髙温合金工业、催化剂制造、髙能燃料等方面应用广泛。
(1)氮化硼是一种耐高温材料,巳知相关反应的热化学方程式如下:
2B(s)+N2(g)= 2BN(s) ΔH=a kJ • mol-1
B2H6 (g)=2B(s) + 3H2 (g) ΔH =b kJ • mol-1
N2 (g) + 3H2
(g) 2NH3 (g) ΔH =c kJ• mol-1
2NH3 (g) ΔH =c kJ• mol-1
①反应B2H6(g)+2NH3(g)=2BN(s) +6H2(g) ΔH = (用含a、b、c 的代数式表示)kJ ·mol-1。
②B2H6是一种髙能燃料,写出其与Cl2反应生成两种氯化物的化学方程式: 。
(2)硼的一些化合物的独特性质日益受到人们的关注。
①最近美国化学家杰西·萨巴蒂尼发现由碳化硼制作的绿色焰火比传统焰火(硝酸钡)更安全,碳化硼中硼的质量分数为78. 6%,则碳化硼的化学式为 。
②近年来人们将LiBH4和LiNH2球磨化合可形成新的化合物 Li3BN2H8和Li4BN3 H10,Li3BN2H8球磨是按物质的量之比n(LiNH2) : n(LiBH4) = 2 : 1加热球磨形成的,反应过程中的X衍射图谱如图所示。

Li3BN2H8在大于250℃时分解的化学方程式为 ,Li3BN2H8与Li4BN3H10 的物质的量相同时,充分分解,放出等量的H2,Li4BN3 H10分解时还会产生固体Li2NH和另一种气体,该气体是 。
(3)直接硼氢化物燃料电池的原理如图,负极的电极反应式为 。电池总反应的离子方程式为 。


| OH- |
| H+ |
| OH- |
| H+ |
| ||
| ||
| ||
| ||
| ||
| ||
(14分)根据下列化合物:① NaCl ② NaOH ③ HCl ④ NH4Cl ⑤ CH3COONa ⑥CH3COOH ⑦ NH3•H2O ⑧H2O
请回答下列问题:
(1)NH4Cl溶液显 性,用离子方程式表示 ,其溶液中离子浓度大小顺序为 ;
(2)常温下,pH=11的CH3COONa溶液中,水电离出来的c(OH-)= ;在pH=3的CH3COOH 溶液中,水电离出来的c(H+)= ;
(3)已知水存在如下平衡:H2O+ H2OH3O++OH- △H>0,现欲使平衡向右移动,且所得溶液显酸性,选择方法是 。
A. 向水中加入NaHSO4固体 B. 向水中加Na2CO3固体
C. 加热至100℃[其中c(H+) = 1×10-6mol•L-1] D. 向水中加入 (NH4)2SO4固体
(4)若等浓度、等体积的②NaOH和⑦NH3•H2O分别加水稀释m倍、n倍,稀释后两种溶液的pH相等,则 m n (填 “<”、“>”或“=”)。
(5)除⑧H2O外,若其余7种溶液的物质的量浓度相同,则这7种溶液按pH由大到小的顺序为:____________________________________________________。
镁砂(MgO)是一种高温耐火材料。下图是氨法制取高纯镁砂的部分工艺流程:
请回答:
(1)MgCl2•6H2O溶于水,溶液呈 (填“酸性”、“中性”、或“碱性”)。
(2)蒸氨是将石灰乳通入氯化铵溶液中,并加热,写出该反应的化学方程式: 。
(3)轻烧后的产物为 。
(4)如何检验沉淀已洗涤干净的方法是 。
(5)氨化反应过程中反应的离子方程式为 。
(6)已知向Mg(OH)2沉淀中滴加氯化铵溶液可观察到沉淀溶解,试解释该反应发生的原理(用离子方程式表示和文字说明) 。
(10分)
海水是人类宝贵的自然资源,从海水中可以提取多种化工原料,下图是某工厂对海水资源综合利用的示意图:
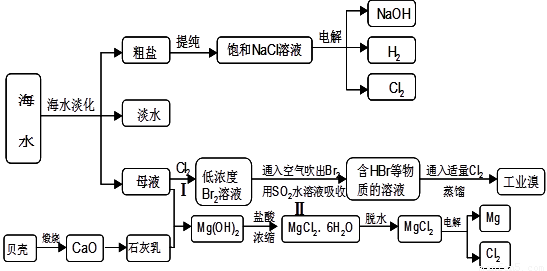
(1)请列举海水淡化的两种方法 、 。
(2)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br—,其目的是: 。
步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,有关反应的离子方程式
(3)在制取无水氯化镁时需要在干躁的HCl气流中加热MgCl2•6H2O,其原因用化学方程式表示为
(4)上述工艺中可以得到金属Mg,请写出工业上冶炼金属铝的化学方程式
。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com