
题目列表(包括答案和解析)
![]()
(1)A既能与NaOH溶液反应,又能与NaHCO3溶液反应,写出A和NaHCO3溶液反应的化学方程式:_____________________________________________________________________;
(2)有机物B在浓H2SO4存在下,相互作用生成一种环状酯(如图)。则有机物B的结构简式为______________________,等物质的量B与Na、NaOH、NaHCO3充分反应,消耗Na、NaOH、NaHCO3的物质的量之比为_________;
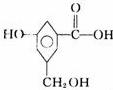
(3)D和B互为同分异构体,且D苯环上的一氯代物只两种,D不与NaHCO3反应,能与Na、NaOH反应,等质量的D消耗:Na、NaOH的物质的量之比为2:3则D的结构简式为(只写一种):
_____________________________________________________________;
(4)1 mol A、C完全燃烧,消耗O2的质量相等,且1 mol C能和1 mol Na完全反应,写出含碳的原子数最少的C的结构简式____________________。
(5)A是多官能团物质,从它所含的结构基团来看,A可以属于___________(填序号)。
①芳香烃 ②醇 ③酚 ④羧酸 ⑤酯

 (
( 或
或 )
) (
( 或
或 )
)




湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com