
题目列表(包括答案和解析)
某消毒液的主要成分为NaCl和NaClO,在空气中易吸收CO2而变质,且NaCl和NaClO在酸性条件下可发生反应:ClO- + Cl- + 2H+ = Cl2↑+ H2O。某学习小组拟探究该消毒液的变质情况。
(1)取适量消毒液放在试管中,加入足量一定浓度的硫酸,有气体放出。通过下列装置检验气体的成分可以判断消毒液是否变质。
学习小组研究后认为变质情况可能有三种:甲:部分变质;乙:未变质;丙: 。
为了验证可能为甲,请完成下列实验方案。限选试剂:
①98%的浓硫酸 ②1%的品红溶液 ③1.0 mol·L-1 的KI-淀粉溶液 ④1.0 mol·L-1 的NaOH溶液 ⑤澄清石灰水 ⑥饱和NaCl溶液

|
所加试剂 |
预期现象和结论 |
|
试管A中加足量 (填序号); 试管B中加1%品红溶液; 试管C中加 (填序号)。 |
若___ ___, 则甲成立。 |
(2)用滴定法测定消毒液中NaClO的浓度(滴定过程涉及的反应有:NaClO + Na2SO3 = NaCl + Na2SO4 ;2KMnO4 + 5Na2SO3+ 3H2SO4 = K2SO4 + 2MnSO4 + 5Na2SO4 + 3H2O)。实验步骤如下:
①量取25.00 mL消毒液放入锥形瓶中,加入过量的a mol·L-1 Na2SO3溶液v1 mL;
②在使用滴定管之前首先进行的操作是____;将b mol·L-1的酸性KMnO4溶液装入 中;滴定,KMnO4和剩余的Na2SO3发生反应。当溶液由无色变成浅红色,且保持半分钟内红色不褪时,停止滴定,记录数据。
③重复滴定操作2次,平均消耗酸性KMnO4溶液v2 mL。则消毒液中NaClO的浓度为 mol·L-1(用含a、b、v1、v2的代数式表示)。
工业上利用反应:CO(g)+H2O(g)  CO2(g)+H2(g);△H="Q" kJ·mol-1,制备H2 .已知该反应的平衡常数K与温度的关系如图所示。
CO2(g)+H2(g);△H="Q" kJ·mol-1,制备H2 .已知该反应的平衡常数K与温度的关系如图所示。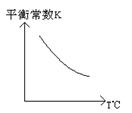
若在一容积固定的密 闭容器中,于850℃时发生上述反应,并测得容器内各物质的浓度(mol·L―1)随时间的变化关系如下表:
闭容器中,于850℃时发生上述反应,并测得容器内各物质的浓度(mol·L―1)随时间的变化关系如下表:
| t/min | CO(g) | H2O(g) | CO2(g) | H2(g) |
| 0 | 0.200 | 0.300 | 0 | 0 |
| 2 | 0.138 | 0.238 | 0.062 | 0.062 |
| 3 | c1 | c2 | c3 | c4 |
| 4 | c1 | c2 | c3 | c4 |
 位时间内减少CO(g)的浓度等于生成CO2(g)的浓度
位时间内减少CO(g)的浓度等于生成CO2(g)的浓度 __(填“增大”、“减小”或“不变”).
__(填“增大”、“减小”或“不变”). | 阳离子 | K+、Ag+、Mg2+、Ba2+ | ||||||||
| 阴离子 | NO
|
| 序号 | 实验内容 | 实验结果 |
| Ⅰ | 想该溶液中加入足量稀盐酸 | 生成白色沉淀并在标准状况下放出0.56L气体 |
| Ⅱ | 将Ⅰ中产生的混合液过滤,将沉淀洗涤、灼烧至恒重,称量所得固体的质量 | 固体质量为2.4g |
| Ⅲ | 向Ⅱ中所得的滤液中滴加BaCl2溶液 | 无明显现象 |
| 阴离子 | NO
|
CO
|
SiO
|
SO
| ||||||||
| c/mol?L-1 | ? ? |
0.25mol/L 0.25mol/L |
0.4mol/L 0.4mol/L |
0 0 |
| A、氧化性:A2>B2>C2>D2 | B、还原性:C->A->B->D- | C、反应2A-+D2→2D-+A2不能进行 | D、反应2C-+B2→2B-+C2不能进行 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com