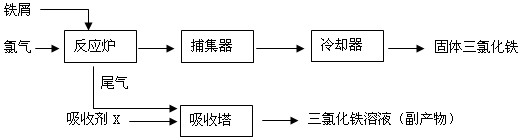
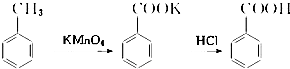(2010?南京二模)β-锂辉石的主要成分是Li
2O?Al
2O
3?4SiO
2,还含有FeO、CaO、MgO等.以β-锂辉石为原料制备碳酸锂的一种流程如下:
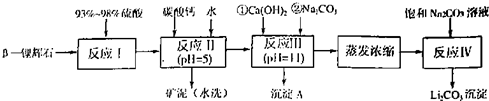
已知:①部分金属氢氧化物开始沉淀和完全沉淀的pH:
| 氢氧化物 |
Fe(OH)3 |
Al(OH)3 |
Mg(OH)2 |
| 开始沉淀pH |
2.7 |
3.7 |
9.6 |
| 完全沉淀pH |
3.7 |
4.7 |
11 |
②Li
2CO
3在不同温度的溶解度如下表:
| 温度/℃ |
0 |
10 |
20 |
50 |
75 |
100 |
| Li2CO3的溶解度/g |
1.539 |
1.406 |
1.329 |
1.181 |
0.866 |
0.728 |
回答下列问题:
(1)反应Ⅱ中加碳酸钙的作用是
除去反应Ⅰ中过量的硫酸,控制pH使Fe3+和Al3+完全沉淀
除去反应Ⅰ中过量的硫酸,控制pH使Fe3+和Al3+完全沉淀
.
(2)写出反应Ⅲ中生成沉淀A的离子方程式
Mg2++2OH-=Mg(OH)2↓
Mg2++2OH-=Mg(OH)2↓
、
Ca2++CO32-=CaCO3↓
Ca2++CO32-=CaCO3↓
.
(3)写出反应Ⅳ的化学方程式
Li2SO4+Na2CO3=Li2CO3↓+Na2SO4
Li2SO4+Na2CO3=Li2CO3↓+Na2SO4
.洗涤所得Li
2CO
3沉淀要用热水而非冷水,原因是
碳酸锂在较高的温度下溶解度小,用热水洗涤可以减少碳酸锂的损耗
碳酸锂在较高的温度下溶解度小,用热水洗涤可以减少碳酸锂的损耗
.

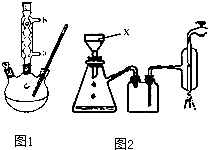 【实验化学】
【实验化学】