
题目列表(包括答案和解析)

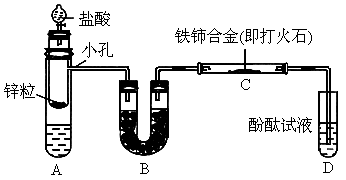
按图所示装置连接好仪器.
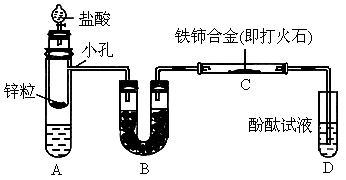
已知:A中装有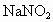 和
和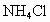 混合溶液,B中装有碱石灰,C中有铁铈合金,D中有酚酞试液.
混合溶液,B中装有碱石灰,C中有铁铈合金,D中有酚酞试液.
C中发生反应的热化学方程式为: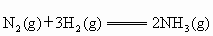 ;
;
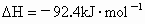
实验步骤如下:①检查装置的气密性;②用酒精灯加热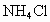 和
和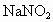 饱和溶液,待有气体生成,可停止加热,但仍有大量气体产生;③再用酒精灯给铁铈合金加热至一定温度;④从分液漏斗中滴入一定浓度盐酸,不久见酚酞试液变红.
饱和溶液,待有气体生成,可停止加热,但仍有大量气体产生;③再用酒精灯给铁铈合金加热至一定温度;④从分液漏斗中滴入一定浓度盐酸,不久见酚酞试液变红.
回答下列问题:
(1)写出A中两溶液间发生反应的化学方程式________,此反应为________热反应(填“放”或“吸”);
(2)先用酒精灯加热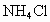 、
、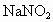 饱和溶液的目的是______________;
饱和溶液的目的是______________;
(3)C中铁铈合金的作用是______________,要先加热至一定温度的原因是______________;
(4)如果通入C中的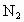 、
、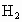 各有1 mol、3 mol,为什么反应后放出的热量比92.4 kJ少?
各有1 mol、3 mol,为什么反应后放出的热量比92.4 kJ少?
按图所示装置连接好仪器.
已知:A中装有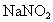 和
和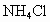 混合溶液,B中装有碱石灰,C中有铁铈合金,D中有酚酞试液.
混合溶液,B中装有碱石灰,C中有铁铈合金,D中有酚酞试液.
C中发生反应的热化学方程式为: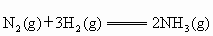 ;
;
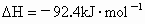
实验步骤如下:①检查装置的气密性;②用酒精灯加热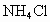 和
和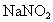 饱和溶液,待有气体生成,可停止加热,但仍有大量气体产生;③再用酒精灯给铁铈合金加热至一定温度;④从分液漏斗中滴入一定浓度盐酸,不久见酚酞试液变红.
饱和溶液,待有气体生成,可停止加热,但仍有大量气体产生;③再用酒精灯给铁铈合金加热至一定温度;④从分液漏斗中滴入一定浓度盐酸,不久见酚酞试液变红.
回答下列问题:
(1)写出A中两溶液间发生反应的化学方程式________,此反应为________热反应(填“放”或“吸”);
(2)先用酒精灯加热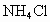 、
、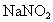 饱和溶液的目的是______________;
饱和溶液的目的是______________;
(3)C中铁铈合金的作用是______________,要先加热至一定温度的原因是______________;
(4)如果通入C中的 、
、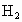 各有1 mol、3 mol,为什么反应后放出的热量比92.4 kJ少?
各有1 mol、3 mol,为什么反应后放出的热量比92.4 kJ少?

| Fe |
| Fe |
(15分)某研究小组设计如下装置分离CO和CO2的混合气体并探究CO还原氧化铜的产物和过氧化钠的性质。已知氯化钯(PdCl2)溶液遇CO气体会产生黑色沉淀(金属单质)。夹持装置未画出。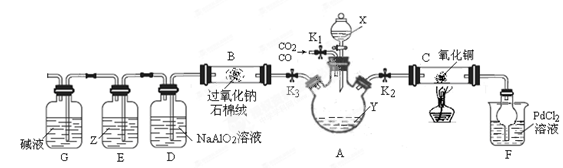
(题9图)
(1)试剂X、Y的焰色反应均呈黄色,则X、Y可能是 、 .
(2)连接装置、检验气密性并装好药品后,关闭分液漏斗活塞和K3,打开K1、K2,分离出CO,当观察到 现象时,可对C装置进行加热操作,反应产物为红色固体。
(3)查询资料获得以下信息:①Cu2O为红色固体;②常温下,Cu2+在溶液中稳定,Cu+易在酸性条件下发生反应:2Cu+ =Cu2++Cu。
甲、乙两组同学取上述红色固体(用M代表)进行实验,探究其成分:
| 组别 | 实验操作 | 实验现象或数据 | 结 论 |
| 甲 | ① 向a g M中加入一定量稀硫酸,充分搅拌; ② 继续滴加稀硫酸至过量, 充分反应. | ①固体明显减少; ②仍然有一定量固体,溶液呈蓝色 | ①M中一定有Cu2O; ②M中一定有Cu. |
| 乙 | 将甲实验后所得溶液过滤 将滤渣洗涤、干燥、称量 | 滤渣质量为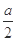 g g | M为Cu和Cu2O的混合物 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com