
题目列表(包括答案和解析)
工业制备的高锰酸钾是锰的重要化合物和常用的氧化剂。以下附图是工业上用软锰矿制备高锰酸钾的一种工艺流程。
(1)KMnO4稀溶液是一种常用的消毒剂。其消毒原理与下列物质相同的是_____(填代号)。
a. 84消毒液(NaClO溶液) b. 双氧水 c. 苯酚 d. 75%酒精
(2)上述流程中可以循环使用的物质有 、 (写化学式)。(3)若不考虑物质循环与制备过程中的损失,则1 mol MnO2可制得 mol KMnO4。
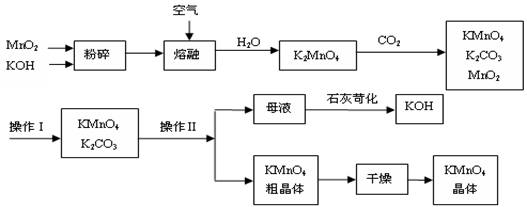 (4)操作Ⅰ的名称是_____________;操作Ⅱ是根据KMnO4和K2CO3两物质在__________(填性质)上差异,采用____________(填操作步骤)、趁热过滤得到KMnO4粗晶体的。
(4)操作Ⅰ的名称是_____________;操作Ⅱ是根据KMnO4和K2CO3两物质在__________(填性质)上差异,采用____________(填操作步骤)、趁热过滤得到KMnO4粗晶体的。
| 实验编号 | T/K | 催化剂的用量/g | KMnO4酸性溶液的浓度/mol?L-1 | 实验目的 |
| ① | 298 | 0.5 | 0.01 | (Ⅰ)实验①和②探究KMnO4酸性溶液的浓度对该反应速率的影响; (Ⅱ)实验①和 ③ ③ 探究温度对该反应速率的影响;(Ⅲ)实验①和 ④ ④ 探究催化剂对该反应速率的影响;) |
| ② | 298 298 |
0.5 0.5 |
0.001 0.001 | |
| ③ | 323K 323K |
0.5 0.5 |
0.01 0.01 | |
| ④ | 298 298 |
0 0 |
0.01 0.01 |
| KMnO4酸性溶液 的浓度/mol?L-1 |
溶液褪色所需时间 t/min | ||
| 第1次 | 第2次 | 第3次 | |
| 0.01 | 14 | 13 | 11 |
| 0.001 | 6 | 7 | 7 |
(共6分)某温度时,在2L容器中X、Y、Z三种物质随时间的变化关系曲线如图所示。

(1)由图中的数据分析,该反应的化学反应方程式为 ;
(2)反应开始至2minZ的平均反应速率为 ;
(3)若不改变外界条件,5min ~ 6min Z的生成速率(V1)与6min后Z的生成速率(V2)的大小关系为:V1 V2(填大于、小于或等于)。
(共6分)某温度时,在2L容器中X、Y、Z三种物质随时间的变化关系曲线如图所示。

(1)由图中的数据分析,该反应的化学反应方程式为 ;
(2)反应开始至2minZ的平均反应速率为 ;
(3)若不改变外界条件,5min ~ 6min Z的生成速率(V1)与6min后Z的生成速率(V2)的大小关系为:V1 V2(填大于、小于或等于)。
(共6分)某温度时,在2L容器中X、Y、Z三种物质随时间的变化关系曲线如图所示。
(1)由图中的数据分析,该反应的化学反应方程式为 ;
(2)反应开始至2minZ的平均反应速率为 ;
(3)若不改变外界条件,5min ~ 6min Z的生成速率(V1)与6min后Z的生成速率(V2)的大小关系为:V1 V2(填大于、小于或等于)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com