利用N
2和H
2可以实现NH
3的工业合成,而氨又可以进一步制备硝酸,在工业上一般可进行连续生产.请回答下列问题:
(1)已知:N
2(g)+O
2(g)═2NO(g)△H=+180.5kJ?mol
-1N
2(g)+3H
2(g)?2NH
3(g)△H=-92.4kJ?mol
-12H
2(g)+O
2(g)═2H
2O(g)△H=-483.6kJ?mol
-1若有17g氨气经催化氧化完全生成一氧化氮气体和水蒸气所放出的热量为______;
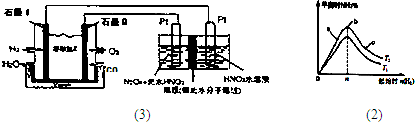
(2)某科研小组研究在其他条件不变的情况下,改变起始物氢气的物质的量对N
2(g)+3H
2(g)?2NH
3(g)反应的影响,实验结果如图2所示:(图中T表示温度,n表示物质的量)
①图象中T
1和T
2的关系是:T
1______T
2(填“>”、“<”、“=”或“无法确定”)
②比较在a、b、c三点所处的平衡状态中,反应物N
2的转化率最高的是______(填字母标号),
③在起始体系中加入N
2的物质的量为______mol时,反应后氨的百分含量最大.若容器容积为1L,n=3mol反应达到平衡时H
2的转化率为60%,则此条件下(T
2),反应的平衡常数K=______;
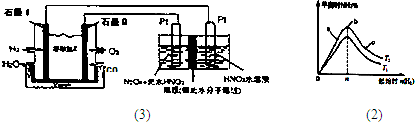
(3)N
2O
3是一种新型硝化剂,其性质和制备受到人们的关注.
①一定温度下,在恒容密闭容器中N
2O
3可发生下列反应:2N
2O
3?4NO
2(g)+O
2△H>0下表为反应在某温度下的部分实验数据则50s内NO
2的平均生成速率为______
| V/s |
0 |
50 |
100 |
| c(N2O3)/mol?L-1 |
5.00 |
3.52 |
2.48 |
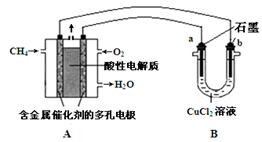
②现以H
2、O
2、熔融盐Na
2CO
3组成的燃料电池,采用电解法制备N
2O
3,装置如图1所示,其中Y为CO
2.写出石墨I电极上发生反应的电极反应式______

 N2O4(g) ΔH < 0反应,在温度为T1,T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。则下列说法正确的是 。
N2O4(g) ΔH < 0反应,在温度为T1,T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。则下列说法正确的是 。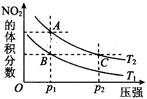
 N2O4(g) ΔH < 0反应,在温度为T1,T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。则下列说法正确的是 。
N2O4(g) ΔH < 0反应,在温度为T1,T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。则下列说法正确的是 。