
ΧβΡΩΝ–±μ(Αϋά®¥πΑΗΚΆΫβΈω)
Ρ≥Ωσ―υΚ§”–¥σΝΩΒΡCuSΦΑ…ΌΝΩΤδΥϋ≤Μ»ή”ΎΥαΒΡ‘”÷ ΓΘ Β―ι “÷–“‘ΗΟΩσ―υΈΣ‘≠Νœ÷Τ±ΗCuCl2ΓΛ2H2OΨßΧεΘ§Νς≥Χ»γœ¬ΘΚ

Θ®1Θ©‘Ύ Β―ι “÷–Θ§”ϊ”Ο37ΘΞ(ΟήΕ»ΈΣ1Θ°19 gΓΛmL-1)ΒΡ―ΈΥα≈δ÷Τ500 mL 6 molΓΛL-1ΒΡ―ΈΥαΘ§–η“ΣΒΡ“«Τς≥ΐΝΩΆ≤ΓΔ…’±≠ΓΔ≤ΘΝßΑτΆβΘ§ΜΙ”–? ?? ? ΓΔ?? ??? ΓΘ
Θ®2Θ©ΔΌ»τ‘Ύ Β―ι “÷–Άξ≥…œΒΝ–≤ΌΉςaΓΘ‘ρœ¬Ν– Β―ι≤ΌΉς÷–Θ§≤Μ–η“ΣΒΡ «??? (Χνœ¬Ν–Ηςœν÷––ρΚ≈)ΓΘ

ΔΎCuCl2»ή“Κ÷–¥φ‘Ύ»γœ¬ΤΫΚβΘΚCu(H2O)42+(άΕ…Ϊ)+4Cl- CuCl42-(ΜΤ…Ϊ)+4H2OΓΘ
CuCl42-(ΜΤ…Ϊ)+4H2OΓΘ
”ϊ”Ο Β―ι÷ΛΟς¬Υ“ΚA(¬Χ…Ϊ)÷–¥φ‘Ύ…œ ωΤΫΚβΘ§≥ΐ¬Υ“ΚAΆβΘ§œ¬Ν– ‘ΦΝ÷–Θ§ΜΙ–η“ΣΒΡ «?? ??? (Χνœ¬Ν–Ηςœν÷––ρΚ≈)ΓΘ
aΘ°FeCl3ΙΧΧε ????? bΘ°CuCl2ΙΧΧε ???? cΘ°’τΝσΥ°
Θ®3Θ©Ρ≥Μ·―ß–ΓΉι”ϊ‘Ύ Β―ι “÷–―–ΨΩCuS±Κ…’ΒΡΖ¥”ΠΙΐ≥ΧΘ§≤ι‘ΡΉ ΝœΒΟ÷Σ‘ΎΩ’ΤχΧθΦΰœ¬±Κ…’CuS ±Θ§ΙΧΧε÷ ΝΩ±δΜ·«ζœΏΦΑSO2…ζ≥…«ζœΏ»γœ¬ΆΦΥυ ΨΓΘ

ΔΌCuSΩσ―υ‘Ύ±Κ…’Ιΐ≥Χ÷–Θ§”–Cu2SΓΔCuOΓΛCuSO4ΓΔCuSO4ΓΔCuO…ζ≥…Θ§ΉΣΜ·Υ≥–ρΈΣΘΚ

ΒΎΔΌ≤ΫΉΣΜ·÷ς“Σ‘Ύ200ΓΪ300oCΖΕΈßΡΎΫχ––Θ§ΗΟ≤ΫΉΣΜ·ΒΡΜ·―ßΖΫ≥Χ ΫΈΣ??????????????????????????????????????????????????????????????? ΓΘ
ΔΎ300ΓΪ400oCΖΕΈßΡΎΘ§ΙΧΧε÷ ΝΩΟςœ‘‘ωΦ”ΒΡ‘≠“ρ «? ??????? ? Θ§…œΆΦΥυ ΨΙΐ≥Χ÷–Θ§CuSO4ΙΧΧεΡήΈ»Ε®¥φ‘ΎΒΡΫΉΕΈ «??? (Χνœ¬Ν–Ηςœν÷––ρΚ≈)ΓΘ
aΘ°“ΜΫΉΕΈ??? bΓΔΕΰΫΉΕΈ??? cΓΔ»ΐΫΉΕΈ? dΓΔΥΡΫΉΕΈ
ΔέΗΟΜ·―ß–ΓΉι…ηΦΤ»γœ¬ΉΑ÷ΟΡΘΡβCuSΩσ―υ‘Ύ―θΤχ÷–±Κ…’ΒΎΥΡΫΉΕΈΒΡΙΐ≥ΧΘ§≤Δ―ι÷ΛΥυΒΟΤχΧεΈΣSO2ΚΆO2ΒΡΜλΚœΈοΓΘ

aΘ°ΉΑ÷ΟΉιΉΑΆξ≥…ΚσΘ§”ΠΝΔΦ¥Ϋχ––ΒΡ“Μœν≤ΌΉς «? ???????????? ΓΘ
bΘ°Β±DΉΑ÷Ο÷–≤ζ…ζΑΉ…Ϊ≥ΝΒμ ±Θ§±ψΡήΥΒΟςΒΎΥΡΫΉΕΈΥυΒΟΤχΧεΈΣSO2ΚΆO2ΒΡΜλΚœΈοΓΘΡψ»œΈΣΉΑ÷ΟD÷–‘≠ά¥ Δ”–ΒΡ»ή“ΚΈΣ? ??? ? »ή“ΚΓΘ
cΘ°»τ‘≠CuSΩσ―υΒΡ÷ ΝΩΈΣl0Θ°0 gΘ§‘Ύ Β―ιΙΐ≥Χ÷–Θ§±Θ≥÷Έ¬Ε»‘Ύ760oCΉσ”“≥÷–χΦ”»»Θ§¥ΐΩσ―υ≥δΖ÷Ζ¥”ΠΚσΘ§ ·”Δ≤ΘΝßΙήΡΎΥυΒΟΙΧΧεΒΡ÷ ΝΩΈΣ8Θ°0 gΘ§‘ρ‘≠Ωσ―υ÷–CuSΒΡ÷ ΝΩΖ÷ ΐΈΣ?? ?? ΓΘ
Ρ≥Ωσ―υΚ§”–¥σΝΩΒΡCuSΦΑ…ΌΝΩΤδΥϋ≤Μ»ή”ΎΥαΒΡ‘”÷ ΓΘ Β―ι “÷–“‘ΗΟΩσ―υΈΣ‘≠Νœ÷Τ±ΗCuCl2ΓΛ2H2OΨßΧεΘ§Νς≥Χ»γœ¬ΘΚ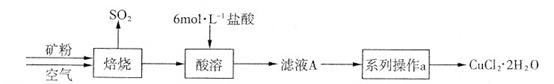
Θ®1Θ©‘Ύ Β―ι “÷–Θ§”ϊ”Ο37ΘΞ(ΟήΕ»ΈΣ1Θ°19 gΓΛmL-1)ΒΡ―ΈΥα≈δ÷Τ500 mL 6 molΓΛL-1ΒΡ―ΈΥαΘ§–η“ΣΒΡ“«Τς≥ΐΝΩΆ≤ΓΔ…’±≠ΓΔ≤ΘΝßΑτΆβΘ§ΜΙ”– ΓΔ ΓΘ
Θ®2Θ©ΔΌ»τ‘Ύ Β―ι “÷–Άξ≥…œΒΝ–≤ΌΉςaΓΘ‘ρœ¬Ν– Β―ι≤ΌΉς÷–Θ§≤Μ–η“ΣΒΡ « (Χνœ¬Ν–Ηςœν÷––ρΚ≈)ΓΘ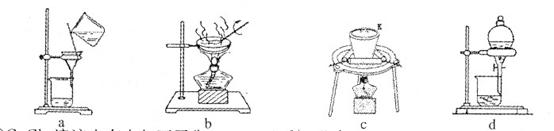
ΔΎCuCl2»ή“Κ÷–¥φ‘Ύ»γœ¬ΤΫΚβΘΚCu(H2O)42+(άΕ…Ϊ)+4Cl-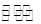 CuCl42-(ΜΤ…Ϊ)+4H2OΓΘ
CuCl42-(ΜΤ…Ϊ)+4H2OΓΘ
”ϊ”Ο Β―ι÷ΛΟς¬Υ“ΚA(¬Χ…Ϊ)÷–¥φ‘Ύ…œ ωΤΫΚβΘ§≥ΐ¬Υ“ΚAΆβΘ§œ¬Ν– ‘ΦΝ÷–Θ§ΜΙ–η“ΣΒΡ « (Χνœ¬Ν–Ηςœν÷––ρΚ≈)ΓΘ
aΘ°FeCl3ΙΧΧε bΘ°CuCl2ΙΧΧε cΘ°’τΝσΥ°
Θ®3Θ©Ρ≥Μ·―ß–ΓΉι”ϊ‘Ύ Β―ι “÷–―–ΨΩCuS±Κ…’ΒΡΖ¥”ΠΙΐ≥ΧΘ§≤ι‘ΡΉ ΝœΒΟ÷Σ‘ΎΩ’ΤχΧθΦΰœ¬±Κ…’CuS ±Θ§ΙΧΧε÷ ΝΩ±δΜ·«ζœΏΦΑSO2…ζ≥…«ζœΏ»γœ¬ΆΦΥυ ΨΓΘ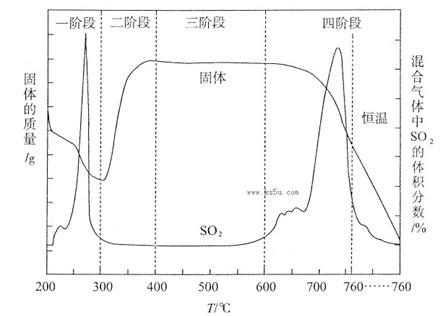
ΔΌCuSΩσ―υ‘Ύ±Κ…’Ιΐ≥Χ÷–Θ§”–Cu2SΓΔCuOΓΛCuSO4ΓΔCuSO4ΓΔCuO…ζ≥…Θ§ΉΣΜ·Υ≥–ρΈΣΘΚ
ΒΎΔΌ≤ΫΉΣΜ·÷ς“Σ‘Ύ200ΓΪ300oCΖΕΈßΡΎΫχ––Θ§ΗΟ≤ΫΉΣΜ·ΒΡΜ·―ßΖΫ≥Χ ΫΈΣ ΓΘ
ΔΎ300ΓΪ400oCΖΕΈßΡΎΘ§ΙΧΧε÷ ΝΩΟςœ‘‘ωΦ”ΒΡ‘≠“ρ « Θ§…œΆΦΥυ ΨΙΐ≥Χ÷–Θ§CuSO4ΙΧΧεΡήΈ»Ε®¥φ‘ΎΒΡΫΉΕΈ « (Χνœ¬Ν–Ηςœν÷––ρΚ≈)ΓΘ
aΘ°“ΜΫΉΕΈ bΓΔΕΰΫΉΕΈ cΓΔ»ΐΫΉΕΈ dΓΔΥΡΫΉΕΈ
ΔέΗΟΜ·―ß–ΓΉι…ηΦΤ»γœ¬ΉΑ÷ΟΡΘΡβCuSΩσ―υ‘Ύ―θΤχ÷–±Κ…’ΒΎΥΡΫΉΕΈΒΡΙΐ≥ΧΘ§≤Δ―ι÷ΛΥυΒΟΤχΧεΈΣSO2ΚΆO2ΒΡΜλΚœΈοΓΘ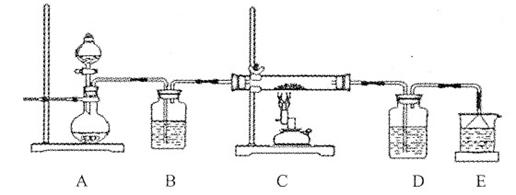
aΘ°ΉΑ÷ΟΉιΉΑΆξ≥…ΚσΘ§”ΠΝΔΦ¥Ϋχ––ΒΡ“Μœν≤ΌΉς « ΓΘ
bΘ°Β±DΉΑ÷Ο÷–≤ζ…ζΑΉ…Ϊ≥ΝΒμ ±Θ§±ψΡήΥΒΟςΒΎΥΡΫΉΕΈΥυΒΟΤχΧεΈΣSO2ΚΆO2ΒΡΜλΚœΈοΓΘΡψ»œΈΣΉΑ÷ΟD÷–‘≠ά¥ Δ”–ΒΡ»ή“ΚΈΣ »ή“ΚΓΘ
cΘ°»τ‘≠CuSΩσ―υΒΡ÷ ΝΩΈΣl0Θ°0 gΘ§‘Ύ Β―ιΙΐ≥Χ÷–Θ§±Θ≥÷Έ¬Ε»‘Ύ760oCΉσ”“≥÷–χΦ”»»Θ§¥ΐΩσ―υ≥δΖ÷Ζ¥”ΠΚσΘ§ ·”Δ≤ΘΝßΙήΡΎΥυΒΟΙΧΧεΒΡ÷ ΝΩΈΣ8Θ°0 gΘ§‘ρ‘≠Ωσ―υ÷–CuSΒΡ÷ ΝΩΖ÷ ΐΈΣ ΓΘ
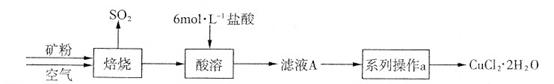
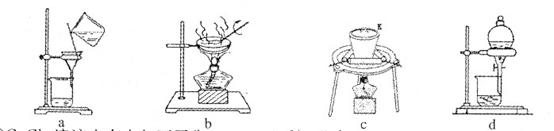
 CuCl42-(ΜΤ…Ϊ)+4H2OΓΘ
CuCl42-(ΜΤ…Ϊ)+4H2OΓΘ

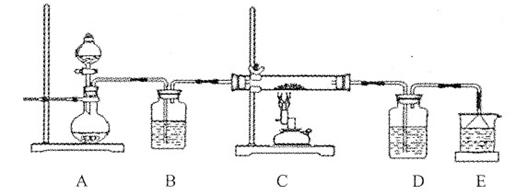
(Ι≤15Ζ÷) Ρ≥Ωσ―υΚ§”–¥σΝΩΒΡCuSΦΑ…ΌΝΩΤδΥϋ≤Μ»ή”ΎΥαΒΡ‘”÷ ΓΘ Β―ι “÷–“‘ΗΟΩσ―υΈΣ‘≠Νœ÷Τ±ΗCuCl2ΓΛ2H2OΨßΧεΘ§Νς≥Χ»γœ¬ΘΚ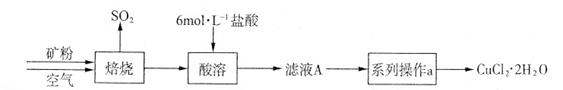
Θ®1Θ©‘Ύ Β―ι “÷–Θ§”ϊ”Ο37ΘΞ(ΟήΕ»ΈΣ1Θ°19 gΓΛmL-1)ΒΡ―ΈΥα≈δ÷Τ500 mL 6 molΓΛL-1ΒΡ―ΈΥαΘ§–η“ΣΒΡ“«Τς≥ΐΝΩΆ≤ΓΔ…’±≠ΓΔ≤ΘΝßΑτΆβΘ§ΜΙ”–_______________ ΓΔ _______________ ΓΘ
Θ®2Θ©ΔΌ»τ‘Ύ Β―ι “÷–Άξ≥…œΒΝ–≤ΌΉςaΓΘ‘ρœ¬Ν– Β―ι≤ΌΉς÷–Θ§≤Μ–η“ΣΒΡ «_______ (Χνœ¬Ν–Ηςœν÷––ρΚ≈)ΓΘ
ΔΎCuCl2»ή“Κ÷–¥φ‘Ύ»γœ¬ΤΫΚβΘΚCu(H2O)42+(άΕ…Ϊ)+4Cl-  CuCl42-(ΜΤ…Ϊ)+4H2OΓΘ
CuCl42-(ΜΤ…Ϊ)+4H2OΓΘ
”ϊ”Ο Β―ι÷ΛΟς¬Υ“ΚA(¬Χ…Ϊ)÷–¥φ‘Ύ…œ ωΤΫΚβΘ§≥ΐ¬Υ“ΚAΆβΘ§œ¬Ν– ‘ΦΝ÷–Θ§ΜΙ–η“ΣΒΡ «____ (Χνœ¬Ν–Ηςœν÷––ρΚ≈)ΓΘ aΘ°FeCl3ΙΧΧε bΘ°CuCl2ΙΧΧε cΘ°’τΝσΥ°
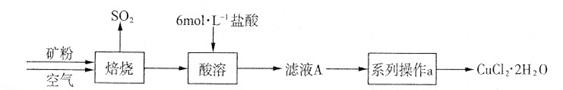
Θ®3Θ©Ρ≥Μ·―ß–ΓΉι”ϊ‘Ύ Β―ι “÷–―–ΨΩCuS±Κ…’ΒΡΖ¥”ΠΙΐ≥ΧΘ§≤ι‘ΡΉ ΝœΒΟ÷Σ‘ΎΩ’ΤχΧθΦΰœ¬±Κ…’CuS ±Θ§ΙΧΧε÷ ΝΩ±δΜ·«ζœΏΦΑSO2…ζ≥…«ζœΏ»γœ¬ΆΦΥυ ΨΓΘ
ΔΌCuSΩσ―υ‘Ύ±Κ…’Ιΐ≥Χ÷–Θ§”–Cu2SΓΔCuOΓΛCuSO4ΓΔCuSO4ΓΔCuO…ζ≥…Θ§ΉΣΜ·Υ≥–ρΈΣœ¬Ν–ΥΡΫΉΕΈΘΚ
ΒΎΔΌ≤ΫΉΣΜ·÷ς“Σ‘Ύ200ΓΪ300oCΖΕΈßΡΎΫχ––Θ§ΗΟ≤ΫΉΣΜ·ΒΡΜ·―ßΖΫ≥Χ ΫΈΣ _______________ ΓΘ
ΔΎ300ΓΪ400oCΖΕΈßΡΎΘ§ΙΧΧε÷ ΝΩΟςœ‘‘ωΦ”ΒΡ‘≠“ρ «_______________Θ§…œΆΦΥυ ΨΙΐ≥Χ÷–Θ§CuSO4ΙΧΧεΡήΈ»Ε®¥φ‘ΎΒΡΫΉΕΈ «__________(Χνœ¬Ν–Ηςœν÷––ρΚ≈)ΓΘ
aΘ°“ΜΫΉΕΈ bΓΔΕΰΫΉΕΈ cΓΔ»ΐΫΉΕΈ dΓΔΥΡΫΉΕΈ
ΔέΗΟΜ·―ß–ΓΉι…ηΦΤ»γœ¬ΉΑ÷ΟΡΘΡβCuSΩσ―υ‘Ύ―θΤχ÷–±Κ…’ΒΎΥΡΫΉΕΈΒΡΙΐ≥ΧΘ§≤Δ―ι÷ΛΥυΒΟΤχΧεΈΣSO2ΚΆO2ΒΡΜλΚœΈοΓΘ
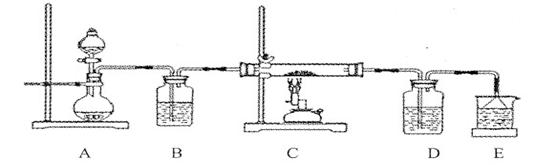
aΘ°ΉΑ÷ΟΉιΉΑΆξ≥…ΚσΘ§”ΠΝΔΦ¥Ϋχ––ΤχΟή–‘Φλ≤ιΘ§«κ–¥≥ωΦλ≤ιA-DΉΑ÷ΟΤχΟή–‘ΒΡ≤ΌΉς __________ ΓΘ
bΘ°Β±DΉΑ÷Ο÷–≤ζ…ζΑΉ…Ϊ≥ΝΒμ ±Θ§±ψΡήΥΒΟςΒΎΥΡΫΉΕΈΥυΒΟΤχΧεΈΣSO2ΚΆO2ΒΡΜλΚœΈοΓΘΡψ»œΈΣΉΑ÷ΟD÷–‘≠ά¥ Δ”–ΒΡ»ή“ΚΈΣ_______________ »ή“ΚΓΘ
cΘ°»τ‘≠CuSΩσ―υΒΡ÷ ΝΩΈΣl0Θ°0 gΘ®Κ§Φ”»»≤ΜΖ¥”ΠΒΡ‘”÷ Θ©Θ§‘Ύ Β―ιΙΐ≥Χ÷–Θ§±Θ≥÷Έ¬Ε»‘Ύ760oCΉσ”“≥÷–χΦ”»»Θ§¥ΐΩσ―υ≥δΖ÷Ζ¥”ΠΚσΘ§ ·”Δ≤ΘΝßΙήΡΎΥυΒΟΙΧΧεΒΡ÷ ΝΩΈΣ8Θ°4 gΘ§‘ρ‘≠Ωσ―υ÷–CuSΒΡ÷ ΝΩΖ÷ ΐΈΣ__________ΓΘ

 CuCl42-(ΜΤ…Ϊ)+4H2OΓΘ
CuCl42-(ΜΤ…Ϊ)+4H2OΓΘ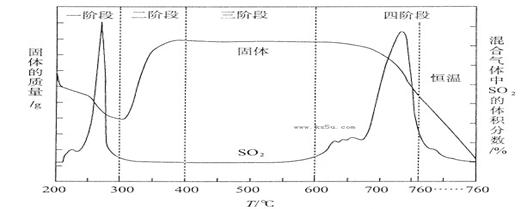

“ΜΓΔ1.ΫβΈωΘΚc(NH )‘ω¥σΘ§ΤΫΚβΡφœρ“ΤΕ·ΓΘ
)‘ω¥σΘ§ΤΫΚβΡφœρ“ΤΕ·ΓΘ
¥πΑΗΘΚC
2.A 3.B 4.B 5.AD 6.B 7.A 8.B 9.D?
ΕΰΓΔ10.Θ®1Θ©100 mL»ίΝΩΤΩ?
Θ®2Θ©ΘΨ b?
Θ®3Θ©≈δ÷ΤpH=1ΒΡHA»ή“ΚΡ―“‘ Βœ÷Θ§≤ΜΆΉ÷°¥Π‘Ύ”ΎΦ”»κΒΡ–ΩΝΘΡ―“‘ΉωΒΫ±μΟφΜΐœύΆ§ΓΘ
Θ®4Θ©≈δ÷ΤNaA»ή“ΚΘ§≤βΤδpHΘΨ7Θ§Φ¥÷ΛΟςHA «»θΒγΫβ÷ ΓΘ?
11.(1)”“?
(2)ΔΌ–Γ«ρœ¬≥ΝΒΫ…’±≠ΒΉ≤Ω ΔΎ≤ζ…ζΑΉ…Ϊ≥ΝΒμ ΔέΒγΝςΦΤ÷Η’κΤΪΉΣΖυΕ»≤ΜΕœ±δ–ΓΘ§ΉνΚσ÷Η’κΜΊΒΫ÷–―κ?
(3)Ca3Θ®PO4Θ©2ΘΪ3H2SO4===2H3PO4ΘΪ3CaSO4?
12.(1)H2Θ¬ Θ®2Θ©C3Θ≠ HBΘ≠ (3)BC?
(4)H
2HΘΝΘΪC3Θ≠===2ΘΝΘ≠ΘΪH
13.Θ®1Θ©Φθ–Γ ‘ω¥σ Θ®2Θ©Φθ–Γ ‘ω¥σ Θ®3Θ©‘ω¥σ Φθ–Γ?
14.Θ®1Θ©ΕΦ≤ζ…ζΤχ≈ίΘ§Zn»ήΫβ a≤ζ…ζΤχ≈ίΓΔZn»ήΫβΥΌΕ»ΕΦΩλ HClΆξ»ΪΒγάκΘ§HCl÷–ΒΡc(H+)¥σ”ΎCH3COOH÷–ΒΡc(H+)?
Θ®2Θ©¥σ Β»”Ύ a÷–c(H+)¥σ”Ύb÷–ΒΡc(H+),ΕχΥαΒΡΉήΝΩœύΒ»
ΙζΦ ―ß–Θ”≈―Γ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com