
ÌâÄ¿Áбí(°üÀ¨´ð°¸ºÍ½âÎö)
£¨10·Ö£©Ö÷×åÔªËØW¡¢X¡¢Y¡¢ZµÄÔ×ÓÐòÊýÒÀ´ÎÔö´ó£¬WµÄÔ×Ó×îÍâ²ãµç×ÓÊýÊÇ´ÎÍâ²ãµç×ÓÊýµÄ3±¶¡£X¡¢YºÍZ·ÖÊô²»Í¬µÄÖÜÆÚ£¬ËûÃǵÄÔ×ÓÐòÊýÖ®ºÍÊÇWÔ×ÓÐòÊýµÄ5±¶£¬ZÔªËصĻù̬Ô×ÓµÄ×îÍâ²ãÒ»¸öδ³É¶Ôµç×Ó£¬ÔÚÓÉÔªËØW¡¢X¡¢Y¡¢Z×é³ÉµÄËùÓпÉÄܵĶþ×é·Ö»¯ºÏÎïÖУ¬ÓÉÔªËØWÓëYÐγɵĻ¯ºÏÎïMµÄÈÛµã×î¸ß¡£Çë»Ø´ðÏÂÁÐÎÊÌ⣺
£¨1£©WÔªËØÓëXÔªËØÏà±È£¬µç¸ºÐÔX´óÓÚW£¬ÏÂÁÐÄÜÖ¤Ã÷ÕâÒ»ÊÂʵµÄÊÇ £¨ÌîÑ¡ÏîÐòºÅ£©
A£®³£ÎÂÏÂXµ¥ÖʵÄÑÕÉ«±ÈWµ¥ÖʵÄÑÕÉ«Éî
B£®Xµ¥ÖÊÓëWµÄÇ⻯Îï¾çÁÒ·´Ó¦£¬²úÉúWµÄµ¥ÖÊ
C£®XÓëWÐγɵĻ¯ºÏÎïÖÐXÔªËسʸº¼Û̬
D£®±È½ÏÁ½ÔªËصĵ¥ÖÊÓëÇâÆø»¯ºÏʱµÃµç×ÓµÄÊýÄ¿
£¨2£©»¯ºÏÎïMµÄ»¯Ñ§Ê½Îª £¬Æ侧Ìå½á¹¹ÓëNaClÏàͬ£¬¶øÈÛµã¸ßÓÚNaCl¡£MÈÛµã½Ï¸ßµÄÔÒòÊÇ ¡£½«Ò»¶¨Á¿µÄ»¯ºÏÎïZX¸ºÔØÔÚMÉÏ¿ÉÖƵÃZX/M´ß»¯¼Á£¬ÓÃÓÚ´ß»¯Ì¼Ëá¶þ¼×õ¥ÓëÔ¹ð´¼õ¥½»»»ºÏ³É̼Ëá¶þÔ¹ðõ¥¡£ÔÚ̼Ëá¶þ¼×õ¥·Ö×ÓÖУ¬Ì¼Ô×Ó²ÉÓõÄÔÓ»¯·½Ê½ÓÐ £¬O¡ªC¡ªOµÄ¼ü½ÇԼΪ £»
£¨3£©×ÆÉÕº¬ÔªËØZµÄÑΣ¬»áʹ»ðÑæ³ÊÏÖÌØÊâµÄÑÕÉ«£¬ÇëÓÃÔ×ӽṹµÄ֪ʶ½âÎöÆäÔÒò£º ¡£
£¨10·Ö£©Ö÷×åÔªËØW¡¢X¡¢Y¡¢ZµÄÔ×ÓÐòÊýÒÀ´ÎÔö´ó£¬WµÄÔ×Ó×îÍâ²ãµç×ÓÊýÊÇ´ÎÍâ²ãµç×ÓÊýµÄ3±¶¡£X¡¢YºÍZ·ÖÊô²»Í¬µÄÖÜÆÚ£¬ËûÃǵÄÔ×ÓÐòÊýÖ®ºÍÊÇWÔ×ÓÐòÊýµÄ5±¶£¬ZÔªËصĻù̬Ô×ÓµÄ×îÍâ²ãÒ»¸öδ³É¶Ôµç×Ó£¬ÔÚÓÉÔªËØW¡¢X¡¢Y¡¢Z×é³ÉµÄËùÓпÉÄܵĶþ×é·Ö»¯ºÏÎïÖУ¬ÓÉÔªËØWÓëYÐγɵĻ¯ºÏÎïMµÄÈÛµã×î¸ß¡£Çë»Ø´ðÏÂÁÐÎÊÌ⣺
£¨1£©WÔªËØÓëXÔªËØÏà±È£¬µç¸ºÐÔX´óÓÚW£¬ÏÂÁÐÄÜÖ¤Ã÷ÕâÒ»ÊÂʵµÄÊÇ £¨ÌîÑ¡ÏîÐòºÅ£©
A£®³£ÎÂÏÂXµ¥ÖʵÄÑÕÉ«±ÈWµ¥ÖʵÄÑÕÉ«Éî
B£®Xµ¥ÖÊÓëWµÄÇ⻯Îï¾çÁÒ·´Ó¦£¬²úÉúWµÄµ¥ÖÊ
C£®XÓëWÐγɵĻ¯ºÏÎïÖÐXÔªËسʸº¼Û̬
D£®±È½ÏÁ½ÔªËصĵ¥ÖÊÓëÇâÆø»¯ºÏʱµÃµç×ÓµÄÊýÄ¿
£¨2£©»¯ºÏÎïMµÄ»¯Ñ§Ê½Îª £¬Æ侧Ìå½á¹¹ÓëNaClÏàͬ£¬¶øÈÛµã¸ßÓÚNaCl¡£MÈÛµã½Ï¸ßµÄÔÒòÊÇ ¡£½«Ò»¶¨Á¿µÄ»¯ºÏÎïZX¸ºÔØÔÚMÉÏ¿ÉÖƵÃZX/M´ß»¯¼Á£¬ÓÃÓÚ´ß»¯Ì¼Ëá¶þ¼×õ¥ÓëÔ¹ð´¼õ¥½»»»ºÏ³É̼Ëá¶þÔ¹ðõ¥¡£ÔÚ̼Ëá¶þ¼×õ¥·Ö×ÓÖУ¬Ì¼Ô×Ó²ÉÓõÄÔÓ»¯·½Ê½ÓÐ £¬O¡ªC¡ªOµÄ¼ü½ÇԼΪ £»
£¨3£©×ÆÉÕº¬ÔªËØZµÄÑΣ¬»áʹ»ðÑæ³ÊÏÖÌØÊâµÄÑÕÉ«£¬ÇëÓÃÔ×ӽṹµÄ֪ʶ½âÎöÆäÔÒò£º ¡£
Ö÷×åÔªËØW¡¢X¡¢Y¡¢ZµÄÔ×ÓÐòÊýÒÀ´ÎÔö´ó£¬WµÄÔ×Ó×îÍâ²ãµç×ÓÊýÊÇ´ÎÍâ²ãµç×ÓÊýµÄ3±¶¡£X¡¢YºÍZ·ÖÊô²»Í¬µÄÖÜÆÚ£¬ËûÃǵÄÔ×ÓÐòÊýÖ®ºÍÊÇWÔ×ÓÐòÊýµÄ5±¶£¬ZÔªËصĻù̬Ô×ÓµÄ×îÍâ²ãÒ»¸öδ³É¶Ôµç×Ó£¬ÔÚÓÉÔªËØW¡¢X¡¢Y¡¢Z×é³ÉµÄËùÓпÉÄܵĶþ×é·Ö»¯ºÏÎïÖУ¬ÓÉÔªËØWÓëYÐγɵĻ¯ºÏÎïMµÄÈÛµã×î¸ß¡£Çë»Ø´ðÏÂÁÐÎÊÌ⣺
£¨1£©WÔªËØÓëXÔªËØÏà±È£¬µç¸ºÐÔX´óÓÚW£¬ÏÂÁÐÄÜÖ¤Ã÷ÕâÒ»ÊÂʵµÄÊÇ £¨ÌîÑ¡ÏîÐòºÅ£©
A£®³£ÎÂÏÂXµ¥ÖʵÄÑÕÉ«±ÈWµ¥ÖʵÄÑÕÉ«Éî
B£®Xµ¥ÖÊÓëWµÄÇ⻯Îï¾çÁÒ·´Ó¦£¬²úÉúWµÄµ¥ÖÊ
C£®XÓëWÐγɵĻ¯ºÏÎïÖÐXÔªËسʸº¼Û̬
D£®±È½ÏÁ½ÔªËصĵ¥ÖÊÓëÇâÆø»¯ºÏʱµÃµç×ÓµÄÊýÄ¿¡®
£¨2£©»¯ºÏÎïMµÄ»¯Ñ§Ê½Îª £¬Æ侧Ìå½á¹¹ÓëNaClÏàͬ£¬¶øÈÛµã¸ßÓÚNaCl¡£MÈÛµã½Ï¸ßµÄÔÒòÊÇ ¡£½«Ò»¶¨Á¿µÄ»¯ºÏÎïZX¸ºÔØÔÚMÉÏ¿ÉÖƵÃZX/M´ß»¯¼Á£¬ÓÃÓÚ´ß»¯Ì¼Ëá¶þ¼×õ¥ÓëÔ¹ð´¼õ¥½»»»ºÏ³É̼Ëá¶þÔ¹ðõ¥¡£ÔÚ̼Ëá¶þ¼×õ¥·Ö×ÓÖУ¬Ì¼Ô×Ó²ÉÓõÄÔÓ»¯·½Ê½ÓÐ £¬O¡ªC¡ªOµÄ¼ü½ÇԼΪ £»
£¨3£©×ÆÉÕº¬ÔªËØZµÄÑΣ¬»áʹ»ðÑæ³ÊÏÖÌØÊâµÄÑÕÉ«£¬ÇëÓÃÔ×ӽṹµÄ֪ʶ½âÎöÆäÔÒò£º ¡£
| ÔªËرàºÅ | a | b | c | d | e | f | g | h | i | j |
| Ô×Ӱ뾶/pm | 111 | 77 | 70 | 104 | 143 | 99 | 117 | 186 | 160 | 64 |
| ×î¸ß»¯ºÏ¼Û»ò ×îµÍ»¯ºÏ¼Û |
+2 | -4 | -3 | +6 | +3 | -1 | +4 | +1 | +2 | -1 |
| Ö÷×å ÖÜÆÚ |
¢ñA | ¢òA | ¢óA | ¢ôA | ¢õA | ¢öA | ¢÷A | 0 |
| 1 | ||||||||
| 2 | a a |
b b |
c c |
j j |
||||
| 3 | h h |
i i |
e e |
g g |
d d |
f f |
||
| ||
| ||
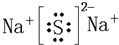
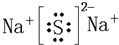


£¨13·Ö£©
µÚËÄÖÜÆÚ¹ý¶ÉÔªËØFe¡¢Ti¿ÉÓëC¡¢H¡¢N¡¢OÐγɶàÖÖ»¯ºÏÎï¡£
£¨1£©¢ÙH¡¢C¡¢N¡¢OËÄÖÖÔªËصĵ縺ÐÔÓÉСµ½´óµÄ˳ÐòΪ ¡£
¢ÚÏÂÁÐÐðÊö²»ÕýÈ·µÄÊÇ ¡££¨Ìî×Öĸ£©
A£®ÒòΪHCHOÓëË®·Ö×Ó¼äÄÜÐγÉÇâ¼ü£¬ËùÒÔCH2OÒ×ÈÜÓÚË®
B£®HCHO ºÍCO2·Ö×ÓÖеÄÖÐÐÄÔ×Ó¾ù²ÉÓÃsp2ÔÓ»¯
C£®C6H6·Ö×ÓÖк¬ÓÐ6¸ö![]() ¼üºÍ1¸ö´ó
¼üºÍ1¸ö´ó![]() ¼ü£¬C2H2ÊǷǼ«ÐÔ·Ö×Ó
¼ü£¬C2H2ÊǷǼ«ÐÔ·Ö×Ó
D£®CO2¾§ÌåµÄÈ۵㡢·Ðµã¶¼±È¶þÑõ»¯¹è¾§ÌåµÄµÍ
¢ÛÇèËᣨHOCN£©ÊÇÒ»ÖÖÁ´×´·Ö×Ó£¬ËüÓëÒìÇèËᣨHNCO£©»¥ÎªÍ¬·ÖÒì¹¹Ì壬Æä·Ö×ÓÄÚ¸÷Ô×Ó×îÍâ²ã¾ùÒÑ´ïµ½Îȶ¨½á¹¹£¬ÊÔд³öÇèËáµÄ½á¹¹Ê½ ¡£
(2) FeÔ×Ó»òÀë×ÓÍâΧÓн϶àÄÜÁ¿Ïà½üµÄ¿Õ¹ìµÀÄÜÓëһЩ·Ö×Ó»òÀë×ÓÐγÉÅäºÏÎï¡£
¢ÙÓëFeÔ×Ó»òÀë×ÓÐγÉÅäºÏÎïµÄ·Ö×Ó»òÀë×ÓÓ¦¾ß±¸µÄ½á¹¹ÌØÕ÷ÊÇ
¢ÚÁùÇèºÏÑÇÌúÀë×Ó[Fe(CN)6]4-Öв»´æÔÚ__________¡£
a¡¢¹²¼Û¼ü b¡¢·Ç¼«ÐÔ¼ü c¡¢Åäλ¼ü d¡¢¦Ò¼ü e¡¢¦Ð¼ü
²¢Ð´³öÒ»ÖÖÓë CN_ »¥ÎªµÈµç×ÓÌåµÄµ¥ÖÊ·Ö×Óʽ______________________¡£
¢ÛÈýÂÈ»¯Ìú³£ÎÂÏÂΪ¹ÌÌ壬È۵㣬·Ðµã
£¬ÔÚ
£ºÒÔÉÏÉý»ª£¬Ò×ÈÜÓÚË®£¬Ò²Ò×ÈÜÓÚÒÒÃÑ¡¢±ûͪµÈÓлúÈܼÁ¡£¾Ý´ËÅжÏÈýÂÈ»¯ÌúµÄ¾§ÌåÀàÐÍΪ___________¡£
£¨3£©¢ÙTiµÄÔÚÖÜÆÚ±íÖÐλÖÃ______________ ¡£
¸ù¾ÝÔªËØÔ×ÓµÄÍâµç×ÓÅŲ¼µÄÌØÕ÷£¬¿É½«ÔªËØÖÜÆÚ±í·Ö³ÉÎå¸öÇøÓò£¬ÆäÖÐTiÊôÓÚ Çø¡£
¢ÚTiµÄÒ»ÖÖÑõ»¯ÎïX£¬Æ侧°û½á¹¹ÈçÉÏͼËùʾ£¬ÔòXµÄ»¯Ñ§Ê½Îª ¡£¹¤ÒµÉÏÀûÓÃXºÍ̼Ëá±µÔÚÈÛÈÚ״̬ÏÂÖÆÈ¡»¯ºÏÎïM£¨M¿É¿´×öÒ»ÖÖº¬ÑõËáÑΣ©,ÖƱ¸MµÄ»¯Ñ§·´Ó¦·½³ÌʽÊÇ________________________________________£»
Ò»¡¢1.D 2.B 3.A 4.B 5.BD 6.B 7.BC 8.B 9.B?
¶þ¡¢10.¢Ù2 2 ?
¢ÚCH
11.2NaCl£«2H2O 2NaOH£«H2¡ü£«Cl2¡ü?
2NaOH£«H2¡ü£«Cl2¡ü?
H2£«Cl2 2HCl?
2HCl?
CaCO3 CaO£«CO2¡ü?
CaO£«CO2¡ü?
C£áO£« C£áC2£«CO¡ü?
C£áC2£«CO¡ü?
CaC2£«2H2O===Ca£¨OH£©2£«C2H2¡ü?
 |
2CH¡ÔCH CH2==CH¨DC¡ÔCH
CH2==CH¨DC¡ÔCH£«HCl CH2==CH¨DCCl==CH2
CH2==CH¨DCCl==CH2

12.(1)CaC2µÄÖÊÁ¿·ÖÊýΪ86%?
(2)ʹ²â¶¨½á¹ûÆ«´ó?
13.£¨1£©B£¨CH3£©3+2HBr B£¨CH3£©Br2+2CH4£»
B£¨CH3£©Br2+2CH4£»
£¨2£©4¡Ã1
14.ÒÀ¾Ý¸÷ÀàÁ´ÌþµÄȼÉÕͨʽ£¬½áºÏÉú³ÉµÄCO2¡¢H2OµÄÌå»ý£¬¿É·ÖÒÔÏÂÇé¿öÌÖÂÛ£º?
£¨1£©ÈôΪÍéÌþ£¬ÓÐ
Ã÷ÏԵأ¬ÓÐ ¡Üx£¼1£¬n=
¡Üx£¼1£¬n=
£¨2£©ÈôΪϩÌþ£¬ÓÐ £¬Ôòx=1£¬n¡Ý2¡£
£¬Ôòx=1£¬n¡Ý2¡£
£¨3£©ÈôΪȲÌþ£¬
Ôò1£¼x¡Ü2£¬n=
¹ú¼ÊѧУÓÅÑ¡ - Á·Ï°²áÁбí - ÊÔÌâÁбí
ºþ±±Ê¡»¥ÁªÍøÎ¥·¨ºÍ²»Á¼ÐÅÏ¢¾Ù±¨Æ½Ì¨ | ÍøÉÏÓк¦ÐÅÏ¢¾Ù±¨×¨Çø | µçÐÅթƾٱ¨×¨Çø | ÉæÀúÊ·ÐéÎÞÖ÷ÒåÓк¦ÐÅÏ¢¾Ù±¨×¨Çø | ÉæÆóÇÖȨ¾Ù±¨×¨Çø
Î¥·¨ºÍ²»Á¼ÐÅÏ¢¾Ù±¨µç»°£º027-86699610 ¾Ù±¨ÓÊÏ䣺58377363@163.com